Maladies tropicales négligées
Les maladies tropicales négligées (souvent désignées sous l'acronyme anglo-saxon NTDs) sont un groupe de diverses maladies tropicales fréquentes au sein des populations à faible revenu dans les régions en développement d'Afrique, d'Asie et d'Amérique. Elles sont causées par divers pathogènes au premier rang desquels les parasites helminthes ou protozoaires, mais également les virus et les bactéries. En Afrique subsaharienne, l'impact de l'ensemble de ces pathologies est comparable au paludisme et à la tuberculose[1]. Certaines de ces pathologies peuvent être prévenues ou traitées par des moyens accessibles aux pays les plus développés, mais non dans les régions les plus pauvres du globe. Dans certains cas pourtant, les traitements sont relativement peu onéreux. Par exemple, le traitement de la bilharziose est de 0,20 $US par enfant et par an en 2007[2]. Cependant, pour la période 2010-2017, le coût du contrôle de ces pathologies à l'échelle mondiale est estimé entre 2 et 3 milliards $US[3].

Ces maladies sont souvent mises en contraste avec les trois grands fléaux mondiaux que sont l'infection par le VIH, la tuberculose et le paludisme, lesquels bénéficient de nombreux fonds de recherche et de traitement. Les maladies tropicales négligées constituent pourtant des comorbidités fréquentes de ces infections[4]. Cependant, on observe de manière sporadique des dons de médicaments nécessaires par certaines compagnies pharmaceutiques et des politiques d'administration de masse ont été efficaces dans plusieurs pays[5].
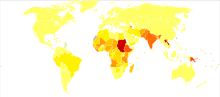
Dix-sept maladies tropicales négligées ont été priorisées par l'OMS. Ces maladies sont considérées comme endémiques dans 149 pays, affectant plus de 1 milliard de personnes dont plus de 500 millions d'enfants[6]. Bien que le poids économique de ces pathologies sur les économies en développement soit difficile à chiffrer, il est estimé à plusieurs milliards de dollars chaque année[7]. Elles ont provoqué 142 000 décès en 2013, chiffre en baisse par rapport aux 204 000 décès en 1990[8]. De ces dix-sept pathologies, deux sont ciblées pour être éradiquées prochainement : la dracunculose d'ici à 2015 et le pian d'ici à 2020. Par ailleurs, quatre sont ciblées pour élimination : le trachome, la maladie du sommeil, la lèpre et la filariose lymphatique d'ici à 2020[7].
Liste des maladies
Il existe un débat au sein de l'OMS, du CDC, et des experts en maladies infectieuses concernant les pathologies à classer comme maladies tropicales négligées. Feasey, chercheur sur le sujet, note treize maladies tropicales négligées: l'ascaridiose, l'ulcère de Buruli, la maladie de Chagas, la dracunculose, l'ankylostomose, la maladie du sommeil, la Leishmaniose, la lèpre, la filariose lymphatique, l'onchocercose, la bilharziose, le trachome, et la trichocéphalose[9]. Fenwick reconnait quant à lui douze maladies tropicales négligées « essentielles »: l'ascaridiose, l'ulcère de Buruli, la maladie de Chagas, la dracunculose, la maladie du sommeil, la Leishmaniose, la lèpre, la filariose lymphatique, l'onchocercose, la bilharziose, le trachome, et la trichocéphalose[10].
Ces pathologies résultent de quatre types de pathogènes: (i) les parasites protozoaires (maladie de Chagas, maladie du sommeil, leishmaniose); (ii) les bactéries (ulcère de Buruli, lèpre, trachome, pian), (iii) les parasites helminthes ou vers (cysticercose/taeniasis, dracunulose, échinococcose, distomatoses, filariose lymphatique, onchocercose, bilharziose, nématodoses instestinales); et (iv) les virus (dengue et chikungunya, rage).
L'Organisation mondiale de la santé (OMS) reconnait les dix-sept pathologies décrites ci-dessous comme maladies tropicales négligée[11].
Protozooses
Trypanosomiase africaine
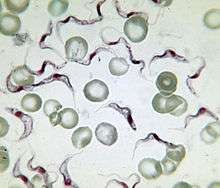
La trypanosomiase africaine est couramment appelée maladie du sommeil. On compte moins de 10 000 cas actuellement[12]. La pathologie est constamment fatale en l'absence de traitement. C'est une maladie vectorielle[13], transmise au cours de la piqûre de glossine, également appelée mouche tsé-tsé.
Les traitements existant sont peu efficaces, notamment en raison du développement de résistances par le parasite, et présentes de nombreux effets indésirables potentiellement graves. Les symptômes les plus fréquents sont la fièvre, les céphalées, des adénopathies, une perturbation du rythme nycthéméral du cycle veille-sommeil, des troubles de la personnalité, un déclin cognitif et en fin d'évolution le coma puis la mort. La maladie peut être diagnostiquée à travers un test sérologique simple.
Trypanosomiase américaine
La trypanosomiase américaine est couramment appelée maladie de Chagas. On estime à 15 millions le nombre d'individus infectés par Trypanosoma cruzi, l'agent de la maladie[9]. La morbidité est supérieure chez les patients immunocompromis, les enfants et les personnes âgées mais très faible en cas de traitement efficace précoce[14]. La maladie de Chagas est d'évolution lente, provoquant l'apparition de symptôme chroniques sur plusieurs années. Il s'agit d'une maladie vectorielle[15],[14] le parasite étant transmis par les fèces d'un triatome infecté. Le protozoaire peut pénétrer dans l'organisme par une brèche cutanée, liée ou non à la piqûre hématophage de l'insecte, ou par les muqueuses. L'infection peut également résulter de l'ingestion de liquide ou de nourriture infectés, voire de l'inhalation de fortes quantités de poussières contenant des fèces de l'insecte[14]. Enfin, on note une proportion non négligeable de transmission verticales au cours de la grossesse, ou encore lors de la transfusion de poches de sang infecté.
Ainsi, la maladie de Chagas peut être prévenue d'abord par l'élimination des foyers domestiques de triatome, l'amélioration des habitats, l'installation de moustiquaires, l'amélioration de l'hygiène alimentaire, et le dépistage, notamment des femmes en âge de procréer et des donneurs de sang[14].
On décrit deux phases à la maladie de Chagas. La phase aiguë est habituellement asymptomatique. Les premiers symptômes sont habituellement le chancre, le chagome, correspondant à un œdème de la paupière unilatéral, des adénopathies locale et la fièvre, accompagnés de différents autres symptômes variés et dépendant du site d'inoculation[14]. On voit le développement d'une phase chronique dans 30 % des infections[9] qui peut se manifester sous trois formes: asymptomatique (le plus fréquent), cardiaque ou digestive[14]. La maladie est de diagnostic difficile, sérologique et microscopique ou par l'objectivation de complications cardiaques ou digestives par imagerie[9]. Bien qu'il soit pourvu d'effets secondaires potentiellement sévères, un traitement existe[14].
Leishmaniose
Les trois formes de leishmaniose sont viscérale (Kala azar), cutanée, et muco-cutanée[16]. On estime à 12 millions le nombre de personnes atteintes[9]. La pathologie est fatale en l'absence de traitement et on estime à 20 000 le nombre de décès annuels[17]. Il s'agit d'une maladie vectorielle[15] transmise lors de la piqûre du phlébotome. Au moins 90 % des leishmanioses viscérales sont réparties entre le Bangladesh, le Brésil, l'Éthiopie, l'Inde, le Soudan et le Soudan du Sud. On retrouve la leishmaniose cutanée en Afghanistan, en Algérie, au Brésil, en Colombie, en Iran, au Pakistan, au Pérou, en Arabie saoudite et en Syrie. Autour de 90 % des leishmanioses cutanéo-muqueuses ont lieu en Bolivie, au Brésil et au Pérou[16].
Le diagnostic repose sur la clinique, les tests sérologiques et l'identification du parasite sur différents prélèvements au premier rang desquels le frottis sanguin et la ponction de moelle osseuse[18]. Des traitements existent mais sont chers, donc relativement peu accessibles aux populations concernées[19]. La prévention repose sur la protection contre les piqûre. De plus, un vaccin est en cours de développement.
Infections bactériennes
Lèpre
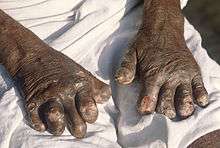
On dénombrait 189 018 cas de lèpre en mars 2013, et 232 857 nouveaux cas étaient diagnostiqués en 2012[20]. On compte 1 à 2 millions d'individus handicapés ou défigurés en raison d'une lèpre active ou passée[21], qu'on retrouve en Angola, au Brésil, en République centrafricaine, en République démocratique du Congo, en Inde, à Madagascar, au Mozambique, au Népal, en Tanzanie[20]. En effet, en l'absence de traitement, la lèpre est une maladie délabrante causée par une bactérie, Mycobacterium leprae. La transmission se fait entre individus par l'intermédiaire de gouttelettes issues de sécrétions nasales et buccales (gouttelettes de Pflügge)[22], l'incubation pouvant alors aller de 5 à 20 ans. Les symptômes sont représentés par une atteinte de la peau, des nerfs, des yeux conduisant à une atrophie tissulaire[22]. Le traitement repose sur une pluri-antibiothérapie[20] mais la maladie est curable à la condition que le traitement soit adapté et précoce[21]. Le vaccin BCG possède un certain effet préventif contre la lèpre.
Ulcère de Buruli
La prévalence de l'ulcère de Buruli est inconnue[9] mais on retrouve cette pathologie en Afrique, en Asie, et en Amérique latine[23].
La maladie est causée par une bactérie[24], Mycobacterium ulcerans, causant des atteintes cutanées à type de nodules puis d'ulcères pouvant se surinfecter et provoquant des difformités responsables de handicaps. Le risque de mortalité est bas, bien que des surinfections de lésions initiales puissent être létales[24]. Le traitement repose sur la chirurgie et les antibiotiques[24] et lorsqu'il est précoce, il permet d'éviter le développement de la majorité des symptômes[24].
Trachome
On estime à 21,4 millions le nombre de personnes atteintes de trachome dont 2,2 millions malvoyants et 1,2 million non voyants. On la retrouve en Afrique, en Asie, en Amérique centrale et du Sud, au Moyen-Orient et en Australie[25]. La maladie atteint préférentiellement les femmes et les enfants[25]. Malgré un pronostic fonctionnel péjoratif, le risque de mortalité est très bas[9],[25].
La maladie est causée par une bactérie, Chlamydia trachomatis, qui se dissémine à partir de sécrétions oculaires sur les mains, les vêtements ou encore les mouches s'abreuvant de ces sécrétions[25]. La symptomatologie consiste en une inflammation de la face interne des paupières provoquant une déformation de la structure de la paupière et une mise en contact des cils avec la cornée qui s’opacifie à force de frottements[25]. Le traitement a recours aux antibiotiques, au premier rang desquels l'azithromycine en collyre. La seule prévention connue consiste en une hygiène personnelle. Des campagnes répétées de traitement et d'éducation des populations concernées semblent n'avoir eu que très peu d'effet tandis que la seule mesure de prévention efficace reste l'accès à une éducation de base des populations atteintes[26].
Pian

Il existe peu de données sur la prévalence du pian mais on sait qu'il affecte préférentiellement les enfants[27]. La maladie est la plus prévalente dans les régions chaudes et humides d'Afrique, d'Asie, d'Amérique du Sud et dans les îles de l'océan pacifique[27].
Il s'agit d'une maladie bactérienne chronique transmise par contact et due à un tréponème, Treponema pallidum pertenue[27]. Le traitement repose sur les antibiotiques (notamment la pénicilline)[27] et la maladie peut être prévenue par de simples mesures d'hygiène individuelle[27]. La symptomatologie est représentée par des lésions cutanées ulcérées sur fond bourgeonnant pouvant le plus souvent se surinfecter et éventuellement s'abcéder[27]. Bien que le risque de mortalité soit bas, le pronostic fonctionnel peut être péjoratif en raison de lésions handicapantes, en plus d'un pronostic esthétique majeur, surtout en cas de lésion faciale[27].
Verminoses
Cysticercose et taeniasis
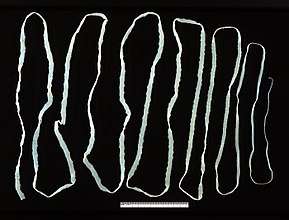
La cysticercose et de manière plus générale les tæniasis sont des maladies parasitaires causées par des vers plats. En effet, c'est la larve de Taenia solium qui est responsable de la cysticercose tandis que le vers adulte de nombreuses espèces telles que Taenia solium ou Taenia saginata pour les plus connues, mais également Hymenolepis nana, Dipylidium caninum ou Diphyllobothrium latum est responsable du tæniasis[28]. Ces maladies sont des helminthiases. La cysticercose représente la première cause évitable d'épilepsie dans les pays en voie de développement[29]. Bien que cosmopolites, ces pathologies se retrouvent principalement en Asie, en Afrique subsaharienne, en Amérique latine[29].
À la différence de la cysticercose qui, dans sa forme neurologique, peut s'avérer fatale, les tæniasis n'entrainent pas le décès du patient[29],[30]. Ces infections se contractent par voie orale par l'ingestion d’œufs de Taenia solium à l'occasion d'un repas contaminé par des selles humaines pour la cysticercose, ou par la consommation de chair de porc, de bœuf ou encore de poisson contaminées pour les tæniasis[28]. La symptomatologie des tæniasis est d'ordinaire assez fruste, incluant douleurs abdominales, nausées, constipation, diarrhées, troubles du sommeil ou encore irritabilité. La cysticercose en revanche, de par son tropisme neuroméningé implique la formation de kystes et de lésions cérébrales pouvant être la cause de céphalées, cécités, épisodes critiques, hydrocéphalie, méningite ou encore de démence[30]. Les médicaments anthelminthiques tels que l'albendazole ou le flubendazole sont utilisés couramment pour traiter ces affections. Une localisation cérébrale de cysticercose fait considérer un traitement immunodépresseur concomitant par corticoïdes[30]. La prévention passe principalement par des mesures d'hygiène incluant l'examen de la viande avant consommation, la cuisson à cœur afin de tuer œufs ou larves, la limitation de l’épandage des excréments humain dans un but de fertilisation des sols ou encore l'accès à un système de tout-à-l'égout efficace[31].
Échinococcose
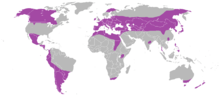
L'échinococcose atteindrait plus d'un million de personnes dans le monde actuellement, particulièrement dans les zones rurales[32]. On regroupe sous le vocable échinococcose principalement deux maladies distinctes causées par deux parasites différents : l'échinococcose alvéolaire (Echinococcus multilocularis) et l'échinococcose kystique ou hydatique ou hydatidose (Echinococcus granulosus). On retrouve l'échinococcose kystique à l'est du pourtour méditerranéen, en Afrique du Nord, dans la moitié sud de l'Amérique du Sud, en Amérique centrale en Asie centrale. L'échinococcose alvéolaire est retrouvée en Chine occidentale et septentrionale, en Russie, en Europe et en Amérique du Nord[33].
La maladie est causée par l'ingestion de parasites présents dans les selles de certains animaux sauvages, classiquement les canidés[33]. Les deux infections impliquent une période d'incubation de plusieurs années. L'échinoccocose cystique provoque, comme son nom l'indique, des kystes hépatiques appelés kystes hydatiques provoquant douleurs abdominales, nausées et vomissements. Ces kystes peuvent également être retrouvés au niveau des poumons, provoquant toux, douleur thoracique et dyspnée. L'échinococcose alvéolaire commence également par un kyste, en général hépatique, qui va progressivement envahir l'organe, provoquant asthénie, douleurs abdominales, nausées et vomissements et pouvant, au terme d'une évolution de plusieurs années, induire une insuffisance hépatique, une cirrhose du foie ou des cancers hépatiques[34]. Ainsi, l'échinococcose non traitée peut être fatale[34]. La maladie est diagnostiquée par les techniques d'imagerie médicale et les tests sérologiques[35]. Le traitement de l'échinoccocose est à la fois chirurgical et médicamenteux concomitamment à la chirurgie par l'administration d'albendazole[34]. La maladie eut être prévenue par la vermifugation des animaux de compagnie, l'amélioration des conditions d'élimination de leurs selles, l'amélioration des conditions d'hygiène globale concernant notamment l'alimentation et la boisson[35].
Dracunculose
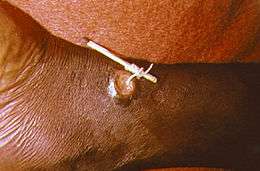
La dracunculose est également connue sous le nom de filariose de Médine. En 2012, les quatre pays endémiques étaient le Tchad, l'Éthiopie, le Mali et le Sud-Soudan[36]. Un programme d'éradication de l'OMS, soutenu par la Fondation Carter a permis de réduire la prévalence et l'incidence de la maladie de façon drastique[36]. Ainsi, on a recensé 113 cas de dracunculose en 2013, chiffre en baisse par rapport aux 542 cas recensés en 2012[36] et en chute libre comparativement aux 3 500 000 cas estimés en 1986[37].
La maladie est dû à une helminthe, Dracunculus medinensis, également appelé filaire de Médine ou ver de Guinée. La transmission a lieu lors de l'ingestion d'eau infestée par des crustacés aquatiques, les cladocères, eux-mêmes infectés par la larve de Dracunculus medinensis[36]. La pathologie n'est pas létale en elle-même, mais peut être la cause d'une inactivité prolongée[36] en raison des plaies durables et handicapantes qu'elle induit. Le traitement consiste en le nettoyage et le bandage des plaies provoquées par l'issue du parasite environ un an après l'infection, en général en zone distale du membre inférieur (classiquement, la zone péri-malléolaire). Ceci est associé à l'extraction très lente du parasite en l'entourant autour d'une petite pièce de bois. L'extraction est de l'ordre du centimètre par jour, le traitement étant ainsi très long, le parasite pouvant mesurer plus d'un mètre de long [36]. Une extraction plus rapide est dangereuse en raison du risque de rupture du parasite qui entraînerait d'importants troubles allergiques chez le patient pouvant conduire au choc anaphylactique puis au décès. La dracunculose peut être prévenue par la filtration de l'eau, l'identification rapide des cas afin de prévenir le risque de dissémination et le traitement des eaux de boissons avec des larvicides. Le cycle du parasite étant long, de l'ordre d'un an, ces méthodes sont rapidement efficaces lorsqu'elles sont suivies à l'échelle d'une population.
Filariose lymphatique
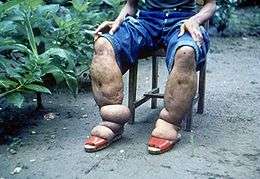
La filariose lymphatique, entraînant l'impressionnant éléphantiasis, touche approximativement 120 millions d'individus[38] dont 40 millions sont atteints de difformités[10]. Ces cas sont répartis pour les deux tiers en Asie du Sud-Est, le tiers restant étant retrouvé en Afrique subsaharienne[38].
La maladie peut-être causée par différentes espèces de nématodes : Wuchereria bancrofti (filaire de Bancroft, la plus fréquente), Brugia malayi (filariose de Malaisie) et Brugia timori[39]. Il s'agit d'une maladie vectorielle transmise par diverses espèces de moustiques des genres Anopheles, Culex, Aedes ou Mansonia[15]. La maladie est rarement fatale[40], mais les dommages liés au parasite perdurent pour le reste de la vie des patients. Ils consistent en des lymphœdèmes des membres, des pathologies génitales et des crises douloureuses. La plupart des patients infectés sont asymptomatiques mais présentent des dommages du système lymphatique et plus de 40 % des patients infectés présentent des dommages rénaux pouvant entraîner une insuffisance rénale[39]. Le diagnostic se fait par l'examen parasitologique du sang de patient, prélevé en milieu de journée ou en milieu de nuit (en général les deux) en fonction de l'espèce infectante considérée[40]. Le traitement historique des filarioses est la diéthylcarbamazine. Toutefois, un traitement antihelmintique à base d'ivermectine ou d'albendazole voire de praziquantel est efficace[41]. Une autre stratégie consiste en l'administration de doxycycline, antibiotique ciblant la Wolbachia, bactérie symbiotique du parasite. La prévention passe par la lutte contre les vecteurs et leurs piqûres et l'administration préventive de filaricides et microfilaricides.
Onchocercose
.png)
L'onchocercose, également connue comme « cécité des rivières », touche environ 37 millions de personnes [9], à 99 % en Afrique subsaharienne[42], notamment dans les zones rurales[42]. La maladie est causée par une filaire, Onchocerca volvulus, transmise par une mouche hématophage du genre Simulie. Ce sont les caractères du vecteur qui expliquent le nom classique de « cécité des rivières », les simulies se retrouvant principalement le long de cours d'eau mouvante, ombragés et aérés. Ainsi, l'onchocercose provoque le déplacement de populations les éloignant de points d'eau douce et l'abandon de villages entiers.
Le parasite provoque à l'état larvaire une cécité, des rashs cutanés, une dépigmentation de la peau et des démangeaisons[43]. La maladie peut être traitée par l'ivermectine[43] et prévenue par l'épandage d'insecticides et l'administration d'antihelminthique à titre préventif[42].
Bilharziose

On décompte plus de 200 millions de cas de bilharziose[10] (également appelée schistosomiase) dans le monde. On estime que 85 % de ces cas sont situés en Afrique sub-saharienne[10] dont très majoritairement des bilharzioses intestinales et urinaires, bien qu'il existe des formes cliniques particulières dues à certaines espèces spécifiques d'autres régions du monde, notamment d'Asie du Sud-Est.
Les différentes espèces de Schistosoma ont un cycle parasitaire complexe où l'humain est hôte définitif tandis que des mollusques d'eau douce font office d'hôte intermédiaire, chaque espèce de schistosome ayant un mollusque différent pour hôte intermédiaire. L'infection a lieu lors du contact cutané avec de l'eau contaminée. Les dommages organiques consécutifs à l'infection ne sont pas tant dus au vers lui-même ou à sa larve mais à l'importante quantité d’œufs produits par les parasites[44]. Les conséquences classiques sont représentées par l'hématurie, l'obstruction vésicale, l'insuffisance rénale, le cancer de vessie, la fibrose péri-portale puis conséquemment l'hypertension portale, l'ascite, les hémorragies digestives hautes consécutives à l'apparition de varices œsophagiennes[9]. Ainsi, la maladie peut-être fatale au terme d'une évolution relativement longue. L'infection par le parasite est également la cause de lésions du col utérin chez la femme et la petite fille, augmentant le risque de transmission du VIH[10].
La maladie peut être diagnostiquée par test sérologique, produisant de nombreux faux positifs, mais également par l'examen direct des selles et des urines (éventuellement des crachats) à la recherche d’œufs[10]. Le praziquantel est utilisé pour traiter les patients atteint de schistosomiase mais ne prévient pas la réinfection. Le coût de prévention est estimé à 0,32 USD par enfant et par an[10] et consisterait en une administration de masse de praziquantel, un meilleur accès à de l'eau propre, une amélioration des conditions d'hygiène et une éducation à la santé des populations concernées[9]. Des vaccins sont également en cours de développement, notamment le Bilhvax.
Nématodoses digestives
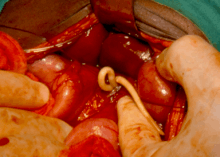
Le terme de nématodose digestive inclut, dans le cadre des maladies tropicales négligées, la trichocéphalose (Trichuris trichiura), l'ascaridiose (Ascaris lumbricoïdes) et l'ankylostomose (Ancylostoma duodenale et Necator americanus)[45]. On estime à 1,5 milliard le nombre d'individus infectés par ces organismes[45]. Les nématodoses digestives sont retrouvées en Afrique subsaharienne, en Amérique centrale et du Sud, en Chine et en Asie du Sud-Est[45].
La transmission de ces vers parasites est généralement due à l'exposition à des selles infectées par voie cutanée ou intestinale (péril fécal), répandues par des pratiques telles que la défécation en plein air ou l’épandage des selles humaines comme engrais agricole[45]. Les symptômes les plus communs sont l'anémie, le retard de croissance, une diminution des capacités physiques ainsi que des performances scolaires et de l'attention[9]. La gravité de la pathologie dépend largement de la charge parasitaire du patient, mais peut inclure des problèmes intestinaux et une asthénie pouvant compromettre le développement physique et cognitif des enfants atteints[45]. Le traitement médicamenteux par flubendazole, albendazole ou ivermectine peut souvent suffire mais le recours à la chirurgie digestive est parfois nécessaire en cas de charge parasitaire très élevée ou de complications digestives[45]. Ces maladies peuvent être prévenues par l'amélioration des conditions d'hygiène domestique et des infrastructures de traitement des eaux usées, par l'accès à l'eau propre et des mesures de préparation alimentaire propre[45]. L'OMS recommande la vermifugation sans diagnostic préalable dans les régions du monde les plus touchées[45].
Viroses
Dengue
On estime entre 50 et 100 millions le nombre d'infections symptomatiques par le virus de la dengue annuellement[46]. On retrouve les cas de dengue principalement en Asie, en Amérique latine et dans le Nord de l'Australie[46].
La dengue est une arbovirose causée par un flavivirus transmise par la piqûre d'un moustique, Aedes aegypti, lors de son repas sanguin[46]. Il n'existe pas de traitement autre que symptomatique[46]. Les symptômes sont peu spécifiques, associant fièvre, céphalées, arthralgies, myalgies, mimant ainsi un syndrome grippal[46]. La dengue n'est pas létale dans la majorité des cas, mais l'infection avec l'un des quatre sérotypes peut augmenter la gravité d'une infection ultérieure par un autre sérotype, résultant en une dengue sévère potentiellement mortelle[46].
Rage
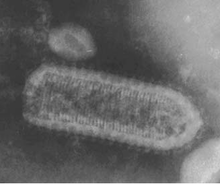
La prévalence est plus élevée dans les zones rurales et affecte prioritairement les enfants d'Asie et d'Afrique[47].
La rage est habituellement fatale après le développement des symptômes[48]. La maladie est causée par un Rhabdoviridae du genre Lyssavirus transmis au travers des blessures ou de morsures par des animaux infectés[47]. Il existe deux formes de rage : furieuse et paralytique. On estime à 60 000 le nombre de victimes de la rage chaque année[49]. Les premiers symptômes sont représentés par la fièvre et la douleur au site d'infection entre 1 et 3 mois après la période d'incubation. La rage furieuse, le type le plus commun de rage, cause hyperactivité, hydrophobie et aérophobie avant que le décès ne survienne par arrêt cardio-respiratoire en quelques jours. La rage paralytique provoque une lente progression vers une paralysie généralisée, puis un coma et enfin le décès[47]. Il est impossible de diagnostiquer une rage avant le début des symptômes mais peut être détecter après le début des symptômes[47]. Elle peut être prévenue par la vaccination des Humains et d'animaux non-humains tels le chien[47] par le nettoyage et la désinfection des blessures (prophylaxie post-exposition)[48], mais il n'existe pas de traitement curatif.
Autres maladies tropicales négligées
Morsure de serpents
L'OMS liste les morsures de serpents comme « autre condition négligée »[50]. Les morsures de serpents sont un problème de santé publique dans les zones rurales d'Afrique et d'Asie du Sud et du Sud-Est. Il n'existe en revanche pas de programme officiel de l'OMS pour le diagnostic, le traitement ou la prévention des morsures de serpent.
Conséquences économiques
Conteh, Engels et Molyneux attribuent le faible coût de traitement des maladies tropicales négligées au nombre important de programmes, la mise à disposition de médicaments gratuite par les compagnies pharmaceutiques, le mode de délivrance des médicaments et la distribution de ceux-ci par des volontaires bénévoles. Ils arguent également du fait que le poids économiques de ces maladies est sous-évalué, permettant mal d'estimer l'impact économique mais également le rapport coût/efficacité des traitements de ces maladies[51]. Le retour sur investissement des mesures de contrôle des NTDs est estimé entre 14 et 30 %, en fonction de la maladie et de la région du monde considérée[52]. Une élimination des verminoses à long terme permettrait une diminution de 25 % de l'absentéisme scolaire et une augmentation du revenu des adultes de 20 %[53].
Cependant, le coût du traitement de certaines de ces maladies, comme l'ulcère de Buruli, peut revenir à plus de deux revenus annuels d'un foyer vivant dans le quartile aux plus faible revenus, alors que dans le quartile aux plus hauts revenus la charge représente un peu moins du revenus annuel moyen par foyer. Ces coûts élevés impactent la qualité du traitement et peuvent mener à une ruine financière. Ces maladies ont également un coût public en termes de développement de programme de santé publique et de perte de productivité de la main-d'œuvre en raison de la morbidité et d'une réduction de l'espérance de vie. Au Kenya, par exemple, on estime qu'une élimination des verminoses permettrait d’augmenter le revenu des adultes de 40 %, représentant un ratio bénéfices/coût de 100 %. On estime à 118 $ la perte de productivité engendrée par chaque cas de trachome. Chaque cas de bilharziose cause une perte de 45,4 jours de travail par an. La plupart des maladies considérées provoquent des pertes économiques des pays en voie de développement se chiffrant par millions de dollars[51].
Impact social
De nombreuses maladies tropicales négligées telles que la lèpre peuvent causer des difformités sévères résultant en une stigmatisation et une mise à l'écart du reste de la société. Un autre exemple frappant est la filariose lymphatique dont les conséquences marginalisent les patients y compris en leur interdisant le travail[10]. Des études au Ghana et au Sri Lanka ont montré que des groupes de soutien aux personnes atteintes de filariose lymphatique peuvent améliorer l'estime de soi des patients, leur qualité de vie et leur relations sociales en leur apportant soutien social et conseils pratiques sur la façon de gérer leur maladie[54].
Les traitements vermifuges sont corrélés à une augmentation de la fréquentation scolaire[10].
L'impact des NTDs est dans certaines situations lié au sexe. Les NTDs affectent particulièrement les femmes, notamment la bilharziose, la dengue ou les helminthiases. Elles sont par ailleurs sujettes aux infections durant la grossesse et il existe un risque de transmission de la mère à l'enfant, notamment dans le cas de la maladie de Chagas[55]. Une étude en Ouganda trouvait que les femmes accédaient plus facilement au traitement en raison d'un temps disponible plus important et d'une plus grande acceptation du traitement, mais l'ignorance d'éventuels effets adverses des médicaments sur les femmes enceintes limitait le recours à des soins adaptés. Ainsi, cet article concluait que le sexe devait entrer en compte dans l'élaboration des protocoles de traitement adapté[56].
Santé publique
La lutte contre les maladies tropicales négligées fait partie d'une des cibles de l'Objectif de développement durable n° 3 de l'ONU.
D'après Fenwick, il sera impossible d'atteindre les objectifs de développement pour le millénaire, tels que l'éducation, la mortalité infantile ou santé maternelle tant que la prévalence des maladies tropicales négligées se maintient au niveau actuel. Il affirme par ailleurs que de nombreux individus souffrent de plusieurs NTDs de façon concomitante[10].
Les traitements vermifuges sont corrélés à la reprise d'un poids physiologique, ce qui est logique considérant que les vers sont responsables en partie de la malnutrition de leur hôte[10],[57]. Cependant, il n'est pas établi que des campagnes de vemifugation de masse améliore les pronostics à long terme[57]. En effet, les preuves manquent encore concernant l'amélioration du poids, du taux d'hémoglobine ou encore des performances scolaires à la suite de ces traitements[57]. Enfin, les traitements vermifuges seuls ne permettront pas d'améliorer à long terme les états de santé des populations concernées si ne sont pas associées des mesures d'amélioration des conditions sanitaires publiques et individuelles.
Hotez milite pour l'inclusion des NTDs au sein des initiatives pour le paludisme, l'infection par le VIH et la tuberculose, tenant compte des nombreux liens existants entre les trois fléaux et les NTDs. Il note également la corrélation existant entre des taux élevés de NTDs et des taux élevés de maladies chroniques non transmissibles telles que des pathologies cardiaques dégénératives ou des cancers. Il attribue cette corrélation aux conséquences à long termes de pathologies inflammatoires telles que les NTDs développant un terrain favorable à des maladies chroniques non transmissibles[55].
Pourquoi ces maladies sont-elle négligées ?
D'après Feasey, ce groupe de maladies est négligé en raison de la population qu'elles touchent, des patients pauvres dans les pays les plus pauvres, mais également en raison d'une attention portée particulièrement sur le contrôle de l'infection par le VIH, la tuberculose et le paludisme[9]. D'après Fenwick, il n'est pas illogique que la lutte contre ces trois grands fléaux ait été privilégiée financièrement eu égard au nombre important de personnes touchées et de la connaissance du public (notamment occidental) de ces trois maladies. Par ailleurs, il suppose que l'importance des maladies tropicales négligées a été sous-estimée puisqu'elles sont souvent asymptomatiques pendant de nombreuses années au cours d'une période d'incubation[10]. Le lien entre un décès et une maladie tropicale négligée d'évolution très lente voire latente, n'est pas souvent réalisé[10]. Dans un article du Financial Times on pouvait lire que le manque d'attrait commercial de ces pathologies et les patients qu'elles touchent limitaient le développement de la recherche et de l'innovation dans ce domaine. Ainsi, la responsabilité de la gestion de ces maladies incombe aux gouvernements ou à des organisations philanthropiques[58].
Prévention
Tandis que Fenwick argue du fait que la prévention et l'éradication sont importantes en raison « de l'épouvantable stigmatisation, la défiguration, la cécité et les déficiences causées par les maladies tropicales négligées »[10], Hotez publie un article en 2013, dans lequel il évoque une potentielle élimination ou éradication de la dracunculose, la lèpre, la filariose lymphatique, l'onchocercose, le trachome, la maladie du sommeil, la leishmaniose viscérale, et la rage dans les dix ans à venir[55]. Un journal dédié maladies tropicales négligées, PLoS Neglected Tropical Diseases, a été lancé en 2007. Il existe également un groupement international dédié au contrôle des NTDs appelé Global Network for Neglected Tropical Diseases Control[9].
Marché et initiatives pharmaceutiques
Les entreprises de biotechnologies ont fait des maladies tropicales négligées une cible en raison du besoin d'amélioration de l'état de santé global des populations issues du monde en développement[59]. L'administration massive de médicaments est considérée comme une méthode possible d'éradication, en particulier concernant la filariose lymphatique, l'onchocercose et le trachome, et ceci malgré le problème potentiel représenté par le développement de résistances aux médicaments[60]. D'après Fenwick, l'entreprise Pfizer aurait donné gracieusement 70 millions de doses de médicaments en 2011 afin d'éliminer le trachome, dans le cadre de l’International Trachoma Initiative[10]. L'entreprise Merck a aidé l’African Programme for the Control of Onchocerciasis (APOC) et Onchocerciasis Elimination Program for the Americas (OEPA) en faisant don d'ivermectine[10]. L'entreprise aurait également promis de mettre à disposition 200 millions de comprimés de praziquantel sur 10 ans[10]. Le groupe GlaxoSmithKline a fait don de deux milliards de comprimés pour le traitement de la filariose lymphatique et promis 400 millions de comprimés anthelminthiques pour la période 2010 - 2015. Le groupe Johnson & Johnson aurait promis 200 millions de comprimés anthelminthiques par an[10]. Novartis aurait promis la mise à disposition d'un traitement de la lèpre. L'entreprise EISAI s'engage à mettre à disposition deux milliards de comprimés de traitement contre la filariose lymphatique[10].
Actions politiques
Il existe de nombreuses campagnes de prévention et d'éradication soutenues par l'Organisation Mondiale de la Santé×, l'Agence des États-Unis pour le développement international, la fondation Bill-et-Melinda-Gates ou encore le Département du Développement international britannique[10].
La Food and Drug Administration (FDA) américaine émet des « bons d'avis de priorité » visant à inciter les compagnies à investir dans la recherche de nouveaux médicaments et vaccins pour les maladies tropicales. Ainsi, la FDA a la possibilité de délivrer ces bons à n'importe quelle compagnie pharmaceutique obtenant une autorisation de mise sur le marché pour un traitement d'une des maladies listées. Ce bon peut être utilisé plus tard par la compagnie afin d'accélérer la procédure d'autorisation par la FDA de n'importe quelle molécule, même sans rapport avec les NTDs. Ce programme concerne toutes les maladies tropicales, y compris le paludisme et la tuberculose. Le premier bon ainsi délivré l'a été pour le Coartem, un traitement anti-paludique[61]. Le terme « négligé » n'est pas utilisé dans la définition du programme bien que la majorité des maladies listées font en fait partie du groupe des maladies tropicales négligées selon la définition de l'OMS.
Organisations Non Gouvernementales
Il existe actuellement deux ONG se concentrant exclusivement sur les maladies tropicales négligées[62] : Schistosomiasis Control Initiative (SCI) et Deworm the World Initiative (DtWI). Malgré un manque de fonds financiers patent, le traitement et la prévention des maladies tropicales négligées est « coût/efficace ». Le coût du traitement d'un enfant atteint d'une helminthiase ou d'une bilharziose est par exemple inférieur à 0,50 USD par année lorsqu'il est administré dans le cadre d'administration de masse au sein de la population scolaire par DtWI. Ce programme est recommandé par Giving What We Can et le Consensus de Copenhague comme une des solutions à la fois les plus efficaces et les plus « coût/efficaces ». Les efforts de SCI pour lutter contre les maladies tropicales négligées inclus l'usage de kit dits « d'impact rapide » contenant quatre ou cinq médicaments et une formation des enseignants sur la manière de les administrer.
Initiatives public-privé
En 2013, le gouvernement japonais, cinq compagnies pharmaceutiques japonaises, la Bill & Melinda Gates Foundation et le PNUD ont établi un nouveau partenariat public-privé nommé Global Health Innovative Technology Fund (GHIT). Les membres ont ainsi engagé cent millions de dollars sur cinq ans destinés à financer des partenariats de recherche et développement au Japon et ailleurs afin de travailler sur de nouveaux médicaments et vaccins de dix-sept maladies tropicales négligées en plus du VIH, du paludisme et de la tuberculose[63],[64],[65]. Le faible coût des vaccins et médicaments ainsi développés est un des critères majeurs à l'obtention des financements[63].
WIPO Re:Search est un programme fondé en 2011 par l'Organisation mondiale de la propriété intellectuelle (OMPI) en collaboration avec BIO Ventures for Global Health (BVGH) et la participation de compagnies pharmaceutiques majeures et d'autres organisations de recherche privées ou publiques. Ce programme permet aux organismes de partager leur propriété intellectuelle, leurs composés, leur expertise, leurs infrastructures et leur expérience de manière libre de droit avec des chercheurs qualifiés internationaux dans le domaine des NTDs, du paludisme et de la tuberculose[66],[67].
Notes et références
- Hotez PJ, Kamath A, « Neglected tropical diseases in sub-saharan Africa: review of their prevalence, distribution, and disease burden. », PLoS Negl Trop Dis., vol. 3(8), (PMID 19707588, lire en ligne)
- (en) « Making the Case to Fight Schistosomiasis », National Public Radio, (lire en ligne)
- Hotez PJ, « A plan to defeat neglected tropical diseases. », Sci Am., vol. 302(1), , p. 90-94, 96 (PMID 20063641, lire en ligne)
- Mike Shanahan, « Beat neglected diseases to fight HIV, TB and malaria », SciDev.Net,
- (en) M. Reddy, S. S. Gill, S. R. Kalkar, W. Wu, P. J. Anderson et P. A. Rochon, « Oral drug therapy for multiple neglected tropical diseases: a systematic review. », JAMA, vol. 298, no 16, , p. 1911-1924 (PMID 17954542, lire en ligne)
- http://www.dndi.org/
- http://www.who.int/neglected_diseases/about/en/
- Collaborators GBD 2013 Mortality and Causes of Death, « Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013. », Lancet, vol. 385, no 9963, , p. 117–71 (PMID 25530442, DOI 10.1016/S0140-6736(14)61682-2)
- Feasey N, Wansbrough-Jones M, Mabey DC, Solomon AW, « Neglected tropical diseases. », Br Med Bull, vol. 93, , p. 179-200 (PMID 20007668, lire en ligne)
- Fenwick A, « The global burden of neglected tropical diseases. », Public Health, vol. 126, no 3, , p. 233-236 (PMID 22325616, lire en ligne)
- Reddy et Gill 2007, Table 1. Key Features of 13 Neglected Tropical Diseases Listed by Prevalence
- « Human African Trypanosomiasis: number of new cases falls to historical low in 50 years »
- name="WorldHealthDay2014"
- « Chagas disease (American trypanosomiasis) » (consulté le 12 mars 2014)
- « World Health Day 2014: small bite, big threat » (consulté le 12 mars 2014)
- « Burden and Distribution » (consulté le 16 mars 2014)
- « Leishmaniasis » (consulté le 16 mars 2014)
- « Diagnosis, detection and surveillance » (consulté le 16 mars 2014)
- « Access to essential antileishmanial medicines and treatment » (consulté le 16 mars 2014)
- « Leprosy Today » (consulté le 16 mars 2014)
- « Leprosy: the disease » (consulté le 16 mars 2014)
- « Leprosy »
- « Buruli Ulcer Endemic Countries » (consulté le 12 mars 2014)
- « Buruli Ulcer » (consulté le 12 mars 2014)
- « Priority eye diseases » (consulté le 16 mars 2014)
- Goldschmidt P, Einterz E, « The limits of medical interventions for the elimination of preventable blindness. », Trop Med Health, vol. 42, no 1, , p. 43-52 (PMID 24808746, lire en ligne)
- « Yaws » (consulté le 16 mars 2014)
- « Transmission of taeniasis/cysticercosis » (consulté le 13 mars 2014)
- « About Taeniasis/cysticercosis » (consulté le 13 mars 2014)
- « Signs, symptoms and treatment of taeniasis/cysticercosis » (consulté le 13 mars 2014)
- « Surveillance, prevention and control of taeniasis/cysticercosis » (consulté le 13 mars 2014)
- « Echinococcosis » (consulté le 16 mars 2014)
- « Transmission of echinococcosis » (consulté le 16 mars 2014)
- « Signs, symptoms and treatment of echinococcosis » (consulté le 16 mars 2014)
- « Surveillance, prevention and control of echinococcosis » (consulté le 16 mars 2014)
- « Dracunculiasis » (consulté le 13 mars 2014)
- « Dracunculiasis eradication — global surveillance summary, 2009 », Wkly. Epidemiol. Rec., World Health Organization, vol. 85, no 19, , p. 166–76 (PMID 20449943, lire en ligne [PDF])
- « Epidemiology » (consulté le 16 mars 2014)
- « Lymphatic filariasis » (consulté le 16 mars 2014)
- « Forms of Lymphatic Filariasis and diagnosis » (consulté le 16 mars 2014)
- Mohammed KA, Hail HJ, Gabrielli AF. et al., « Triple Co-Administration of Ivermectin, Albendazole and Praziquantel in Zanzibar: A Safety Study », PLoS Negl Trop Dis, vol. 2, no 1, , e171 (PMID 18235853, PMCID 2217668, DOI 10.1371/journal.pntd.0000171)

- « Onchocerciasis » (consulté le 16 mars 2014)
- « Onchocerciasis » (consulté le 16 mars 2014)
- « Schistosomiasis Fact Sheet », CDC, Division of Parasitic Diseases (consulté le 3 décembre 2008)
- « Soil-transmitted helminth infections » (consulté le 16 mars 2014)
- « Dengue Control » (consulté le 12 mars 2014)
- « About rabies » (consulté le 16 mars 2014)
- « Rabies » (consulté le 16 mars 2014)
- « Rabies » (consulté le 16 mars 2014)
- WHO, « The 17 neglected tropical diseases », sur WHO, WHO (consulté le 24 octobre 2014)
- Conteh L, Engels T, Molyneux DH, « Socioeconomic aspects of neglected tropical diseases. », Lancet, vol. 375, no 9710, , p. 239-47 (PMID 20109925, lire en ligne)
- Molyneux DH, « "Neglected" diseases but unrecognised successes--challenges and opportunities for infectious disease control. », Lancet, vol. 364, no 9431, , p. 380-3 (PMID 15276399, lire en ligne)
- « Deworm the World: the evidence for school-based deworming »
- Weiss MG, « Stigma and the social burden of neglected tropical diseases », PLoS Negl Trop Dis, vol. 2, no 5, , e237 (PMID 18478049, PMCID 2359851, DOI 10.1371/journal.pntd.0000237, lire en ligne)

- Hotez PJ, « NTDs V.2.0: "blue marble health"--neglected tropical disease control and elimination in a shifting health policy landscape. », PLoS Neglected Tropical Diseases, vol. 7, no 11, (PMID 24278496, lire en ligne)
- Rilkoff H, Tukahebwa EM, Fleming FM, Leslie J, Cole DC, « Exploring gender dimensions of treatment programmes for neglected tropical diseases in Uganda », PLoS Negl Trop Dis, vol. 7, no 7, , e2312 (PMID 23875047, PMCID 3708858, DOI 10.1371/journal.pntd.0002312, lire en ligne)

- DC Taylor-Robinson, N Maayan, K Soares-Weiser, S Donegan et P Garner, « Deworming drugs for soil-transmitted intestinal worms in children: effects on nutritional indicators, haemoglobin and school performance. », The Cochrane database of systematic reviews, vol. 11, , CD000371 (PMID 23152203, DOI 10.1002/14651858.CD000371.pub5)
- http://www.ft.com/intl/cms/s/0/07bfe8f2-5e05-11e4-bc04-00144feabdc0.html#axzz3MMnaQdHZ
- Frew SE, Liu VY, Singer PA, « A business plan to help the 'global South' in its fight against neglected diseases », Health Aff (Millwood), vol. 28, no 6, , p. 1760–73 (PMID 19887417, DOI 10.1377/hlthaff.28.6.1760, lire en ligne)
- Keenan JD, Hotez PJ, Amza A, et al., « Elimination and eradication of neglected tropical diseases with mass drug administrations: a survey of experts », PLoS Negl Trop Dis, vol. 7, no 12, , e2562 (PMID 24340111, PMCID 3855072, DOI 10.1371/journal.pntd.0002562, lire en ligne)

- « FDA Approves Coartem Tablets to Treat Malaria », USFDA (consulté le 11 décembre 2009)
- « Giving What We Can; recommended interventions »
- "Japan in pioneering partnership to fund global health research", by Andrew Jack, Financial Times, May 30, 2013
- "An Audience with… Tachi Yamada", by Asher Mullard, Nature magazine, September 2013, Volume 12, p. 658
- "Joining the Fight Against Neglected Diseases", Science magazine, June 7, 2013, Volume 340, p. 1148
- Ramamoorthi R, Graef KM, Dent J, « WIPO Re:Search: Accelerating anthelmintic development through cross-sector partnerships. », Int J Parasitol Drugs Drug Resist., vol. 4, no 3, , p. 220-5 (PMID 25516832, lire en ligne)
- « WIPO Re:Search » (consulté le 16 mars 2015)
Article connexe
- Global Network for Neglected Tropical Diseases
Liens externes
- Portail de la médecine
- Portail de l’humanitaire
- Portail de la microbiologie
- Portail de l’Afrique
- Portail de l’Asie
- Portail de l’Amérique
- Portail de la parasitologie