Aedes aegypti
Aedes aegypti est une espèce de moustique qui est le vecteur principal de la dengue, du virus Zika, du chikungunya et de la fièvre jaune.

| Règne | Animalia |
|---|---|
| Embranchement | Arthropoda |
| Classe | Insecta |
| Ordre | Diptera |
| Famille | Culicidae |
| Genre | Aedes |
| Sous-genre | Aedes (Stegomya) |
Nom binominal
(Linnaeus, 1762)
C'est un petit moustique, long de 5 mm environ, de couleur sombre que l'on peut reconnaître par les marques blanches bien visibles sur les pattes et un dessin en forme de lyre sur le thorax (ce dernier détail le distingue du moustique tigre Aedes albopictus avec lequel il peut être confondu, alors que celui-ci possède à la place une ligne blanche longitudinale sur son thorax et sa couleur générale noire est plus foncée). Il est originaire d'Afrique[1], mais on le trouve maintenant dans les régions tropicales à travers le monde[2].
Ce moustique est considéré comme un des plus importants vecteurs de maladies. Il a un mode de vie qui le rend particulièrement proche de l'homme et, comme la plupart des moustiques, semble pouvoir rapidement développer des résistances à la plupart des insecticides. On cherche donc à mieux comprendre son écologie. Seule la femelle pique.
Génomique
Le génome de cette espèce de moustique a été séquencé par un consortium comprenant des scientifiques de l'Institut J. Craig Venter et de l'université Notre-Dame et publié en 2007. L'effort de séquençage de son ADN était destiné à fournir de nouvelles pistes pour la recherche sur les insecticides et les modifications génétiques possibles pour prévenir la propagation du virus. Il s'agissait de la deuxième espèce de moustique dont le génome ait été séquencé en entier (le premier était Anopheles gambiae). Les données publiées incluent les 1,38 milliard de paires de base contenant les 15 419 gènes codant des protéines. Le séquençage indique que l'espèce a divergé de Drosophila melanogaster (la mouche à fruit commune) il y a environ 250 millions d'années, et qu'Anopheles gambiae et cette espèce ont divergé il y a environ 150 millions d'années[3],[4].
Cycle de vie
De la larve issue de l'œuf au moustique adulte, il se passe 7 à 12 jours selon les conditions, notamment la température et l'alimentation. Cet insecte holométabole se reproduit en grand nombre et rapidement, ce qui lui permet d'évoluer rapidement pour s'adapter aux variations de son environnement (et à l'arrivée des pesticides anti-moustiques)[5] ; il existe un lien fonctionnel et important entre les capacités des adultes et l'écologie des larves, les microbes qu'elles rencontrent et parfois intègrent dans leur microbiote, et plus généralement les conditions environnementales auxquelles elles sont exposées[6],[7] et la variation phénotypique d'insectes holometaboliques vecteurs de maladies zoonotiques[8].
Ponte
La femelle de Aedes aegypti pond ses œufs qui peuvent éclore très rapidement en environ 24 heures si les conditions sont optimales.
Larves
Elles passent par différents stades jusqu'à la nymphe d'où émergera le moustique adulte.
La niche écologique de la larve est très différente de celle du futur moustique adulte qui n'est plus du tout aquatique (les adultes femelles iront faire un repas de sang chez divers animaux ou dans les habitations humaines) ; le stade larvaire est le moment de formation du microbiote[9] qui influera sur la "fitness[Quoi ?]" de l'animal, c'est à dire son adaptation au milieu : les conditions environnementales rencontrées par les larves lors de leur développement affectent les « traits » adultes[8].
La larve d' A. aegypti rencontre des communautés bactériennes différente selon son environnement larvaire, lesquelles vont influer sur la capacité du futur adulte à véhiculer des agents pathogènes vers l'humain. Ainsi des larves expérimentalement exposées à différents isolats bactériens indigènes lors de leur développement ont donné des adultes présentant des différences significatives de taux de pupaison et en termes de taille corporelle (mais non en termes de durée de vie)[8]. L'exposition de larves de ce moustique à un isolat d'Enterobacteriaceae a entraîné chez les moustiques adultes une diminution de l'activité antibactérienne de l'hémolymphe et un titre réduit de propagation du virus de la dengue[8].
Adulte
Sa durée de vie dans la nature estimée à 2 à 3 semaines au maximum.
Mais il peut vivre bien plus longtemps, environ 2 à 3 mois en conditions de laboratoire[10].
Vecteur de maladies
Ce moustique qui peut piquer plusieurs fois une même personne ou des personnes différentes est réputé vecteur de nombreux virus susceptibles d'affecter l'homme.
Cas de la dengue
L’Institut Pasteur étudie les migrations de moustiques par le biais de marqueurs génétiques, pour mieux comprendre la propagation de certaines maladies, dont la dengue (4 sérotypes de dengue) qui connaît une recrudescence dans certaines régions tropicales, et dont on peut craindre une extension de l'aire de répartition avec le phénomène de réchauffement climatique.
Selon les premiers résultats qui montrent par exemple que les sous-populations d'Aedes aegypti en Polynésie n'ont pas d'échanges génétiques importants entre les îles, la propagation du virus de la dengue serait favorisée par les déplacements de voyageurs infectés, plutôt que par la migration d'insectes. Cependant, le ministère de la Santé français déclare en 2010 le « premier cas de dengue autochtone » en métropole française (les autres cas déjà signalés sur le territoire étaient des personnes ayant voyagé dans les régions du monde touchées par l'épidémie)[11] . La dengue importée par ce moustique avait déjà touché le continent européen, notamment la Grèce en 1881, 1889, 1895-1897 et 1910, et particulièrement 1927-1928 avec une épidémie d'une gravité sans précédent : plus d'un million de personnes furent malades et on comptabilisa environ 1500 morts[12].
Un projet du gouvernement malaisien, consistant en l'introduction de deux à trois mille mâles de cette espèce, porteurs d'une modification génétique réduisant la durée de vie de leurs descendants, est à l'étude et pourrait être mis en œuvre dans le cadre de la lutte contre la dengue[13].
Virus Zika
Aedes aegypti transmet le virus Zika, comme les autres moustiques du genre Aedes[14].
Prévention
Elle passe surtout par le contrôle des populations urbaines, périurbaines et villageoises de moustiques, en favorisant leurs prédateurs et en limitant les habitats qui les favorisent. Les moustiquaires pré-traitées, les anti-moustiques sont des solutions locales. L'usage de pesticides est ponctuellement efficace, mais présente le risque d'affecter les prédateurs des moustiques, de susciter d'autres problèmes liés à la toxicité ou l'écotoxicité de ces produits, ou d'être inutiles face à l'émergence de souches résistantes par sélection naturelle.
Des micro-solutions se développent aussi : par exemple, dans les cimetières aux Antilles et en Guyane, ne pas remplir les vases des plantes avec de l'eau mais avec du sable mouillé ou gravier assez fin qui donnent d'aussi bons résultats sans risque de développement de larves. Les fleurs en plastique sont à disposer dans du sable ou dans un pot dont le fond est muni d'un large trou afin qu'il n'accumule pas d'eau. Les soucoupes ou bacs disposés sous les pots de fleurs peuvent être couverts d'un voile de tulle, ou l'eau (là où elle ne manque pas) peut être changée régulièrement, etc.
Transgénisation
L'entreprise britannique Oxitec, étroitement liée au géant agrochimique Syngenta, a mis au point une lignée de moustiques Aedes aegypti mâles, rendus stériles par transgénèse, qui permettraient de contrôler la population des moustiques vecteurs. Elle a déposé une demande de commercialisation au Brésil en juillet 2013. Le 10 avril 2014, la Commission technique nationale de biosécurité (CNB) a autorisé, par seize voix contre une, la dissémination dans l'environnement de ces moustiques de nom de code OX513A. Pour être effective, cette autorisation doit néanmoins encore être validée par l’Agence nationale de surveillance sanitaire (Anvisa). OX513A deviendrait alors le premier « animal » génétiquement modifié qui pourrait être dispersé dans la nature.
Tentatives d'éradication
La Fondation Rockefeller en 1916[15] puis l'Organisation panaméricaine de la santé au milieu du XXe siècle[15],[16] ont tenté en vain d'éradiquer Aedes aegypti. Pour ce faire, l'Organisation panaméricaine de la santé a notamment vaporisé du dichlorodiphényltrichloroéthane (DDT), insecticide qui a été interdit depuis[16].
Galerie
 Larve
Larve Adulte
Adulte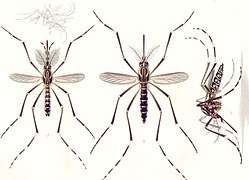 Mâle à gauche, femelles à droite
Mâle à gauche, femelles à droite
Références
- (en) L. Mousson, C. Dauga, T. Garrigues et al., « Phylogeography of Aedes (Stegomyia) aegypti (L.) and Aedes (Stegomyia) albopictus (Skuse, Diptera: Culicidae) based on mitochondrial DNA variations », Genet. Res., vol. 86, no 1, , p. 1–11 (PMID 16181519, DOI 10.1017/S0016672305007627, lire en ligne).
- (en) M. Womack, « The yellow fever mosquito, Aedes aegypti », Wing Beats, vol. 5, no 4, , p. 4.
- Heather Kowalski, Scientists at J. Craig Venter Institute Publish Draft Genome Sequence from Aedes aegypti, Mosquito Responsible for Yellow Fever, Dengue Fever, J. Craig Venter Institute, (lire en ligne).
- V. Nene, J. R. Wortman, D. Lawson et al., « Genome sequence of Aedes aegypti, a major arbovirus vector », Science, vol. 316, no 5832, , p. 1718–1723 (PMID 17510324, DOI 10.1126/science.1138878).
- N. A. Moran (1994), Adaptation and constraint in the complex life cycles of animals. Annu. Rev. Ecol. Syst. 25, 573–600.
- A. J. Crean, K. Monro, D. J. Marshall (2011), Fitness consequences of larval traits persist across the metamorphic boundary. Evolution 65, 3079–3089 .
- De Block M & Stoks R(2005), Fitness effects from egg to reproduction: Bridging the life history transition. Ecology 86, 185–197.
- Laura B. Dickson, Davy Jiolle, Guillaume Minard, Isabelle Moltini-Conclois, Stevenn Volan, Amine Ghozlane, Christiane Bouchie, Diego Ayala, Christophe Paupy, Claire Valiente Moro & louis Lambrechts (2017), Carryover effects of larval exposure to different environmental bacteria drive adult trait variation in a mosquito vector | Science Advances | 16 aout 2017 | Vol. 3, no. 8, e1700585 | DOI: 10.1126/sciadv.1700585 |URL:http://advances.sciencemag.org/content/3/8/e1700585.full |résumé
- G. Minard, P. Mavingui, C. V. Moro (2013), Diversity and function of bacterial microbiota in the mosquito holobiont. Parasit. Vectors 6, 14.
- Dossier questions-réponses sur la dengue en guyane établi par l'inpes, Document validé par la DGS, l'AFFSAPS, le SDD et la DSDS de la Guyane. Le 15 novembre 2006.
- « DENGUE - Premier cas non importé en France métropolitaine à Nice », Le Point.fr, (lire en ligne).
- Claude Chastel, En 1927-1928, la dengue s'abattait sur la Grèce: les enseignements d'une épidémie, Bulletin de l'Académie nationale de médecine, vol. 193, no 2, 2009, p. 485-493.
- Louise Cuneo, « Des moustiques génétiquement modifiés au chevet de la dengue », Le Point.fr, (lire en ligne)
- Christian Losson, « Virus zika : l’OMS piquée au vif », Libération.fr, (lire en ligne).
- André Yébakima, La dengue dans les départements français d’Amérique : comment optimiser la lutte contre cette maladie ?, IRD Éditions, (lire en ligne).
- Audrey Garric, « Et si on éradiquait tous les moustiques ? », Blogs Le Monde.fr, (lire en ligne).
Liens externes
- (en) Référence Animal Diversity Web : Aedes aegypti (consulté le )
- (en) Référence Catalogue of Life : Aedes aegypti (Linnaeus, 1762) (consulté le )
- (en) Référence Fauna Europaea : Aedes aegypti (consulté le )
- (en) Référence GISD : espèce Aedes aegypti (consulté le )
- (fr) Référence INPN : Aedes aegypti (Linnaeus, 1762) (consulté le )
- (fr+en) Référence ITIS : Aedes aegypti (Linnaeus, 1762) ( ) (consulté le )
- (en) Référence NCBI : Aedes aegypti (consulté le )
- (en) Référence uBio : Aedes aegypti (Linnaeus, 1762) (consulté le )
- Institut Pasteur
- « Lien vers photo et base de donnée génomique »(Archive • Wikiwix • Archive.is • Google • Que faire ?) (consulté le 30 mars 2013)
- Entomologie médicale
- Portail de l’entomologie
- Portail de la parasitologie