Vitamine E
La vitamine E est une vitamine liposoluble recouvrant un ensemble de huit molécules organiques, quatre tocophérols et quatre tocotriénols. La forme biologiquement la plus active est l'α-tocophérol, la plus abondante dans l'alimentation étant le γ-tocophérol. Ces molécules sont présentes en grande quantité dans les huiles végétales. Elles agissent, parallèlement à la vitamine C et au glutathion, essentiellement comme antioxydants contre les dérivés réactifs de l'oxygène produits notamment par l'oxydation des acides gras.

Découverte
En 1922, l'embryologiste Herbert McLean Evans (en) et son assistante Katharine Scott Bishop, de l'université de Californie à Berkeley, constatent que chez des rats soumis à un régime appauvri en lipides, les femelles peuvent tomber enceintes mais aucun fœtus ne se développe. Cependant, les grossesses arrivent à terme quand le régime est supplémenté avec des feuilles de laitue ou du germe de blé. Les deux scientifiques soupçonnent l'existence d'un composé lipophile, qu'ils nomment Facteur X, indispensable au développement du fœtus.
En 1924, indépendamment des recherches de Herbert Evans et Katharine Bishop, Bennett Sure, de l'université de l'Arkansas, montre qu'un composé retiré d'un régime alimentaire induit la stérilité chez les rats mâles. Bennett Sure nomme ce composé Vitamine E, les lettres A, B, et C étant déjà utilisées, et la lettre D étant pressentie pour un facteur antirachitique. La vitamine E reçoit aussi le nom de tocophérol, du grec tokos : progéniture et pherein : porter.
Herbert Evans et Oliver Emerson réussissent à isoler la vitamine E à partir de l'huile de germe de blé en 1936, et Erhard Fernholz en détermine la structure en 1938. La même année, le Prix Nobel de chimie Paul Karrer réalise la synthèse de l'alpha-tocophérol racémique. Ce n'est qu'en 1968 que la vitamine E est reconnue comme un élément nutritif essentiel pour l'homme par le National Research Council des États-Unis.
Structure
La vitamine E existe sous huit formes naturelles, quatre tocophérols et quatre tocotriénols :
|
Les tocophérols sont constitués d'un noyau chromanol et d'une chaîne latérale saturée à seize atomes de carbone. Les tocotriénols diffèrent des tocophérols par la présence de trois doubles liaisons sur cette chaîne latérale. La vitamine E fait référence à la fois aux tocophérols et aux tocotriénols, qui présentent une activité alpha-tocophérol. En raison de la teneur en hydrogène du 2H-1-benzopyran-6-Ole, ces composés présentent différents niveaux d'activité antioxydante en fonction de l'emplacement et du nombre de groupes méthyle et du type d'isoprénoïdes.[1]
La différence entre les formes alpha, bêta, gamma et delta réside dans le nombre et la position des groupes méthyle sur le noyau chromanol :
- Structure et dénomination des quatre tocophérols :
Substituants des tocophérols R1 R2 R3 Nom 
CH3 CH3 CH3 α-tocophérol CH3 H CH3 β-tocophérol H CH3 CH3 γ-tocophérol H H CH3 δ-tocophérol
- Structure et dénomination des quatre tocotriénols :
Substituants des tocotriénols R1 R2 R3 Nom 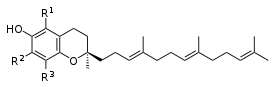
CH3 CH3 CH3 α-tocotriénol CH3 H CH3 β-tocotriénol H CH3 CH3 γ-tocotriénol H H CH3 δ-tocotriénol
Rôles
Antioxydant
L'organisme produit continuellement des radicaux libres, composés très réactifs comportant des électrons célibataires. Les radicaux libres endommagent des composants cellulaires aussi divers que les protéines, les lipides ou l'ADN. Les réactions radicalaires se propagent en chaîne : les molécules déstabilisées par un électron célibataire deviennent à leur tour des radicaux libres. Les antioxydants ont pour rôle de stopper ce processus en neutralisant les radicaux libres, pour réduire leur nocivité. Ainsi, la vitamine E a la capacité de capter et de stabiliser (par résonance) l'électron célibataire des radicaux libres, suivant la réaction :
Le tocophérol porteur d'un radical peut réagir avec un nouveau radical libre pour former une espèce neutre, ou être régénéré par la vitamine C, le glutathion ou le coenzyme Q10.
La vitamine E joue principalement son rôle d'antioxydant dans les membranes biologiques. Les mitochondries, qui sont génératrices de radicaux libres, contiennent de forts taux de vitamine E dans leur membrane lipidique, constituée d'acides-gras polyinsaturés et soumis au stress oxydant.
La vitamine E est souvent utilisée comme conservateur alimentaire (E306 à E309) pour éviter le rancissement des aliments par les radicaux libres.
Additif
De la vitamine E synthétique peut être utilisée comme additif alimentaire sous les noms suivants (officiels pour l'Union européenne[2]) :
- « acétate de tout-rac-α-tocophéryle », dénommé « Vitamine E/Acétate d'alpha-tocophéryle totalement racémique » avant 2015 ;
- « acétate de RRR-α-tocophéryle », autrefois dénommé «Vitamine E/Acétate de RRR-alpha-tocophéryle» ;
- « RRR-α-tocophérol », autrefois dénommé « vitamine E/RRR-alpha-tocophérol ».
Utilisation médicale
Elle est prescrite soit en milligrammes soit en unités internationales : 1 UI de vitamine E est l'équivalent biologique d'environ 0,667 mg de d-alpha-tocophérol (²⁄₃ mg exactement), ou de 1 mg de dl-alpha-tocophérol acétate.
En plus de son rôle antioxydant, la vitamine E évite l'agrégation excessive des plaquettes responsable des thromboses, a une action protectrice sur les globules rouges et pourrait prévenir, par ce biais les maladies cardio-vasculaires d'origine athéromateuse. En pratique, cependant, aucune action en ce sens n'a été démontrée[3]. De plus, elle augmenterait le taux d'accident vasculaire cérébral de type hémorragique[4].
La vitamine E a également un effet bénéfique sur le taux de cholestérol. Bien que les observations de Evans aient montré l'importance de la vitamine E sur la fécondité de certains animaux, aucun effet n'a été mis en évidence chez l'Homme.
Elle pourrait aussi protéger de la maladie de Parkinson en empêchant l'oxydation des acides gras oméga-3 et du fer.
Une étude de 2011[5] sur la maladie d'Alzheimer montre une plus faible concentration en vitamine E chez les personnes atteintes d'Alzheimer que les personnes en bonne santé. Les chercheurs pensent que les huit formes de la vitamine E pourraient protéger de la maladie ou ralentir son évolution, bien plus efficacement qu'en utilisant de l'alpha-tocophérol seul.
Elle est utilisée en complément de traitements antidépresseurs lorsque l'action de ceux-ci est insuffisamment opérante[réf. nécessaire].
Elle aurait également une certaine efficacité sur les stéatoses non alcooliques, permettant de freiner leur progression vers la cirrhose[6].
La vitamine E est utilisée dans le traitement médical de la maladie de La Peyronie avec effet positif sur la douleur.
La carence en vitamine E occasionne des problèmes neuromusculaires tels que des myopathies (dégénerescence du tissu musculaire), des troubles de la rétine ou du système immunitaire[7].
Limites recommandées
L'EFSA dans un rapport de 2006[8] recommande de ne pas dépasser 270 mg/j.
Le NIH américain recommande[9] de ne pas dépasser 1 500 UI/j pour les sources naturelles et 1 100 UI/j pour les formes synthétiques.
Polémique sur la dangerosité des suppléments en vitamine E
Une action favorable sur la prévention de certains cancers a été suspectée dans un premier temps[10] mais non confirmée par les études les plus récentes[11],[12].
L'étude SELECT[13] a été stoppée en 2008 car elle montrait un risque accru de cancer de la prostate avec des suppléments de vitamine E synthétique (400 UI/j) et/ou de sélénium (200 µg/j)[14],[15]. En , ces mêmes chercheurs publient[16] une explication sur les résultats :
- la complémentation en sélénium a augmenté le risque de cancer chez ceux qui avaient déjà des taux de sélénium élevés au départ, mais n’avait aucun effet chez les hommes qui avaient de bas niveaux de sélénium ;
- la vitamine E seule a augmenté le risque de cancer chez ceux qui avaient peu de sélénium au départ, ce qui n'était pas le cas de ceux qui prenaient à la fois du sélénium et de la vitamine E. Le sélénium protégerait donc des effets nocifs de la vitamine E.
Une méta-analyse publiée en 2005 montre qu'à trop fortes doses (apports supérieurs à 400 UI/j), la vitamine E sous forme d'alpha-tocophérol seul pourrait augmenter la mortalité globale[17].
Cette méta-analyse a été critiquée par la communauté scientifique[18] :
- les essais cliniques avec moins de dix décès étaient exclus de l'analyse, la méta-analyse ne porte ainsi que sur seulement dix-neuf études entre 1966 et 2004 ;
- la méthode d’analyse (régression logistique hiérarchique) choisie n'est pas utilisée habituellement dans ce type de travail. Si on utilise deux méthodes habituelles (variance inverse de Wolfe et Mantel Haenszel), les suppléments de vitamine E ne sont plus associés à une mortalité accrue ;
- les études utilisées portaient sur des personnes en très mauvaise santé. Les conclusions ne peuvent pas être extrapolées à la population en bonne santé.
Teneurs en vitamine E
La vitamine E est présente dans les huiles végétales, principalement dans l'huile de figue de barbarie, l'huile de germe de blé, d'argousier, l'huile de palme non raffinée (rouge) et dans les huiles d'argan, de tournesol, de soja, d'arachide ou d'olive. On la trouve aussi en moindre quantité dans les céréales, les amandes, les légumes verts, le beurre, la margarine, les poissons gras.
Les carences en vitamine E sont rarement observées. D'une part, l'alimentation couvre largement les besoins journaliers[réf. nécessaire] (de l'ordre de 15 mg/j chez l'adulte), d'autre part, cette vitamine stockée par le foie et dans les graisses est peu détruite par l'organisme. Pour les cas de carence, on trouve cependant dans les circuits pharmaceutiques de l'acétate de tocophérol à raison de 500 mg par capsule à prendre quotidiennement pendant un mois.
Le tableau ci-dessous présente les aliments possédant la plus importante teneur en vitamine E. Les valeurs sont indiquées en mg de vitamine E pour 100 g d'aliment (pour rappel, 1 mg = 1,49 UI).
| Aliment | Teneur en mg pour 100 g |
Aliment | Teneur en mg pour 100 g |
|---|---|---|---|
| Huile de germe de blé | 133,0 | Soja sec | 8,5 |
| Huile de palme rouge (non raffinée) | 105,0 | Arachide fraîche | 8,1 |
| Huile d'argousier (argousier) | 100 | Thon | 6,3 |
| Huile d'argan | 90,0 | Mûre | 3,5 |
| Huile de tournesol | 48,7 | Crème fraîche | 3,5 |
| Huile de pépins de raisin | 28,8 | Avocat | 3,2 |
| Pollen frais de ciste | 27,8 | Asperge | 2,5 |
| Germe de blé | 27,0 | Épinard | 2,0 |
| Huile de palme (raffinée) | 25,6 | Persil | 1,8 |
| Margarine | 25,0 | Beurre | 1,5 |
| Huile d'olive | 21,7[19] | Cervelle | 1,2 |
| Noisette et amandes sèches | 20,0 | Œuf et fromage | 1,0 |
| Huile de colza | 18,4 | Tomate et chou | 1,0 |
| Germe de maïs et d'orge | 15,0 | Cassis | 1,0 |
| Huile d'arachide | 13,0 | Farine de blé complète | 1,0 |
| Soja | 11,0 | ||
Notes et références
- (sw) Val Snow, « Vitamin E », sur Healthy Food Near Me, (consulté le )
- « Règlement d'exécution (UE) 2015/1747 de la Commission du 30 septembre 2015 portant rectification de l'annexe du règlement (UE) n° 26/2011 en ce qui concerne l'autorisation de la vitamine E en tant qu'additif pour l'alimentation de toutes les espèces animales », document 32015R1747, sur EUR-Lex, (consulté le ).
- (en) Sesso HD, Buring JE, Christen WG et al., « Vitamins E and C in the prevention of cardiovascular disease in men: The Physicians' Health Study II Randomized Controlled Trial », JAMA, 2008, 300:2123-2133
- (en) Schürks M, Glynn RJ, Rist PM, Tzourio C et Kurth T, « Effects of vitamin E on stroke subtypes: meta-analysis of randomised controlled trials », BMJ, 2010, 341:c5702
- « Les 8 formes de la vitamine E pourraient protéger de la maladie d'Alzheimer », sur Lanutrition.fr (consulté le ).
- (en) Sanyal AJ, Chalasani N et Kowdley KV, « Pioglitazone, vitamin E, or placebo for nonalcoholic steatohepatitis », N. Eng. J. Med., 2010, 362:1675-1685.
- « Découverte d'une fonction majeure de la vitamine E », sur Lanutrition.fr (consulté le ).
- http://www.efsa.europa.eu/sites/default/files/efsa_rep/blobserver_assets/ndatolerableuil.pdf
- « Office of Dietary Supplements - Vitamin E », sur Nih.gov (consulté le ).
- (en) Heinonen OP, Albanes D, Virtamo J et al., « Prostate cancer and supplementation with alpha-tocopherol and beta-carotene: incidence and mortality in a controlled trial », J. Natl. Cancer Inst., 1998, 90:440-446
- (en) Lippman SE, Klein EA, Goodman PJ et al., « Effect of selenium and vitamin E on risk of prostate cancer and other cancers, The Selenium and Vitamin E Cancer Prevention Trial (SELECT) »], JAMA, 2009, 301:39-51
- (en) Gaziano JM, Glynn RJ, Christen WG et al., « Vitamins E and C in the prevention of prostate and total Cancer in men, The Physicians' Health Study II Randomized Controlled Trial », JAMA, 2009, 301:52-62
- « Selenium and Vitamin E Cancer Prevention Trial (SELECT) : Questions and Answers », sur National Cancer Institute (consulté le ).
- « Vitamine E synthétique et sélénium à doses élevées peuvent augmenter le risque de cancer de la prostate », sur Lanutrition.fr (consulté le ).
- (en) Klein EA, Thompson IM Jr., Tangen CM et al., « Vitamin E and the risk of prostate cancer: The selenium and vitamin E cancer prevention trial (SELECT) »], JAMA, 2011, 306:1549-1556
- (en) Kristal AR, Darke AK, Morris JS, Tangen CM, Goodman PJ, Thompson IM, Meyskens FL Jr., Goodman GE, Minasian LM, Parnes HL, Lippman SM et Klein EA., « Baseline Selenium Status and Effects of Selenium and Vitamin E Supplementation on Prostate Cancer Risk », J. Natl. Cancer Inst., 22 février 2014, 106(3)
- (en) Miller ER, Pastor-Barriuso R, Dalal D et al., « Meta-analysis: high-dosage vitamin E supplementation may increase all-cause mortality », Ann. Intern. Med., 2005, 142:37-46.
- http://www.lanutrition.fr/bien-comprendre/les-complements-alimentaires/les-verites-du-dr-fricker-et-du-pr-cynober/le-dr-fricker-et-le-pr-cynober-ont-ils-tout-dit-sur-ces-13-substances/page-13.html
- ANSES, « Anses Table Ciqual 2016 Composition nutritionnelle des aliments », sur pro.anses.fr (consulté le )
Voir aussi
- Portail de la biochimie
- Portail de la médecine
- Portail de la chimie