Composé organosulfuré
Un composé organosulfuré est un composé organique qui comporte au moins un atome de soufre.
Les composés organosulfurés sont souvent associés à une mauvaise odeur mais beaucoup de composés les plus doux sont des dérivés organosulfurés. Le soufre étant très important dans la chimie du vivant, ces composés sont très abondants dans la nature. Deux des vingt acides aminés sont des composés organosulfurés. Les combustibles fossiles comme le pétrole, le charbon et le gaz naturel, produits par la fossilisation d'êtres vivants, contiennent ainsi toujours des composés organosulfurés et leur élimination est un des enjeux majeurs de leur raffinage.
Le soufre fait partie du groupe des chalcogènes avec l'oxygène et il est attendu que les composés organosulfurés aient des similarités avec les composés oxo correspondants, ce qui est vrai dans une certaine mesure. Formellement, dans tout composé comportant un ou plusieurs atomes d'oxygène, celui-ci peut être remplacé par du soufre pour donner un composé organosulfuré.
Le test chimique classique pour la détection de composés soufrés est la méthode halogène de Carius.
Familles
Les composés organosulfurés peuvent être classés en fonction du groupe fonctionnel comportant le soufre ; ils sont listés ci-dessous par ordre décroissant de leur occurrence.
Thioéthers, thioesters et thioacétals
Les thioéthers sont caractérisés par une liaison C-S-C. Ils sont aussi appelés « sulfure », par exemple (CH3)2S = sulfure de diméthyle ou thioéther méthylique. La liaison C-S est plus longue parce que l'atome de soufre est plus gros, et plus faible qu'une liaison carbone-oxygène. En moyenne, les longueurs de liaison dans les composés soufrés sont de 183 pm pour la liaison simple C-S dans le méthanethiol à 173 pm dans le thiophène. L'énergie de dissociation de la liaison C-S pour le méthanethiol est de 370 kJ/mol (89 kcal/mol) à comparer aux 420 kJ/mol (100 kcal/mol) de la liaison C-H dans le méthane et quand l'hydrogène est remplacé par un groupe méthyle (sulfure de diméthyle), cette énergie décroit à 305 kJ/mol (73 kcal/mol)[1].
La liaison simple C-O est plus courte que la liaison C-C. Les énergies de dissociation de liaison pour le sulfure de diméthyle (thioéther méthylique) et le éther méthylique sont respectivement de 305 et 322 kJ/mol (73 et 77 kcal/mol).
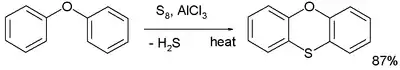
Les thioéthers sont typiquement préparés par alkylation de thiols. Ils peuvent être aussi préparés par un réarrangement de Pummerer. Dans une réaction nommée la réaction de Ferrario, le phénoxybenzène est converti en phénoxathiine par action du soufre élémentaire et de chlorure d'aluminium[2] :
Les thioesters sont de trois types : les plus courants ont pour formule générale R-C(=O)-S-R' et sont dits « S-thioester ». Cependant, il en existe de formule R-C(=S)-O-R' (« O-thioester ») et même R-C(=S)-S-R' qui sont dénommés dans ce dernier cas, « dithioester ».
Les thioacétals, qui sont très utiles pour l'inversion de polarité des groupes carbonyle (umpolung), sont une famille spéciale de thioéthers comme de thioesters. Ils ont pour formule générale R-C(-OR)-SR'. Les composés de formule R-C(-SR)-SR' sont appelés « dithioacétals ».
Les thiophènes sont une famille de thioéthers à part parce qu'ils sont aromatiques. L'énergie de stabilisation par résonance du thiophène est de 121 kJ/mol (29 kcal/mol) à comparer aux 84 kJ/mol (20 kcal/mol) pour le composé oxygéné homologue, le furane. La raison de cette différence est l'électronégativité de l'oxygène qui attire les électrons au détriment du courant de cycle aromatique. A contrario, comme substituant aromatique, l'atome de soufre est moins efficace comme attracteur d'électrons que l'atome d'oxygène.
Thiols, disulfures et polysulfures
Les thiols contiennent le groupe R-SH. Ils sont structuralement similaires aux alcools mais leurs propriétés chimiques sont très différentes. Les thiols correspondants sont plus nucléophiles, plus acides et plus facilement oxydés. Leurs acidité peut différer de cinq unités de pKa[3].
La différence d'électronégativité entre le soufre (2,58) et l'hydrogène (2,20) est petite. Par conséquent, il n'y a pas de liaisons hydrogène dans les thiols.
Des thiols aliphatiques forment des couches mono-moléculaires sur l'or, ce qui est à l'étude en nanotechnologie.
Certains thiols aromatiques peuvent être obtenus via une réaction de Herz.
Les disulfures (R-S-S-R) avec une liaison covalente soufre-soufre sont importants dans les phénomènes de réticulation :
- en biochimie, pour le repliement et la stabilité de certaines protéines ;
- en chimie des polymères, pour la vulcanisation du caoutchouc.
Des chaînes de soufre plus longues sont aussi connues, comme dans le composé naturel varacine qui comporte un cycle pentathiépine inusuel (une chaîne de cinq soufres cyclisée sur une cycle benzène).
Doubles liaisons C=S
Les doubles liaisons entre le carbone et le soufre sont relativement inhabituelles car de tels composés tendent à s'oligomériser et/ou à polymériser. Des exceptions à cette règle sont le disulfure de carbone, l'oxysulfure de carbone, le thiophosgène et la thiobenzophénone. Les liaisons C=S stabilisées par résonance sont plus courantes, comme celles des thioamides (voir ci-dessous) et composés apparentés.
Les thiocétones possèdent la structure générale RC(=S)R'. Ces composés sont relativement rares contrairement à leurs homologues oxgénés. Les thioaldéhydes (RC(=S)H) sont encore plus rares, reflétant leur manque de protection stérique.
Les thioamides de formule générale R1C(=S)N(R2)R3 et les radicaux R peuvent des atomes d'hydrogène sont plus communs. Ils sont typiquement préparés par la réaction d'amides avec le réactif de Lawesson.
Des doubles liaisons C=S existent dans les ylures de sulfonium, par exemple dans la réaction de Johnson-Corey-Chaykovsky (en).
Acides sulfoniques, sulfonates et sulfonamides
Les acides sulfoniques possèdent le groupe RS(=O)2OH. Ce sont des acides forts qui sont habituellement solubles dans les solvants organiques. Des acides sulfoniques comme l'acide trifluorométhanesulfonique (acide triflique et triflates) ou l'acide para-toluènesulfonique (acide tosylique et tosylates) sont des réactifs fréquemment utilisés en synthèse organique. En médecine, les sulfamidés (sulfamides) sont des composés courants, la plupart dérivant de sulfonations aromatiques.
Sulfaranes et persulfaranes
Les sulfaranes comportent un groupe fonctionnel relativement spécialisé, ce sont des composés contenant du soufre tétravalent de formule SR4[4] et de même, les persulfuranes sont hypervalents (hexavalent) avec une formule SR6.
Les persulfuranes tout carbone ont été connus après les plus lourds représentants du groupe des chalcogènes, par exemple le composé hexaméthylpertellurane (Te(Me)6) a été obtenu en 1990[5] par réaction entre le tétraméthyltellurane et le difluorure de xénon qui donne Te(Me)4F2, suivi d'une réaction avec le diméthylzinc. L'homologue soufré, l'hexaméthylpersulfurane (SMe6) est prévu comme étant stable[6] mais n'a pas encore été, à ce jour[7], synthétisé.
Le premier persulfurane tout carbone réellement synthétisé en laboratoire est celui avec deux méthyles et deux ligands bisphényle[8] :

Il a été préparé à partir du sulfurane correspondant 1 qui réagit avec un mélange difluorure de xénon/trifluorure de bore dans l'acétonitrile pour donner le dication sulfuranyle 2 qui réagit avec le butyllithium dans le tétrahydrofurane pour former le persulfurane 3 stable et sous forme de l'isomère cis. La diffractométrie de rayons X montre que les longueurs des liaisons C-S sont de 189 et 193 pm (plus longues que les liaisons C-S standards) avec un atome de soufre au centre dans une géométrie octaédrique distordue.
In silico, des expériences suggèrent que ces liaisons sont très polaires avec une charge négative sur les atomes de carbone.
Composés organosulfurés naturels
Tous les composés organosulfuré ne sont pas des polluants de mauvaise odeur. Des composés comme l'allicine et l'ajoène sont la cause de l'odeur de l'ail et la lenthionine contribue au parfum des champignons shiitaké. Beaucoup de ces composés organosulfurés naturels ont aussi des propriétés médicinales importantes comme de prévenir l'agrégation des plaquettes du sang ou dans la lutte contre le cancer.
Pollutions dues aux composés organosulfurés
Des composés organiques sulfurés présents dans l'environnement sont générés comme sous-produits de procédés industriels comme la fabrication de plastiques et des pneus, mais la majorité des organosulfurés présents dans l'environnement sont des composés naturels car le soufre étant essentiel à la vie, de nombreuses biomolécules en contiennent.
De tels composés organosulfurés odorants sont aussi produits par la cokéfaction du charbon, opération qui permet de le débarrasser des composés sulfurés et d'autres impuretés volatiles dans le but d'obtenir du « charbon pur » (coke), principalement utilisé dans la fabrication de l'acier.
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Organosulfur compounds » (voir la liste des auteurs).
- Handbook of Chemistry and Physics, 81e éd., CRC Press (ISBN 0-8493-0481-4).
- Phenoxthin, Organic Syntheses, vol. 2, p. 485 (1943) ; vol. 18, p. 64 (1938).
- Janssen, M.J., Organosulfur chemistry. Reviews of current research, Interscience, New York, 1967.
- Par exemple, le bis[2,2,2-trifluoro-1-phenyl-1-(trifluoromethyl)ethoxy]-diphenyl-sulfurane, Organic Syntheses, vol. 6, p. 163 (1988) ; vol. 57, p. 22 (1977).
- Latif Ahmed et John A. Morrison, Synthesis and characterization of hexamethyltellurium(VI), J. Am. Chem. Soc., 1990, vol. 112(20), p. 7411-7413. Résumé.
- Fowler, J. E. ; Schaefer, H. F., III et Raymond, K. N., The S6 Point Group Conformers of the Hexamethylchalcogens: Me6S, Me6Se, Me6Te, Inorg. Chem., 1996, vol. 35(2), p. 279-281, DOI:10.1021/ic940240d.
- Au 20 octobre 2009.
- Sato, S. ; Matsunaga, K. ; Horn, E. ; Furukawa, N. et Nabeshima, T., Isolation and Molecular Structure of the Organo-persulfuranes [12-S-6(C6)], J. Am. Chem. Soc., 2006, vol. 128(21), p. 6778-6779, DOI:10.1021/ja060497y
Voir aussi
- Acide sulfénique de formule générale RSOH
- Thiosulfinate de formule générale R-S(=O)-S-R'
- Mercaptan (Thiol)
- Méthanethiol
- Éthanethiol
- Butane-1-thiol
- Butyl séléno-mercaptan
- Thio-
- Thioséléniure
| CH | He | |||||||||||||||||
| CLi | CBe | CB | CC | CN | CO | CF | Ne | |||||||||||
| CNa | CMg | CAl | CSi | CP | CS | CCl | CAr | |||||||||||
| CK | CCa | CSc | CTi | CV | CCr | CMn | CFe | CCo | CNi | CCu | CZn | CGa | CGe | CAs | CSe | CBr | CKr | |
| CRb | CSr | CY | CZr | CNb | CMo | CTc | CRu | CRh | CPd | CAg | CCd | CIn | CSn | CSb | CTe | CI | CXe | |
| CCs | CBa | * | CLu | CHf | CTa | CW | CRe | COs | CIr | CPt | CAu | CHg | CTl | CPb | CBi | CPo | CAt | Rn |
| Fr | CRa | * * |
Lr | Rf | Db | CSg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| ↓ | ||||||||||||||||||
| * | CLa | CCe | CPr | CNd | CPm | CSm | CEu | CGd | CTb | CDy | CHo | CEr | CTm | CYb | ||||
| * * |
Ac | CTh | CPa | CU | CNp | CPu | CAm | CCm | CBk | CCf | CEs | Fm | Md | No | ||||
| Liaison de base en chimie organique | Nombreuses utilisations en chimie |
| Recherche académique, mais pas d'usage courant | Liaison inconnue / non évaluée |
- Portail de la chimie
- Portail des odeurs, des senteurs et du parfum