Stent
Un stent, endoprothèse vasculaire[1], extenseur vasculaire ou tuteur vasculaire, est un dispositif, le plus souvent métallique, maillé et tubulaire, glissé dans une cavité naturelle humaine (ou animale) pour la maintenir ouverte. Il s'agit donc, le plus souvent, d'un support[2] artériel[3]. Il est essentiellement utilisé dans des artères au cours d'une angioplastie, dans le cas de la maladie coronarienne par exemple. Il peut également être employé dans l'urètre, les canaux biliaires… Il est appelé communément « ressort ».


Cet article parle essentiellement des stents vasculaires, c'est-à-dire positionnés dans une artère.
Avant-propos
Stent est un ancien terme anglais décrivant un support. Dans la littérature médicale, le nom de Charles Thomas Stent (en), un dentiste anglais du XIXe siècle[4] est parfois évoqué comme étant à l'origine du terme.
En français, on parle souvent d'endoprothèse artérielle, par contre, le terme prothèse est réservé à un dispositif artificiel destiné à remplacer un membre, un organe ou une articulation.
Historique
La première angioplastie coronaire a été faite par Andreas Gruentzig le 16 septembre 1977 à Zurich. Le premier stent est le WallStent développé par Hans Wallsten à Lausanne[5] par Medinvent en collaboration avec Ulrich Sigwart et l'ingénieur Christian Imbert. Le Wallstent a été introduit en 1985 par Rousseau à Toulouse en vasculaire périphérique puis en coronaire en 1986 par Jacques Puel à Toulouse[6] et Sigwart à Lausanne[7] afin de traiter les dissections artérielles et les resténoses. La démonstration effective de la diminution du risque de resténose est faite vers 1993 (études Benestent[8] et Stress). Le premier stent « actif » (c'est-à-dire enrobé d'un médicament) a été testé en 2001 (résultats publiés en 2002[9]).
Mode d'action
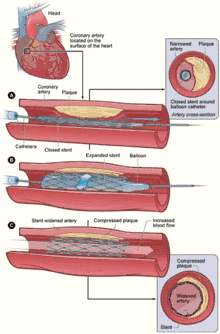
L'angioplastie est la procédure permettant de dilater une artère rétrécie à l'aide d'un ballon qu'on gonfle dans cette dernière, écrasant ainsi la plaque d'athérome responsable de la sténose. Le principal inconvénient de cette technique est le taux important de resténose, c'est-à-dire de récidive du rétrécissement (près de la moitié des cas). Cette dernière peut être précoce (retour élastique de l'artère après dégonflage du ballon) ou tardive (par prolifération des cellules de la paroi de l'artère (endothélium) et surtout par rétraction cicatricielle.
Le stent est un ressort métallique qui est positionné sur un ballon d'angioplastie dégonflé. Lors du gonflage de ce dernier dans l'artère, il se dilate et empêche le retour élastique de la sténose. Le ballon est alors retiré et le stent reste en place. Il peut être mis d'emblée (stenting direct) ou après une dilatation par un premier ballon. La mise en place d'un stent se fait sous radioscopie et n'allonge pas sensiblement la procédure d'angioplastie.
S'agissant d'un matériel étranger au corps humain, c'est un point d'appel naturel à la formation d'un caillot. Un traitement empêchant l'apparition de ce dernier reste donc indispensable pendant au moins plusieurs semaines, jusqu'à ce que le métal soit naturellement recouvert par les cellules de la paroi interne de l'artère (endothélialisation). Ce traitement est à base d'aspirine à petites doses, associé historiquement à la ticlopidine. Actuellement l'association de choix comporte de l'aspirine et un autre antiagrégant plaquettaire (clopidogrel, prasugrel ou ticagrelor).
Types de stents
Un stent se caractérise par son diamètre (une fois déplié) et sa longueur.
Il est constitué d'un maillage métallique. Ce dernier est soit en acier inoxydable, soit en alliage (cobalt-chrome, platine-chrome) [10] ou nitinol (alliage nickel titane) qui a la propriété d'avoir une mémoire de forme[11].
Des stents à base de plastique biodégradable (dits « stents biorésorbables ») et disparaissant au bout de plusieurs années[12] sont aussi utilisés. Ils ont l'avantage d'éviter les resténoses fréquentes avec les stents métalliques[13].
Les stents actifs
Certains modèles sont recouverts d'une substance médicamenteuse antiproliférative, réduisant notablement le risque de resténose. Cette substance est incluse dans un polymère qui est plaqué sur le maillage métallique. En moyenne la resténose est diminuée de 55 à 65 %[14]. La première génération des stents de ce type sont à base de paclitaxel ou de sirolimus. La seconde est à base d'évérolimus[15] et de zotarolimus. On parle ainsi de stents actifs ou de stents coatés (francisation du terme anglais : coated stent = stent habillé, l'autre appellation anglaise étant drug-eluting stent = endoprothèse artérielle à élution médicamenteuse).
Leur mécanisme implique l'emploi de deux anti-agrégants plaquettaires combinés de manière prolongée (au moins un an). Il existe aujourd'hui des stents dont le revêtement en polymère est biodégradable[16] et dont les résultats, à court terme, sont équivalents aux stents de deuxième génération[17].
Ces molécules inhibent la prolifération de l'intima de l'artère, permettant, théoriquement, la couverture complète du maillage du stent par un intima régulier (« endothélialisation »), ce qui diminue très sensiblement, à terme, le risque de formation d'un caillot (thrombus), permettant, alors, d'alléger, le traitement antiagrégant. Mais la substance peut dépasser son but et inhiber trop fortement cette endothélialisation et laissant des parties du stent complètement découverte, avec alors un risque de thrombose à long terme[18].
Avantages
Le stent diminue de façon très sensible la fréquence de resténose après angioplastie. Il est d'utilisation très courante au cours d'une angioplastie.
Il n'existe pas d'allergie. Bien que métallique, il ne gêne pas la réalisation d'une IRM (hormis certains stents posés avant les années 2000 ; il vous sera alors demandé les références du ou des stents posés).
Inconvénients
Outre les problèmes secondaires à l'angioplastie, le risque essentiel est celui de la récidive de sténose (resténose) de l'artère, qui n'est pas complètement éliminé, même avec les stents actifs. Cette resténose est essentiellement due à une prolifération cellulaire à l'intérieur du stent. L'occlusion aiguë par formation d'un caillot est plus rare si le traitement est bien suivi. Elle peut être traitée par une nouvelle angioplastie, parfois aidée par des techniques complémentaires (utilisation d'un ballon « coupant »), avec implantation d'un nouveau stent (pouvant être actif). Historiquement, des tentatives de prévention de cette resténose par irradiation locale par rayonnement bêta ont été faites à la fin des années 1990. Cette technique, appelée brachythérapie, est tombée progressivement en désuétude depuis l'apparition des stents actifs.
La mise sous médicaments anti-agrégants plaquettaires, consécutive à l'implantation d'un stent, augmente le risque de saignement en cas de traumatisme ou en cas de chirurgie, rendant cette dernière beaucoup plus délicate. L'arrêt prématuré des anti-agrégants expose à un risque important de la formation d'un caillot dans le stent (thrombose intra-stent) qui peut alors occlure l'artère (entraînant un infarctus du myocarde s'il s'agit d'une artère coronaire).
Un inconvénient non négligeable de ces dispositifs reste leur prix : de l'ordre de 800 euros pour un stent nu jusqu'à près de 1 600 euros pour un stent actif en 2005.
Cas des stents actifs
Les stents actifs semblent avoir une discrète augmentation de risque d'occlusion par rapport aux stents nus au-delà d'un an[19], ce qui incite à penser que le traitement par Clopidogrel doit sans doute être plus prolongé et que les indications de ces stents doivent être précisées. Cela pourrait être dû à une réendothélisation incomplète et très retardée des mailles[20], celles-ci restant « à nu » durant une période prolongée, favorisant la formation de caillots. Plusieurs études retrouvent un risque de mortalité à trois ans plus élevé avec les stents actifs qu'avec les stents nus[21] (risque relatif augmenté de 18 %[22]). Ce risque est dû en partie aux thromboses tardives de stent qui ont un risque de 0,6 % et qui se cumulent chaque année (1,8 % à trois ans).
Les stents actifs, dits « de deuxième génération », auraient un risque moindre de thrombose tardive[23],[24].
Divers
En novembre 2007 a été diffusé aux États-Unis le premier spot publicitaire concernant un dispositif médical spécifique, un type précis de stent actif, destiné au grand public. Cette diffusion a fait l'objet d'une controverse dans le milieu médical[25].
Notes et références
- « endoprothèse vasculaire », Office québécois de la langue française (consulté le 16 septembre 2017)
- Définition de stent dans Futura science
- http://www.dr-azencott.com/fr/l--endoprothese-221.html Définition de stent sur le site du Dr Azencott, chirurgien vasculaire
- (en) Merriam-Webster Online Dictionary
- Hans Wallstén, un Suédois génial qui crée des emplois en Pays de Vaud « Ma grande chance est d'avoir été à la fois un inventeur et un gestionnaire », 24H, 3 mai 1997.
- J Puel, B Lacapère, M Sabathier, R Schmitt, J P Monassier, B Valeix, P Labrunie, J P Bounhoure, « [Coronary revascularization at the acute phase of myocardial infarction. Short and median-term survival of 359 patients. Multicenter study] », Archives des maladies du cœur et des vaisseaux, vol. 79, no 4, , p. 409-417 (ISSN 0003-9683, PMID 3090958)
- (en) U Sigwart, J J Goy, L Finci, M Blanc, M Grbic, F Stumpe, « Mechanical emergency recanalization of the left main coronary artery », Clinical cardiology, vol. 9, no 5, , p. 217-220 (ISSN 0160-9289, PMID 2940042)
- (en) P W Serruys, P de Jaegere, F Kiemeneij, C Macaya, W Rutsch, G Heyndrickx, H Emanuelsson, J Marco, V Legrand, P Materne, « A comparison of balloon-expandable-stent implantation with balloon angioplasty in patients with coronary artery disease. Benestent Study Group », The New England journal of medicine, vol. 331, no 8, , p. 489-495 (ISSN 0028-4793, PMID 8041413, DOI 10.1056/NEJM199408253310801, lire en ligne)
- (en) Morice MC, Serruys PW, Sousa JE et al. A randomized comparison of a sirolimus-eluting stent with a standard stent for coronary revascularization, N Engl J Med, 2002;346:1773–80.
- (en) Stefanini GG, Holmes DR, « Drug-eluting coronary-artery stents », N Engl J Med. 2013; 368:254-265
- émission Le magazine de la santé du 16 mai 2016
- Serruys PW, Garcia-Garcia HM, Onuma Y, From metallic cages to transient bioresorbable scaffolds: change in paradigm of coronary revascularization in the upcoming decade?, Eur Heart J, 2012;33:16-25b
- (en) Waksman R, Pakala R, « Biodegradable and bioabsorbable stents », Curr Pharm Des., vol. 16, no 36, , p. 4041-51. (PMID 21208182, DOI 10.2174/138161210794454905)
- Utilisation des stents actifs. Consensus d'experts de la Société Française de Cardiologie. Octobre 2007
- (en) Grube E, Sonoda S, Ikeno F, Honda Y, Kar S, Chan C, Gerckens U, Lansky AJ, Fitzgerald PJ, « Six- and twelve-month results from first human experience using everolimus-eluting stents with bioabsorbable polymer », Circulation, vol. 109, no 18, , p. 2168-71. (PMID 15113533, DOI 10.1161/01.CIR.0000128850.84227.FD, lire en ligne [html])
- Stent biodégradable Nobori
- (en) Smits PC, Hofma S, Togni M et al. « Abluminal biodegradable polymer biolimus-eluting stent versus durable polymer everolimus-eluting stent (compare II): a randomised, controlled, non-inferiority trial » Lancet 2013;381!651-660.
- (en) Joner M, Finn AV, Farb A et al. « Pathology of drug-eluting stents in humans: delayed healing and late thrombotic risk » J Am Coll Cardiol. 2006;48:193-202.
- (en) Trading Restenosis for Thrombosis? New Questions about Drug-Eluting Stents, Miriam Shuchman, New Eng J Med, 2006;355:1949-1952
- (en) Joner M, Finn AV, Farb A et al. Pathology of drug-eluting stents in humans: delayed healing and late thrombotic risk, J Am Coll Cardiol, 2006;48:193-202
- (en) Nordmann AJ, Briel M, Bucher HC. Mortality in randomized controlled trials comparing drug-eluting vs. bare metal stents in coronary artery disease: a meta-analysis. Eur Heart J. 2006;27(23):2784-814
- (en) Lagerqvist B, James SK, Stenestrand U, Lindback J, Nilsson T, Wallentin L; SCAAR Study Group. Long-Term Outcomes with Drug-Eluting Stents versus Bare-Metal Stents in Sweden. N Engl J Med. 2007;356(10):1009-19
- (en) Stone GW, Rizvi A, Newman W et al. Everolimus-eluting versus paclitaxel-eluting stents in coronary artery disease, N Engl J Med, 2010;362:1663-1674
- (en) Kedhi E, Joesoef KS, McFadden E et al. Second-generation everolimus-eluting and paclitaxel-eluting stents in real-life practice (COMPARE): a randomised trial, Lancet, 2010;375:201-209
- (en) Boden WE, Diamond GA, DTCA for PTCA — Crossing the line in consumer health education?, N Eng J Med, 2008, 358:2197-2200
Voir aussi
Articles connexes
- Endoprothèse aortique
Liens externes
- Portail de la médecine