Cortisol
Le cortisol (ou hydrocortisone) est une hormone stéroïde (corticostéroïde) sécrétée par la zone fasciculée du cortex (la partie externe) de la glande surrénale à partir du cholestérol, sous la dépendance de l'ACTH hypophysaire. Ses fonctions ou actions principales sont :
- l'augmentation de la glycémie par le biais de la néoglucogenèse ;
- l'inhibition de certaines réponses du système immunitaire ;
- la régulation du métabolisme des lipides, protéines et glucides ;
- régulation du cycle circadien (en complément de la mélatonine)[4].
| Cortisol | ||

| ||
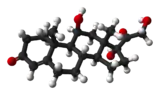 | ||
| Représentation moléculaire du cortisol. | ||
| Identification | ||
|---|---|---|
| Nom UICPA | (8S,9S,10R,11S,13S,14S,17R)-11,17-dihydroxy-17-(2-hydroxyacetyl)-10,13-dimethyl-2,6,7,8,9,11,12,14,15,16-decahydro-1H-cyclopenta[a]phenanthren-3-one | |
| No CAS | ||
| No ECHA | 100.000.019 | |
| No CE | 200-020-1 | |
| Code ATC | A01, A07, C05, D07, D07, D07, D07, D07, H02, S01, S01, S02 | |
| DrugBank | DB00741 | |
| PubChem | 25113440 | |
| ChEBI | 17650 | |
| SMILES | ||
| InChI | ||
| Propriétés chimiques | ||
| Formule | C21H30O5 [Isomères] |
|
| Masse molaire[1] | 362,4599 ± 0,0204 g/mol C 69,59 %, H 8,34 %, O 22,07 %, |
|
| Propriétés physiques | ||
| T° fusion | 220 °C [2] | |
| Solubilité | 320 mg·l-1 (eau,25 °C) [2] | |
| Précautions | ||
| SIMDUT[3] | ||
 D2A, |
||
| Écotoxicologie | ||
| DL50 | 500 mg·kg-1 (souris, s.c.) 150 mg·kg-1 (rat, i.p.) 449 mg·kg-1 (rat, s.c.) [2] |
|
| LogP | 1,61 [2] | |
| Unités du SI et CNTP, sauf indication contraire. | ||
D'un point de vue pathologique, l'hypersécrétion de cortisol – ou hypercortisolisme chronique – définit le syndrome de Cushing, tandis qu'à l'opposé un déficit en cortisol – ou hypocortisolisme – est l'une des formes de l'insuffisance surrénalienne.
Différentes formes de corticostéroïdes synthétiques, apparentés au cortisol, sont utilisées pour le traitement médicamenteux de plusieurs maladies.
Métabolisme
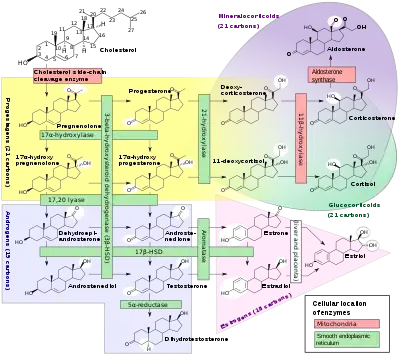
Le cortisol est synthétisé à partir du cholestérol dans la zone fasciculée et la zone réticulée du cortex de la glande surrénale. Son excrétion est régulée au niveau de l'hypothalamus qui stimule l'hypophyse par la Corticotropin-releasing hormone (CRH). L'hypophyse sécrète alors l'hormone corticotrope ou ACTH qui stimule la glande surrénale. Le cortisol est alors excrété. Le cortisol a également un effet de rétrocontrôle inhibiteur sur l'hypothalamus et l'hypophyse et inhibe la CRH et l'ACTH.
Dans le sang, le cortisol est en grande partie (environ 90 %) lié aux protéines (essentiellement à la CBG pour Cortisol Binding Globulin ou transcortine), mais seules les molécules non liées ont une action sur l'organisme. Ces deux formes sont en équilibre.
La 11β-hydroxystéroide deshydrogénase de type 1 permettrait de transformer la cortisone inactive en cortisol actif. Cette enzyme semble donc jouer un rôle dans la régulation de son métabolisme[5].
La destruction (catabolisme) du cortisol se fait au niveau du foie (5β-reductase et 5α-reductase) et du rein (par la 11β-hydroxystéroide dehydrogénase de type 2, transformant le cortisol en cortisone). Ce catabolisme peut être perturbé dans certaines maladies graves, conduisant à un hypercortiscisme[6].
Action physiologique
Véritable initiateur et régulateur métabolique, cette hormone de la cortico-surrénale stimule l'augmentation du glucose sanguin ; elle permet donc de libérer de l'énergie à partir des réserves de l'organisme.
Effet sur le métabolisme glucido-protéique
- Il stimule la dégradation protéique et graisseuse dans la plupart des tissus (excepté au niveau du système nerveux) ;
- le cortisol agit sur le métabolisme glucidique et la régulation de la glycémie, en augmentant la synthèse de glucose par le foie (néoglucogenèse). Il augmente aussi la dégradation des lipides ;
- au niveau de l'eau et des électrolytes, il a un effet minéralocorticoïde modéré (hypokaliémiant et hypernatrémiant) et permet l'augmentation de la filtration glomérulaire (action diurétique) ;
- une action minéralocorticoïde forte avec rétention d'eau apparait à des doses thérapeutiques (corticoïdes médicamenteux) bien supérieures aux normes physiologiques ;
- il augmente également la synthèse d'enzymes spécifiques comme la pyruvate déshydrogénase, la phosphoénolpyruvate carboxykinase, la fructose-1,6-biphosphatase et la glucose-6-phosphatase.
Effet sur le squelette
- Effet catabolisant à dose pharmacologique : ostéoporose ;
- action directe : inhibe l'activité ostéoblastique ;
- action indirecte : diminution de l'absorption intestinale de calcium et augmente son élimination au niveau du rein.
Conséquences :
- chez l'enfant, ralentissement de la croissance des cartilages et de la formation de l'os ;
- chez l'adulte, ostéoporose.
Effets cardiovasculaires
Le cortisol augmente la sensibilité des fibres musculaires lisses vasculaires aux agents hypertenseurs : catécholamines et angiotensine II. Il stimule la synthèse des catécholamines et inhibe leur dégradation par l'enzyme COMT. Le cortisol diminue l'efficacité des agents vasodilatateurs (tel que le NO) sur l'endothélium.
Effets hématologiques
Il entraîne la diminution des lymphocytes circulants, la stimulation de l'érythropoïèse, et l'augmentation des neutrophiles et des plaquettes. Cette diminution fut d'abord attribuée à une suppression immunitaire, mais il a été démontré que cette diminution est plutôt liée à une redistribution des leucocytes vers la périphérie : les nodules lymphatiques, la peau et la moelle épinière (Cohen, 1972 ; Cox & Ford, 1982 ; Dhabhar & McEwen, 1996 ; Dhabhar et Dhabhar; Fauci, 1975 ; Fauci et Dale, 1974 ; Fauci et Dale, 1975 ; Yu et al. 1974).
Effets cutanés
Le cortisol entraîne un retard de cicatrisation des plaies. Par la stimulation de synthèse des enzymes de dégradation de la matrice extracellulaire telles que les métalloprotéinases et l'inhibition des gènes codants les collagènes, l'hypercortisolisme chronique a également un effet de dégradation du derme, caractérisé par une diminution des propriétés mécaniques de la peau (diminution de l'épaisseur du tissu conjonctif sous-jacent).
Effets sur le rein
Le cortisol a une action minéralocorticoïde par fixation sur le récepteur de l'aldostérone. Cette action est empêchée par l'enzyme 11β-hydroxystéroïde déhydrogénase de type 2 (11βHSD2) rénale qui métabolise le cortisol en cortisone inactive. Dans le cas où la cortisolémie est élevée, l'action minéralocorticoïde s'exprime avec des états hypertensionnels et hypokaliémiques.
Effets anti-inflammatoires
Son action anti-inflammatoire et immunosuppressive est à la base de son emploi thérapeutique : le cortisol naturel a donné naissance à une classe de médicaments connue sous l'appellation de corticostéroïdes ou corticoïdes de synthèse. Il agit au niveau sanguin en favorisant le retour des lymphocytes et des polynucléaires éosinophiles dans les organes immunitaires (rate, moëlle osseuse, ganglions lymphatiques) et en accroissant le nombre de polynucléaires neutrophiles circulants (démargination). Au niveau cellulaire, il agit au niveau des lymphocytes T et B en favorisant leur apoptose et en diminuant leur sécrétion de cytokines et d'interleukines (inhibition du facteur NF-kappaB). Il diminue la production de facteurs chimiques de l'inflammation : prostaglandines et leucotriènes (en inhibant la phospholipase A2 (PLA2) par le biais d'une augmentation de la lipocortine), sérotonine, histamine et enzymes lysosomiales.
Les états de stress chronique accompagnés d'une sécrétion élevée et continue de cortisol peuvent faire apparaître des immunodéficiences avec infections. L'exposition de l'organisme aux POPs (polluants organiques persistants) s'accompagne d'une augmentation de la production de cortisol, avec des risques pour le fœtus quand il y est exposé.
Chez le fœtus
Chez tous les mammifères, le cortisol contrôle divers processus hormonaux durant le développement du fœtus. Il contribue au maintien des fonctions vitales et normales du corps durant les périodes de stress. Le cortisol assure également la maturation des poumons du fœtus[7]. Il a été récemment montré que certains polluants organiques persistants (POPs) tels que les PCB modifient, chez l'embryon, aux concentrations trouvées dans notre nourriture (dans le poisson par exemple), la synthèse du cortisol ainsi que d'hormones sexuelles, ce qui peut être nuisible à la santé du futur adolescent et adulte[8]. Chez l'animal de laboratoire, l'exposition fœtale aux PCB — mais aussi durant l'allaitement — modifie le taux sanguin de cortisol des fœtus, et affectent plus tard l'adulte (risque accru de diabète et maladies cardiovasculaires notamment). Néanmoins, il semble exister des processus de synergies encore très mal compris[8].
Rôle et importance en chronobiologie
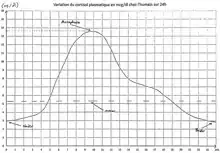
La sécrétion de cortisol, comme celle de la mélatonine, suit un rythme nycthéméral, dont le synchroniseur environnemental est le cycle jour-nuit ou lumière-obscurité. Ainsi, les gens isolés de la lumière ou de tout repère temporel de l'environnement voient leurs rythmes circadiens dériver (leur horloge interne n'est plus recalée sur les 24 h du cycle jour-nuit) et ils connaissent des troubles du sommeil et une somnolence diurne. Des troubles similaires (y compris dans le rythme de production de la mélatonine et du cortisol) existent chez la plupart des personnes totalement aveugles, même s'ils vivent dans une société normale et ont eu accès à de nombreux indices temporels[4].
Les sécrétions de CRH, d’ACTH et de cortisol suivent toutes un rythme circadien. La sécrétion de cortisol est à son maximum, appelé « pic d'acrophase », entre 6 heures et 8 h du matin, puis elle diminue pour être presque nulle en milieu de nuit, avant de réaugmenter pour atteindre un nouveau pic le lendemain matin. C'est la raison pour laquelle le dosage du cortisol plasmatique se réalise le matin vers 8 h. La néoglucogenèse qu'il induit est de nature à nourrir le cerveau au début du jour, et cela même si l'apport récent de nourriture n'a pas été suffisant.
Le rythme circadien de sécrétion du cortisol est indépendant des horaires du sommeil. Cependant, une perturbation de son cycle circadien est observable chez les travailleurs de nuit. Enfin, une variation de la courbe du cortisol a pu être observée dans le cadre circannuel : acrophase en été, batyphase en hiver.
Chez l'adulte, la sécrétion de la mélatonine augmente quand celle de cortisol diminue. Chez des personnes souffrant de troubles du sommeil, l'administration de mélatonine exogène au crépuscule avance de quelques heures l'horloge circadienne[9]. Le vieillissement entraine une diminution de la production de mélatonine et un décalage (retard) du pic de mélatonine, alors que la production de cortisol augmente et que son pic se produit plus tôt dans la nuit[9]. Chez des insomniaques, schizophrènes et patients déprimés dont la production de mélatonine est faible et retardée, l'administration de mélatonine à libération prolongée en soirée peut remédier à une production précoce de cortisol (avec amélioration de la qualité du sommeil, de la pression sanguine, et du métabolisme et de l'humeur)[9].
Maladies liées au cortisol
De nombreuses maladies sont associées à une dérégulation de la sécrétion de cortisol. L'hypercortisolisme (ou hypercorticisme) chronique caractérise les différentes formes du syndrome de Cushing (comprenant différentes formes et origines pathologiques distinctes) et l'hypocortisolisme primaire (ou maladie d'Addison), l'hypocortisolisme secondaire (dû à une insuffisance d'ACTH hypophysaire).
Par ailleurs, il a été observé que les gens déprimés produiraient trop de cortisol et ceux qui sont en épuisement professionnel pas assez[10].
Certaines de ces maladies peuvent même être guéries par la chronopharmacologie.
Divers
L'hydrocortisone fait partie de la liste des médicaments essentiels de l'Organisation mondiale de la santé (liste mise à jour en avril 2013)[11].
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Cortisol », sur ChemIDplus, consulté le 8 juillet 2009.
- « Dihydrocortisone » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 24 avril 2009.
- (en) R. L. Sack, A. J. Lewy, M. L. Blood, L. D. Keith et H. Nakagawa, « Circadian rhythm abnormalities in totally blind people: incidence and clinical significance » Journal of Clinical Endocrinology and Metabolism, Vol. 75, 1992, p. 127-134, DOI:10.1210/jc.75.1.127.
- (en) J. W. Tomlinson, E. A. Walker, I. J. Bujalska et al., « 11Beta-hydroxysteroid dehydrogenase type 1: a tissue-specific regulator of glucocorticoid response », Endocr Rev, no 25, 2004, p. 831-866.
- (en) E. Boonen, H. Vervenne, P. Meersseman et al., « Reduced cortisol metabolism during critical illness », N. Engl. J. Med., no 368, 2013, p. 1477-1488.
- Roger Smith, « Le déclenchement de l'accouchement », Pour la Science, , p. 199 (lire en ligne).
- (en) « Persistent organic pollutants affect the stress hormone cortisol », Norwegian School of Veterinary Science le 28 décembre 2010 [lire en ligne].
- (en) N. Zisape, R. Tarrasch, M. Laudon, « The relationship between melatonin and cortisol rhythms: clinical implications of melatonin therapy », Drug Development Research, numéro spécial : New Drug Targets for Depression and Anxiety Part I: Focus on Monoamines, Volume 65, no 3, pages 119–125, juillet 2005 ; mis en ligne le 21 novembre 2005 DOI:10.1002/ddr.20014 [lire en ligne].
- source: http://age-des-possibles.com/-Burnout,5-.
- « WHO Model List of Essential Medicines, 18th list », avril 2013.
Articles connexes
- Portail de la biochimie
- Portail de la chimie
- Portail de la médecine
- Portail de la pharmacie