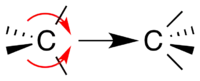Géométrie moléculaire tétraédrique
En chimie, la géométrie moléculaire tétraédrique est la géométrie des molécules où un atome central, noté A, est lié à quatre atomes, notés X, aux sommets d'un tétraèdre régulier (ou presque régulier). Ces composés appartiennent à la classe AX4E0 selon la théorie VSEPR.
| Géométrie moléculaire tétraédrique | |
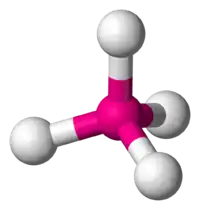
| |
| Notation VSEPR | AX4E0 (AX4) |
|---|---|
| Exemple(s) | CH4, PO43−, SO42- |
| Symétrie moléculaire | Td |
| Nombre stérique | 4 |
| Coordinence | 4 |
| Doublet non liant | 0 |
| Angle de liaison | ≈ 109,47° |
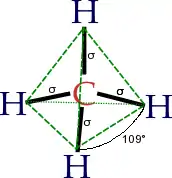
Les angles de liaison sont de ≈ 109,47° lorsque tous les substituants sont les mêmes, comme dans le cas du méthane (CH4)[1],[2]. Les tétraèdres parfaitement symétriques appartiennent au groupe ponctuel de symétrie Td, mais la plupart des molécules tétraédriques ne possèdent pas une si forte symétrie. Les molécules tétraédriques peuvent être chirales.
Cette géométrie est proche de la géométrie moléculaire pyramidale trigonale (AX3E1), où la place de l'un des substituants est tenue par un doublet non liant. Dans cette géométrie les angles de liaison sont inférieurs à 109,5°, par exemple 107° dans le cas de l'ammoniac. Cette légère contraction résulte de la plus forte répulsion que ce doublet non liant, par rapport à un substituant, exerce sur les autres substituants.
Exemples
Chimie du groupe principal
Virtuellement, tous les composés organiques saturés sont tétraédriques ; c'est aussi le cas de la plupart des composés du silicium, du germanium et de l'étain. Souvent, les molécules tétraédriques présentent des liaisons multiples avec des ligands externes, comme pour le tétraoxyde de xénon (XeO4), l'ion perchlorate (ClO4-), l'ion sulfate(SO42-) ou l'ion phosphate (PO43-). Le trifluorure de thiazyle (SNF3) est un composé tétraédrique présentant une liaison triple soufre-azote[3].
Chimie des métaux de transition
De la même façon, cette géométrie est assez répandue, en particulier dans les complexes où le métal a une configuration en d0 ou d10. On peut ainsi citer le tétrakis(triphénylphosphine)palladium(0), le tétracarbonyle de nickel ou encore le tétrachlorure de titane. De nombreux complexes avec une couche d incomplète sont aussi tétraédriques, par exemple les tétrahalogénures de fer(II), de cobalt(II) et de nickel(II).
Exceptions et distorsions
L'inversion d'une structure tétraédrique arrive couramment en chimie organique et chimie de groupe principal. L'inversion de Walden illustre les conséquences de cette inversion au niveau du carbone.
Inversion de géométrie tétraédrique
Les contraintes géométriques d'une molécule peuvent causer de sérieuses distorsions vis-à-vis d'une géométrie tétraédrique parfaite. Dans ces composés comportant un « carbone inversé » par exemple, le carbone est pyramidal[4].
Les plus simples exemples de molécules organiques présentant un carbone inversé sont les plus petits propellanes, tels que le [1.1.1]propellane, ou d'une façon générale les paddlanes[5] et les pyramidanes[6],[7]. Des telles molécules sont en général sous tension, ce qui accroît leur réactivité.
Planarisation
Un tétraèdre peut aussi être distordu par un accroissement de l'angle entre deux liaisons, allant dans les cas les plus extrêmes à former un angle plat. Pour le cas du carbone, de tels phénomènes peuvent être observés dans une classe de composés appelés fenestranes.
Notes et références
- "Angle Between 2 Legs of a Tetrahedron" – Maze5.net
- Valence Angle of the Tetrahedral Carbon Atom W.E. Brittin, J. Chem. Educ., 1945, 22 (3), p 145
- (en) G. L. Miessler et D. A. Tarr, Inorganic Chemistry, Pearson/Prentice Hall, 3rd éd. (ISBN 978-0-13-035471-6 et 0-13-035471-6)
- Kenneth B. Wiberg, « Inverted geometries at carbon », Acc. Chem. Res., vol. 17, no 11, , p. 379–386 (DOI 10.1021/ar00107a001)
- (en) « paddlanes », Compendium of Chemical Terminology [« Gold Book »], IUPAC, 1997, version corrigée en ligne : (2006-), 2e éd.
- Joseph P. Kenny, Karl M. Krueger, Jonathan C. Rienstra-Kiracofe, and Henry F. Schaefer III, « C5H4: Pyramidane and Its Low-Lying Isomers », J. Phys. Chem. A, vol. 105, no 32, , p. 7745–7750 (DOI 10.1021/jp011642r)
- Lewars E., « Pyramidane: an ab initio study of the C5H4 potential energy surface », Journal of Molecular Structure: THEOCHEM, vol. 423, no 3, , p. 173–188 (DOI 10.1016/S0166-1280(97)00118-8)
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Tetrahedral molecular geometry » (voir la liste des auteurs).