Flavonol
Les flavonols sont un sous-groupe de flavonoïdes dérivés de la 3-hydroxyflavone (3-hydroxy-2-phénylchromén-4-one en nomenclature IUPAC) ou flavonol, c'est-à-dire des flavonoïdes possédant un hydroxyle phénolique en C3 et une fonction carbonyle C=O en C4 sur l'hétérocycle central du squelette de base des flavonoïdes. Ce sont des pigments végétaux de couleur jaune plus ou moins clair. Ils diffèrent par le nombre et la position d’hydroxyle phénolique –OH, parfois méthylés (groupes méthoxy).
Les flavonols ne doivent pas être confondus avec les flavanols qui ne comportent pas en position 4 de fonction carbonyle C=O.
Principaux flavonols
| Nom | Structure | R5 | R6 | R7 | R8 | R2' | R3' | R4' | R5' | R6' | CAS | Nom IUPAC |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Flavonol |  | H | H | H | H | H | H | H | H | H | 3-hydroxy-2-phénylchromén-4-one | |
| Azaléatine | OCH3 | H | OH | H | H | H | OH | OH | H | 2-(3,4-dihydroxyphényl)-3,7-dihydroxy-5-méthoxychromén-4-one | ||
| Fisétine | H | H | OH | H | H | H | OH | OH | H | 3,3',4',7-tétrahydroxy-2-phénylchromén-4-one | ||
| Galangine | OH | H | OH | H | H | H | H | H | H | 3,5,7-trihydroxy-2-phénylchromén-4-one | ||
| Gossypétine | OH | H | OH | OH | H | OH | OH | H | H | 2-(3,4-dihydroxyphényl)-3,5,7,8-tétrahydroxychromén-4-one | ||
| Herbacétine | OH | H | OH | OH | H | H | OH | H | H | 3,5,7,8-tétrahydroxy-2-(4-hydroxyphényl)chromén-4-one | ||
| Isorhamnétine | OH | H | OH | H | H | OCH3 | OH | H | H | 3,5,7-trihydroxy-2-(4-hydroxy-3-méthoxyphényl)chromén-4-one | ||
| Kaempféride | OH | H | OH | H | H | H | OCH3 | H | H | 3,5,7-trihydroxy-2-(4-méthoxyphényl)chromén-4-one | ||
| Kaempférol | OH | H | OH | H | H | H | OH | H | H | 3,4',5,7-tétrahydroxy-2-phénylchromén-4-one | ||
| Morine | OH | H | OH | H | OH | H | OH | H | H | 3,3',4',7-tétrahydroxyflavone | ||
| Myricétine | OH | H | OH | H | H | OH | OH | OH | H | 3,3',4',5',5,7-hexahydroxy-2-phénylchromén-4-one | ||
| Natsudaidaine | OCH3 | OCH3 | OCH3 | OCH3 | H | H | OCH3 | OCH3 | H | 2-(3,4-diméthoxyphényl)-3-hydroxy-5,6,7,8-tétraméthoxychromén-4-one | ||
| Pachypodol | OH | H | OCH3 | H | H | H | OH | OCH3 | H | 5-hydroxy-2-(4-hydroxy-3-méthoxyphényl)-3,7-diméthoxychromén-4-one | ||
| Quercétine | OH | H | OH | H | H | OH | OH | H | H | 3,3',4',5,7-pentahydroxy-2-phénylchromén-4-one | ||
| Rhamnazine | OH | H | OCH3 | H | H | OCH3 | OH | H | H | 3,5-dihydroxy-2-(4-hydroxy-3-méthoxyphényl)-7-méthoxychromén-4-one | ||
| Rhamnétine | OH | H | OCH3 | H | H | OH | OH | H | H | 2-(3,4-dihydroxyphényl)-3,5-dihydroxy-7-méthoxychromén-4-one |
Hétérosides de flavonols
On trouve fréquemment les flavonols sous la forme d'hétéroside (glycoside) où ils jouent le rôle de l'aglycone.
On trouve des mono-, di- et triglycosides[1].
| Hétéroside | Aglycone | R3 | R7 | R8 | R4' | R5' | CAS |
|---|---|---|---|---|---|---|---|
| Astragaline | Kaempférol | Glucose | |||||
| Azaléine | Azaléatine | Rhamnose | |||||
| Hypéroside | Quercétine | Galactose | |||||
| Isoquercitine | Quercétine | Glucose | |||||
| Kaempféritrine | Kaempférol | Rhamnose | Rhamnose | ||||
| Myricitrine | Myricétine | Rhamnose | 17912-87-7 | ||||
| Quercitrine | Quercétine | Rhamnose | |||||
| Robinine | Kaempférol | Robinose | Rhamnose | ||||
| Rutoside | Quercétine | Rutinose | |||||
| Spiraéoside | Quercétine | Glucose | |||||
| Xanthorhamnine | Rhamnétine | Triholoside | |||||
| Amurensine | Kaempférol | Glucose | tert-amyl alcool | ||||
| Icariine | Kaempféride | Rhamnose | Glucose | prényle | méthoxyle | 489-32-7 | |
| Troxerutine | Quercétine | Rutinose | hydroxyéthyle | hydroxyéthyle | hydroxyéthyle | 7085-55-4 |
Pour les monoglycosides, l’association de sucre se fait principalement sur le carbone 3 : l'astragaline (kaempférol 3-O-glucoside) du ginkgo biloba, isoquercitine (en) (quercétol 3-O-glucoside) du raisin rouge.
Dans le cas des diglycosides, les deux sucres peuvent être liés
- au même carbone : 3-O-diglycoside comme la rutoside, c'est-à-dire le quercétol 3-O-(6-O-α-L-rhamnosyl-β-D-glucoside) fréquent dans les fruits et légumes
- ou à deux carbones différents : 3,7-di-O-glucoside, quercétol 3,4'-di-O-glucoside dans la peau de pomme.
Les triglycosides de flavonol sont moins fréquemment trouvés dans la nature.
Les monosaccharides les plus fréquents des glycosides sont le D-glucose, D-galactose, L-rhamnose, L-arabinose, D-apiose (en). Mais la substitution peut aussi se faire avec des acides-phénols comme les acides p-coumarique, férulique, caféique, p-hydroxybenzoïque et gallique. Le plus largement distribué est le kaempférol 3-(p-coumaryl).
 Quercétol 3-O-glucoside
Quercétol 3-O-glucoside Rutoside
Rutoside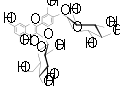 Quercétol 3-4'-diglucoside
Quercétol 3-4'-diglucoside
Environ 200 flavonols ont été identifiés dans la nature.
Plantes riches en flavonols[2]
La quantité de flavonols trouvée dans les fruits, légumes et plantes médicinales peut varier considérablement suivant la variété cultivée, les conditions de croissance et la saison de récolte. Pour les fruits, Sultana et als. (2008[3]) ont trouvé la plus grande quantité de flavonols dans les fraises (3 575 mg/kg de matière sèche) et la plus basse dans la pomme (460 mg kg−1). Pour les légumes, ce sont les épinards et les choux-fleurs qui sont les plus riches (1 720 et 1 603 mg kg−1 respectivement) alors qu'aucun flavonol n'a été détecté dans l'ail.
Hertog et als 1993[4] estiment que la prise quotidienne de flavonols aux Pays-Bas est de 23 mg/jour. Les sources principales sont le thé, les oignons et les pommes. En Finlande la prise quotidienne est de 2,6–9,6 mg, tandis qu'au Japon elle atteint 68,2 mg/jour.
Propriétés médicinales
Les flavonols sont de bons anti-oxydants et anti-inflammatoires (pour plus de détails voir quercétol).
Les diverses méthodes de mesure du pouvoir anti-oxydant des composés phénoliques donnent des résultants très différents[5]. La moyenne pondérée des résultats obtenus par quatre méthodes différentes donne le classement suivant des flavonols :
Myritcétol-3-rhamnoside > Myricétol > Quercétol, Rutoside > Kaempférol-3-glucoside > Kaempférol
Une étude de 8 ans portant sur un échantillon de plus de 180 000 personnes a montré qu'une prise alimentaire de flavonols (quercétol, kaempférol et myricétol) était associée à un risque réduit du cancer du pancréas[6].
Synthèse
Les flavonols peuvent être obtenus synthétiquement à partir des chalcones, par la réaction d'Algar-Flynn-Oyamada.
Références
- (en) Fereidoon Shahidi, Marian Naczk, Phenolics in Food and Nutraceuticals, CRC Press, (ISBN 1-58716-138-9).
- (en) U.S. Department of Agriculture, « USDA Database for the Flavonoid Content of Selected Foods », sur http://www.nal.usda.gov, National Agricultural Library, (consulté le ), p. 1-78 [PDF]
- (en) B Sultana et F Anwar, « Flavonols (kaempferol, quercetin, myricetin) contents of selected fruits, vegetables and medicinal plants », Food Chemistry, vol. 108, no 3, , p. 879-884 (DOI 10.1016/j.foodchem.2007.11.053)
- (en) M.G. Hertog, E.J. Feskens, P.C. Hollman, M.B. Katan et D. Kromhout, « Dietary antioxidant flavonoids and risk of coronary heart disease: the Zutphen Elderly Study. », Lancet, vol. 342,
- (en) Jessica Tabart, Claire Kevers, Joël Pincemail, Jean-Olivier Defraigne et Jacques Dommes, « Comparative antioxidant capacities of phenolic compounds meausured by various tests », Food Chemistry, vol. 113, , p. 1226-1233
- (en) U Nöthlings, SP Murphy, LR Wilkens, BE Henderson et LN Kolonel, « Flavonols and Pancreatic Cancer Risk, The Multiethnic Cohort Study », American Journal of Epidemiology, vol. 166, no 8, , p. 924–931 (DOI 10.1093/aje/kwm172, lire en ligne [PDF])
Voir aussi
Articles connexes
Liens externes
- (en) Flavonoid (myricetin, quercetin, kaempferol, luteolin, and apigenin) content of edible tropical plants.
- (en) Content of the flavonols quercetin, myricetin, and kaempferol in 25 edible berries
- (en) Flavonol and flavone intakes - Fruit and Vegetable Consumption
- (en) Antioxidant flavonols from fruits, vegetables and beverages: measurements and bioavailability
Bibliographie
- Bruneton, J., Pharmacognosie - Phytochimie, plantes médicinales, 4e éd., revue et augmentée, Paris, Tec & Doc - Éditions médicales internationales, , 1288 p. (ISBN 978-2-7430-1188-8)
- Portail de la biologie
- Portail de la chimie