Acide gamma-hydroxybutyrique
L'acide 4-hydroxybutanoïque ou γ-hydroxybutyrate (GHB), anciennement et uniquement dans le monde francophone, connu sous le nom abrégé de gamma-OH, est un psychotrope et très puissant dépresseur du système nerveux central, utilisé à des fins médicales (Xyrem, seulement sur ordonnance spécifique par un médecin spécialiste[6]) ou à des fins détournées. Le GHB est une substance endogène, produite physiologiquement et naturellement dans le cerveau des mammifères et sa structure chimique est très proche du neurotransmetteur GABA[7].
GHB
Pour les articles homonymes, voir GHB (homonymie).
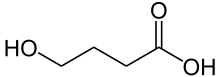
| Acide γ-hydroxybutyrique | ||
| ||
 | ||
| Structure de l'acide γ-hydroxybutyrique. | ||
| Identification | ||
|---|---|---|
| Nom UICPA | Acide 4-hydroxybutanoïque | |
| No CAS | ||
| No ECHA | 100.218.519 | |
| Code ATC | N01 N07 |
|
| DrugBank | DB01440 | |
| PubChem | 3037032 | |
| ChEBI | 30830 | |
| SMILES | ||
| InChI | ||
| Apparence | liquide incolore et inodore[1],[2] | |
| Propriétés chimiques | ||
| Formule | C4H8O3 [Isomères] |
|
| Masse molaire[3] | 104,1045 ± 0,0047 g/mol C 46,15 %, H 7,75 %, O 46,11 %, |
|
| Propriétés physiques | ||
| T° fusion | −17 °C[4] | |
| T° ébullition | 178 à 180 °C (décomp.)[1] | |
| Écotoxicologie | ||
| DL50 | 4 800 mg kg−1 (souris, oral) 3 700 mg kg−1 (souris, i.v.) 4 500 mg kg−1 (souris, s.c.) 4 200 mg kg−1 (souris, i.p.)[5] |
|
| Caractère psychotrope | ||
| Catégorie | Dépresseur | |
| Mode de consommation |
Ingestion |
|
| Autres dénominations |
|
|
| Unités du SI et CNTP, sauf indication contraire. | ||
Historique
Le GHB est synthétisé pour la première fois en 1874 par le chimiste russe Aleksandr Mikhaïlovitch Zaïtsev mais ne rencontre aucune application scientifique ni pharmaceutique. Henri Laborit, au cours de ses études sur le neurotransmetteur GABA, le synthétise de nouveau en 1961[7].
Il est utilisé dans les années 1960 comme anesthésique hypnotique. Il trouve rapidement une grande variété d'utilisations due à ses effets secondaires minimaux et son action de contrôle, la seule difficulté étant la marge étroite de son usage en sécurité.
Chimie
Synthèse
La GBL (gamma-butyrolactone) est un précurseur synthétique du GHB. La mise en réaction de la GBL par une base, le plus souvent la soude (NaOH), la transforme en GHB qui est atoxique, car produit physiologiquement, contrairement à la GBL qui a quelques effets toxiques avec une activité pharmacologique peu, voire pas, modifiée.[réf. souhaitée]
Synthèse endogène
Le GHB est synthétisé à partir de l'acide gamma-aminobutyrique (GABA)[8] dans le cerveau des mammifères. Le GABA subit une première étape de transamination effectuée par la transaminase GABA-T pour produire du semialdéhyde succinique, celui-ci est ensuite réduit en GHB par la semialdéhyde succinique réductase[9]. Le GHB est dosé dans le plasma en quantités micro-molaires.
Une autre voie de synthèse biochimique est celle partant du butane-1,4-diol qui par ADH (alcool déshydrogénase) forme le 4-hydroxybutanal (GHBAL), puis par ALDH (aldehyde déshydrogénase) sur ce dernier forme le GHB[10]. Finalement, il y a aussi la γ-butyrolactone (GBL) qui se transforme in vivo en GHB via une lactamase[11].
Pharmacologie
Deux sites d'actions distincts ont été identifiés dans le système nerveux central : le récepteur GHB (GHB-R) identifié pour la première fois en 2003[9], et le récepteur GABAB responsable des effets sédatifs[12]. Lorsque le GHB est administré par voie périphérique, il traverse rapidement la barrière hémato-encéphalique et modifie le système GHB endogène et donc le système GABAergique dans le cerveau.
Il inhibe temporairement la libération de dopamine dans le striatum[13].
Le GHB est un agoniste faible des récepteurs GABAB[14].
Il agit sur les endorphines ce qui lui donne des propriétés sédatives et anesthésiantes.
Le GHB agit notamment sur le septum et l'hippocampe par l'intermédiaire du locus cœruleus. Il gère pour une part les comportements d'alarme, de peur, d'anxiété et d'éveil. C'est également cette minuscule structure qui met l'ensemble des muscles du corps en état de profonde relaxation (et même de paralysie) pendant le rêve ou la paralysie du sommeil.
Que ce soit pour ses effets thérapeutiques ou récréatifs, l’induction d’un effet neuropharmacologique par le GHB nécessite l’absorption d’une grande quantité de cette substance (deux à trois grammes chez l'homme).
Il peut être métabolisé en GABA et s'élimine sous forme de CO2.
Usage médical

Le 4-hydroxy-butyrate de soude a été utilisé comme anesthésiant[15] général et comme hypnotique dans le traitement de l'insomnie. Il est également utilisé en Europe et aux États-Unis pour le traitement de certains troubles du sommeil, et particulièrement pour diminuer les attaques de sommeil diurne et les épisodes de cataplexie chez les patients narcoleptiques[7],[14]. Cette utilisation se fait sous le nom de marque Xyrem ou, en France de Gamma-OH.
Il est aussi utilisé en Italie (depuis 1991) et en Autriche (depuis 1999) dans le traitement de l'alcoolisme pour la prévention du syndrome de sevrage et au maintien de l'abstinence chez le sujet alcoolodépendant sous le nom d'Alcover, en solution liquide. En France, en 2013, il n'a pas encore cette AMM mais fait l'objet d'études[16].
Il fait aussi l'objet d'études cliniques pour le traitement d’autres assuétudes et pharmacodépendances (toxicomanies)[7], pour la réduction des symptômes chez le patient atteint de fibromyalgie[14], ainsi que pour aider à l'accouchement[15].
Enfin, il est aussi utilisable dans les hyperkaliémies sévères en milieu réanimatoire notamment.
Usage détourné
Comme drogue, il est utilisé le plus souvent sous la forme d'un sel chimique (Na-GHB ou K-GHB) et il est vendu la plupart du temps sous forme liquide mais aussi parfois sous forme de poudre.
Ses usages détournés sont[7] :
- drogue récréative puisqu'à faibles doses le GHB induit un état de désinhibition et d'euphorie proche de l'ivresse. On le désigne donc parfois par le terme apparemment mal approprié d'« ecstasy liquide »[17],[18] ;
- Certains culturistes apprécient le GHB comme complément alimentaire stimulant l'hormone de croissance mais aussi parce qu'il possède des qualités myorelaxantes qui sont donc forts appréciées dans le milieu homosexuel et parmi les adeptes du viol puisque une surdose de GHB provoque également une amnésie chez la victime[19].
- surnommée « drogue du viol » ou « drogue du violeur »[20],[21],[22], le GHB est également utilisé à des fins criminelles. Ses effets sédatifs augmentent lorsque le GHB est mélangé à de l'alcool[23], c'est pourquoi sa présence est parfois attestée lors d'évènements festifs. Le mélange de GHB et d'alcool plonge le plus souvent la victime dans une profonde inconscience et provoque à plus long terme une amnésie. Cet état n'est cependant pas immédiat car il peut être précédé par un coma, des vertiges, des nausées, des vomissements, des convulsions, un décès, etc.[17].
Il ne doit pas être accompagné d'alcool, de benzodiazépines ou de barbituriques car ils amplifieraient les effets dépresseurs du système nerveux central produits par le GHB. Toutes ces drogues agissent au niveau du même récepteur membranaire neuronal, le récepteur GABAA et ont un effet synergique induisant une activité neuronale caractéristique des phases de sommeil.
Effets recherchés
- Décontraction/ Relaxation musculaire (effet myorelaxant).
- Sensation de chaleur.
- Désinhibition.
- Légère euphorie.
- Sensation de flottement, de quitétude et d'apaisement.
- Diminution de l'anxiété.
- Légère altération de la perception de l'environnement (adoucissement et embellissement).
- Exacerbation de la sensibilité (libido, érotisme, tactilité).
- Exacerbation du sentiment d'empathie (effet empathogène).
Effets à court terme
- Ralentissement de la fréquence cardiaque (possible bradycardie) et respiratoire[24].
- Hypotension artérielle[24].
- Somnolence relative à la dose ingérée (effet hypnotique).
- Production d'hormones de croissance.
- Perte de coordination et de l'équilibre[8].
- Vertiges, maux de tête (surdose).
- Nausées, vomissements (surdose)[24].
- Amnésie (surdose)[24].
- Perte de connaissance et/ou de conscience (G-Hole), évanouissement ou coma (surdose)[24].
Effets à long terme
L'utilisation excessive et prolongée conduit à la tolérance et à la dépendance physique[7].
Les symptômes de sevrage sont brusques[7] et comprennent l'anxiété, l'insomnie, les tremblements, l'irritabilité, la sensibilité aux stimuli externes (bruit, lumière, toucher), tachycardie et crampes musculaires. Ces symptômes de sevrage apparaissent de 1 à 6 heures après la dernière prise et disparaîtront après 2 à 21 jours en fonction de la dépendance.
Surdose
Les seuls cas de surdosage au GHB connus chez l'homme sont liés à un mélange de GHB et d'alcool, mélange très fréquemment rencontré dans le cas où le GHB est utilisé comme drogue récréative (vomissements et décès par obstruction des bronches). Les effets du GHB et de l'alcool sont plus qu'additifs : ils agissent en synergie au niveau des récepteurs GABAB. Cette synergie est une allostérie, la présence de l'un des composés augmente la fixation et donc l'effet de l'autre. Tout se passe comme s'il fallait moins de GHB pour obtenir les mêmes effets. Le récepteur GABAB étant impliqué dans le contrôle autonome des voies aériennes, la mort peut survenir par dépression respiratoire[25].
Il a été classé en 1999, sur la liste I des substances vénéneuses pour la forme injectable réservée à l’usage hospitalier, et sur la liste des stupéfiants pour les formes orales, ce qui a poussé certains utilisateurs à se tourner vers un de ses précurseurs chimiques, non classé, la gamma-butyrolactone (GBL), rarement a priori comme « drogue du viol » mais plutôt à but récréatif, avec des cas d'intoxications avérées et des risques de décès. La médecine légale peut faire la preuve de son usage par dosage de la molécule dans l'urine ou le sang (chromatographie en phase gazeuse-spectrométrie de masse (CPG-SM), voire par l'analyse de phanères (ongles, cheveux[26], poils pubiens). Des taux de 285 et 815 mg/L ont été associés à plusieurs cas d'intoxications mortelles[27].
La DL50 du GHB chez le rat est entre 1 100 mg kg−1 et 2 000 mg kg−1[28], ce qui rapporté à l'homme en fait une drogue peu toxique. Encore une fois, les effets de l'alcool et du GHB étant synergiques, la combinaison des deux diminue fortement cette DL50, rendant de facto le GHB bien plus toxique. On rencontre ce même type de synergie entre les benzodiazépines et l'alcool, tous deux se liant au même récepteur.
Trafic et production
Jusqu'en 1998, il était relativement disponible sur Internet[8].
Selon l'OICS dans son rapport du , comme pour la plupart des « drogues de synthèse », la production s'effectue près des lieux de consommation grâce à la mise en œuvre de laboratoires clandestins mobiles.
Sous sa forme artisanale, il peut avoir un goût salé[8].
Législation
Il est répertorié par la convention sur les substances psychotropes de 1971.
Le décès de Samantha Reid, une adolescente américaine, a été le point de départ à la classification du GHB comme stupéfiant[30].
- En France, le GHB a été classé comme stupéfiant en 1999, à l'exception des préparations injectables destinées aux usages médicaux et vétérinaires, qui sont sur la liste I des substances vénéneuses[31].
- Aux États-Unis, il est interdit de vente au public en 2000. Mais il est prescrit depuis 2002 dans le traitement de la narcolepsie accompagnée d’accès de cataplexie.
- Au Canada, le GHB est inscrit à l'annexe III de la Loi réglementant certaines drogues et autres substances. La simple possession, la possession en vue d'en faire le trafic, la production, l'exportation, ainsi que l'importation sont illégales.
- En Suisse, le GHB a été introduit dans la loi fédérale sur les stupéfiants et les substances psychotropes en 2002 après approbation de la convention sur les substances psychotropes de 1971 en 1995.
Molécules voisines
Après son interdiction, des substances analogues et qui se transforment une fois ingéré en GHB, tels que la GBL et le 1,4-BD sont devenues plus disponibles. Ces deux substances sont ensuite devenues illégales en France en 2011[32].
Notes et références
- (de) Entrée Hydroxybuttersäuren sur Römpp Online. Georg Thieme Verlag, consultée le 28 novembre 2018.
- M. Sylvia Stein, Stellungnahme zur Nicht Geringen Menge von γ-Hydroxybuttersäure [PDF], Toxichem, Krimtech., 2003, vol. 70, no 2, p. 87–92.
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- M. R. Witkowski et al., GHB free acid: II. Isolation and spectroscopic characterization for forensic analysis, J. Forensic. Sci., 2006, vol. 51, p. 330–339, , DOI:10.1111/j.1556-4029.2006.00074.x.
- (en) « Acide gamma-hydroxybutyrique », sur ChemIDplus (consulté le 11 juillet 2009).
- « XYREM 500 mg/ml sol buv - prescription_delivrance_prise_en_charge », sur vidal.fr (consulté le ).
- Denis Richard, Jean-Louis Senon et Marc Valleur, Dictionnaire des drogues et des dépendances, Larousse, (ISBN 2-03-505431-1).
- Michel Hautefeuille, Dan Véléa, Les drogues de synthèse, Presses Universitaires de France, coll. « Que sais-je ? », (ISBN 2-13-052059-6).
- (en) Andriamampandry Christian, Taleb Omar, Viry Sandrine, Muller Claude, Humbert Jean Paul, Gobaille Serge, Aunis Dominique et Maitre Michel (2003), « Cloning and characterization of a rat brain receptor that binds the endogenous neuromodulator γ-hydroxybutyrate », The FASEB Journal, vol. 17, no 12, p. 1691-3.
- PubChem CID 3037032.
- Fiche toxicologique no 247 - Gamma-Butyrolactone, INRS.
- (en) Vienne Julie, Bettler Bernhard, Franken Paul et Tafti Mehdi (2010), « Differential effects of GABAB receptor subtypes, {gamma}-hydroxybutyric Acid, and Baclofen on EEG activity and sleep regulation », The Journal of Neuroscience, vol. 30, no 42, p. 14194-14204.
- (en) Howard Sherrel C., Feigenbaum et Jeffrey J. (1997), « Effect of gamma-hydroxybutyrate on central dopamine release in vivo », Biochemical Pharmacology, vol. 53, p. 103–110.
- Maitre Michel, Humbert Jean-Paul, Kemmel Véronique, Aunis Dominique et Andriamampandry Christian (2005), « Mécanismes d’action d’un médicament détourné : le γ-hydroxybutyrate », Médecine/Sciences, vol. 21, p. 284-9.
- Drogues, savoir plus risquer moins, comité français d'éducation pour la santé et de la mildt, (ISBN 2-908444-65-8).
- F. Paille et le groupe de travail sur les médicaments de la SFA, « Oxybate de sodium (acide gamma-hydroxybutyrique ou GHB) et alcool » [PDF], .
- « Le dico des drogues - GHB », sur Drogues Info Service (consulté le ).
- « Usages de GBL en France: retour sur une controverse », sur vih.org (consulté le ).
- Bourin Michel, Le GHB, du médicament à la « drogue du violeur », dans La science des sixties (dir. Néron de Surgy Olivier et Tirard Stéphane), Paris, Belin, 2014, p. 48-49.
- Lire en ligne, Metro-France, 4 mars 2003.
- « La drogue du violeur efficace contre l'alcoolisme ? », sur 20minutes.fr (consulté le ).
- « Un nouveau médicament testé contre l'alcoolisme », Le Parisien, (lire en ligne, consulté le ).
- « Drogues: Savoir plus, risquer moins - GHB », sur toxquebec.com (consulté le ).
- Yasmina Salmandjee, Les drogues, Tout savoir sur leurs effets, leurs risques et la législation, Eyrolles, coll. « Eyrolles Pratique », (ISBN 2-7081-3532-5).
- La dépression respiratoire est l'un des problèmes rencontré au cours de l'anesthésie générale
- Pépin, G., Gaillard, Y., Cheze, M. et Goulle, J. P. (2003), Le GHB dans les phanères : résultats et interprétation, Journal de médecine légale droit médical, 46(2), 93-100 (résumé avec Inist/CNRS).
- Marjorie Chèze, Guillaume Hoizey, Marc Deveaux, Aurélie Muckensturm, François Vayssette, Francis Billault et Gilbert Pépin, Une série de nouveaux cas d'intoxications par le GHB ou la GBL. Dosages dans le sang, l'urine et les phanères, Ann. Toxicol. Anal. (Société française de Toxicologie analytique), 2012, vol. 24, no 2, p. 59-65, DOI:10.1051/ata/2012005, en ligne le 22 juin 2012.
- (en) Galloway, Frederick, Gonzales et al., « Gamma-hydroxybutyrate: an emerging drug of abuse that causes physical dependence », Addiction, 1997, 92(1):98-96.
- Lire en ligne, Le Journal du Pays basque, 19 août 2006.
- (en) Article du PBS, 11 avril 2000.
- Arrêté du 5 mai 1999 portant classement sur la liste I des substances vénéneuses et sur la liste des substances classées comme stupéfiants.
- Arrêté du 2 septembre 2011 portant application d'une partie de la réglementation des stupéfiants.
Voir aussi
Articles connexes
Liens externes
- (en) Page d'information du Bureau de Contrôle des Drogues des États-Unis
- Le Gamma-OH, bonheur ou maléfice ?, sur auriol.free.fr
- Portail de la biochimie
- Portail de la chimie
- Portail de la médecine
- Portail de la pharmacie
- Portail des neurosciences