Plasticité neuronale
La plasticité neuronale, neuroplasticité ou encore plasticité cérébrale sont des termes génériques qui décrivent les mécanismes par lesquels le cerveau est capable de se modifier lors des processus de neurogenèse dès la phase embryonnaire ou lors d'apprentissages. Elle s’exprime par la capacité du cerveau de créer, défaire ou réorganiser les réseaux de neurones et les connexions de ces neurones. Le cerveau est ainsi qualifié de « plastique » ou de « malléable ». Ce phénomène intervient durant le développement embryonnaire, l'enfance, la vie adulte et les conditions pathologiques (lésions et maladies). Il est responsable de la diversité de l'organisation fine du cerveau parmi les individus (l'organisation générale étant, elle, régie par le bagage génétique de l'espèce) et des mécanismes de l'apprentissage et de la mémorisation chez l'enfant et l'adulte. Ainsi, la plasticité neuronale est présente tout au long de la vie, avec un pic d’efficacité pendant le développement à la suite de l'apprentissage, puis toujours possible mais moins fortement avec l’adulte[1],[2].
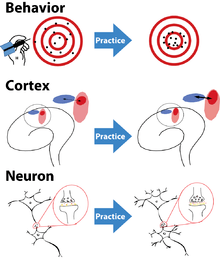
La plasticité neuronale est donc, avec la neurogenèse adulte, une des découvertes récentes les plus importantes en neurosciences, et montre que le cerveau est un système dynamique, en perpétuelle reconfiguration[3],[4].
Elle est opérante avec l’expérience, dans l’apprentissage par exemple qui va faire des renforcements de réseaux et de connexions, mais aussi lors de lésions sur le corps ou directement dans le cerveau[5].
La plasticité, une propriété complexe
Le terme de plasticité est très largement utilisé en neurobiologie dès les années 1970 et reste depuis un terme très en vogue[6].
Ce concept fait référence à la plasticité d'un matériau qui est sa propriété à modifier sa forme sous l'effet d'une action et à la conserver à l'arrêt de cette action. À l'inverse, l'élasticité désigne la propriété d'un matériau qui se déforme puis reprend sa forme initiale lorsque l'action cesse. En neurobiologie, la plasticité désigne la modification d'une propriété, ou d'un état, face à une modification de l'environnement (stimulus externe). Le terme a cependant été utilisé de manière abusive sans réellement établir de correspondance avec la propriété de plasticité (telle qu'elle est définie en science de la matière) et son concept n'est pour l'instant pas clairement défini.
Le cerveau est constitué de neurones et de cellules gliales étroitement interconnectées. L'apprentissage modifie la force des connexions entre les neurones (voir plasticité synaptique) et modifie les réseaux neuronaux en favorisant l'apparition, la destruction ou la réorganisation non seulement des synapses mais également des neurones eux-mêmes. C'est l'ensemble de ces phénomènes qui peuvent être regroupés sous le terme de plasticité neuronale.
La plasticité est une propriété présente à tous les niveaux d'organisation du cerveau :
- Au niveau des molécules, les récepteurs possèdent plusieurs « états » ou configurations qui permettent de modifier la transmission de l'influx nerveux ;
- Au niveau de la synapse, l'ensemble des molécules est régi par l'activité, avec notamment le recrutement de nouveaux récepteurs vers la membrane (exocytose, traduction locale, etc.) (plasticité synaptique) ;
- Au niveau du corps cellulaire, l'expression génétique est également modulée par l'activité des différentes synapses ;
- Au niveau des axones et des dendrites, les prolongements se réorganisent en fonction de l'activité des synapses et des neurones en contact, ainsi que des interactions avec la glie environnante ;
- Le neurone est susceptible de se développer ou de régresser en fonction de son implication dans un réseau (plasticité neuronale) ;
- Le réseau lui-même change ses connexions internes et externes constamment au cours du temps (plasticité cérébrale) ;
- Le cerveau est enfin capable de produire de nouveaux neurones (voir neurogenèse) ;
- L'individu ne cesse de changer son comportement en fonction des situations rencontrées, par exemple dans l'approche d'un problème. Il est également susceptible de subir des lésions ou de modifier certaines de ses capacités par l'activité, la prise d'aliments, de médicaments, de drogues, etc.
L'ensemble de ces échelles interagissent entre elles et doivent être étudiées à la fois séparément et dans leur ensemble pour comprendre la propriété fondamentale qu'est la plasticité en neurosciences.
Une décennie de recherche a montré que des changements sont susceptibles de continuer après la période de l’enfance et que ces changements des patrons d'activations neuronaux dépendent de l'expérience. Cette théorie de la neuroplasticité suggère donc que l'expérience peut changer à la fois la structure anatomique du cerveau mais aussi son organisation physiologique. Les chercheurs s'accordent, désormais, sur la présence, tout d'abord, d'une période critique ou d'une fenêtre de plasticité des différents réseaux neuronaux durant l'enfance (par exemple l'aire visuelle) durant laquelle les changements majeurs interviennent en fonction de l'expérience, mais également que cette fenêtre ne se refermerait pas complètement et que certains changements mineurs ou même majeurs peuvent encore avoir lieu tout au long de la vie.
Dans le cas d’une activité normale, sans lésions, la plasticité neuronale s’exprime surtout par le renforcement ou la dépression de la quantité de connexions entre les neurones ou dans un réseau neuronal. Par exemple, lors de l’apprentissage de la lecture, le début est laborieux et difficile, puis avec de la pratique et de l’expérience, cela devient de plus en plus facile et rapide. C’est l’expression de la croissance du nombre de connexions dans l’aire responsable de la lecture. À l’inverse, lorsque l’on utilise moins un réseau de neurones, ses connexions diminuent, cela s’extériorise par la difficulté de refaire l’action en rapport avec ce réseau. Par contre, comme le réseau est déjà en place, si on le réutilise, les connexions seront plus rapides à se remettre en action, et tout l’apprentissage ne sera pas à refaire.
La mémoire fonctionnant sur une base de facilitation est répartie dans tout le cerveau en se servant des différentes aires perceptives pour fixer le souvenir et les représentations qui s’y attachent[7]. En effet, l’activation d’un réseau neuronal permettrait de retrouver le vécu et les représentations spécifiques à cette expérience lors de la réactivation de ce réseau. On a donc une préservation du réseau à la suite de son utilisation, mais aussi un renforcement de ce réseau en fonction de sa fréquentation. C’est le phénomène même de la plasticité neuronale qui serait donc à l’origine de ce mécanisme de facilitation de la mémoire, par le développement de réseaux neuronaux, et la mise en lien de ces réseaux[8].
Dans le cas d’une activité anormale mais non lésée, comme des personnes aveugles de naissance, ce qui implique que l’aire visuelle de ces personnes n’est pas stimulée, ni développée puisqu’il n’y a pas eu d’apport visuel. Pourtant, des IRM ont permis de constater que l’aire visuelle était sollicitée dans l’apprentissage et l’utilisation du braille (langage écrit pour personnes aveugles). Ici, la plasticité agit en réorientant les neurones inactifs vers une fonction différente de leur fonction première[9].
Réaction aux lésions
L'utilisation la plus courante, car la plus ancienne, désigne la capacité du cerveau des enfants à se réorganiser après une lésion. De nombreuses études montrent en effet qu'une lésion cérébrale qui survient durant l'enfance provoque des défauts comportementaux et cognitifs bien moindres que ceux que l'on observe chez l'adulte, pour le même type de lésions. Ces observations mettent en évidence la capacité de réorganisation plastique du cerveau durant le développement, capacité de réorganisation qui diminue avec la maturation des réseaux neuronaux. Cette capacité viendrait du fait que le support neuronal disponible à la naissance est bien supérieur à celui nécessaire pour coder les fonctions cognitives. Si une blessure intervient au niveau d'une zone particulière, les neurones non utilisés des autres zones sont recrutés pour remplacer ce défaut. Néanmoins, avec la maturation du cerveau, la quantité de neurones non utilisés diminue, diminuant, par là même, la plasticité avec laquelle le cerveau répond aux lésions[10]. Ce point de vue, développé dès les années 1960-1970, décrit donc la plasticité comme une capacité du cerveau de changer ses « plans de développement » normaux en réaction à une lésion[11].
Dans le cas d’une lésion, la plasticité neuronale agira différemment en fonction du type de lésion.
Prenons le cas d’une lésion du cerveau, la zone n’est plus innervée par perte des neurones, ce qui donne des déficiences directes sur les fonctions qu’occupaient ces neurones. Pourtant, il arrive que des individus retrouvent partiellement ou complètement leurs capacités. Si la lésion survient chez un jeune individu, alors le sujet a plus de chance de recouvrir toutes ses capacités par l’utilisation de neurones encore non utilisés. Mais plus généralement, ce sont les aires neuronales voisines qui viennent prendre en partie le relais ce qui permet de récupérer une partie de ses capacités correspondant à la zone lésée[12].
Nous allons voir aussi comment la plasticité neuronale réagit à une amputation. Tout d’abord il faut parler de l’existence d’une carte représentant toute la surface de la peau (l’homonculus sensitif), elle se situe sur le gyrus postcentral, et est appelé « Carte de Penfield ». Cette carte expose en formes plus ou moins grosse les zones du corps, la taille variant en fonction du degré de sensibilité. De plus, les différentes zones du corps ne sont pas représentés dans l’ordre que l’on perçoit extérieurement, comme la zone de la main à côté de celle du visage. C’est cet aspect qui va être important lors de la réponse à l’amputation[13],[9].
Ainsi, lors d’une amputation, la zone du membre amputé n’est plus stimulée, pourtant il arrive que des sensations persistent, c’est le principe du membre fantôme. Cela s’explique par la persistance de la carte cérébrale du membre amputé qui cherche à être stimulé. Par exemple, prenons une personne amputée de l’avant-bras qui perçoit son membre fantôme, on observe une superposition de sensation sur le visage, ce sont ces sensations sur le visage qui amènent les sensations du membre fantôme. En effet, sur la carte cérébrale, les zones de la main et celle du visage sont voisines, une fois la zone de la main non stimulée, on constate une invasion de la zone vacante par la zone du visage qui vient remplacer les connexions nerveuses à l’abandon. Il est ainsi possible de dessiner sur le visage de la personne amputée, une carte sensible et complète de la main[13],[9].
Une utilisation thérapeutique
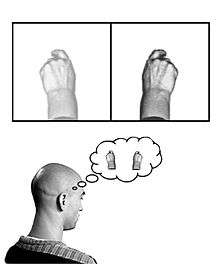
À la suite de ce problème que pose le membre fantôme, qui peut causer de terribles souffrances à la personne, Vilayanur S. Ramachandran un neuroscientifique s’est posé la question du soin de ces douleurs et paralysies fantômes. Il parvient à mettre en place un protocole permettant de soigner ces patients en utilisant la plasticité neuronale[14].
Tout d’abord, il émet l’hypothèse que ces douleurs et paralysies seraient des phénomènes appris par le cerveau. En effet, lorsqu’il regarde l’histoire de ces patients amputés, il constate qu’ils ont souffert pendant une longue période d’une paralysie ou de douleurs chroniques les empêchant de mouvoir leur membre. Il explique cela par le fait que le cortex moteur envoie en continu des commandes de mouvement, qui est mis en opposition avec les feed-back sensoriels qui montrent sʼil y a mouvement ou non. Avant l’amputation, il n’y a pas de réponses musculaires ou sensoriels sur une longue période, ce qui va donner une paralysie apprise à force. Après l’amputation, la sensation de paralysie et de douleur peut rester puisqu'il n’y a pas de feed-back sensoriel pour contredire la commande motrice. D'où des sensations de membres fantômes bloqués dans une position douloureuse, sensible et très inconfortable[15].
Le protocole de soin établi par Ramachandran en 1996 est une boite à miroirs qui vient utiliser le feed-back visuel pour corriger les sensations acquises par le cerveau du patient. Cette boite se compose d’un miroir vertical au centre d’un carton. Le patient (amputé de l’avant-bras) vient placer de part et d’autre du miroir son bras réel et son membre fantôme. En regardant le miroir sous un angle précis, la main réelle vient se superposer à la main ressentie, ce qui donne la sensation d’avoir deux mains même si cela est faux et que le patient en est parfaitement conscient[16].
Ramachandran fait une première expérience avec un de ses patients, Jimmie, qui a un avant-bras gauche fantôme et qui souffre de terribles crampes. Il utilise la boite à miroir et lorsque ses mains se superposent cela lui donne « l’impression visuelle que son fantôme avait été ressuscité ». En effectuant des mouvements symétriques des deux bras, il a non seulement « l’impression que le fantôme obéissait à ses ordres », mais aussi « il sentit ses douloureux spasmes fantômes s’estomper »[14].
Une autre expérience de Ramachandran avec la boite à miroir a permis d’arriver à un résultat encore plus conséquent. Un autre patient amputé, Ron, utilise régulièrement la boite chez lui pendant trois semaines, et finit par constater la disparition de son membre fantôme[14].
Donc, les douleurs fantômes qui sont entretenues par le manque de réponses aux commandes motrices, peuvent être démobilisées par le biais visuel. Ce protocole vient manipuler les perceptions du cerveau pour que celui-ci puisse adapter ses réponses (auparavant douloureuses), à la situation nouvelle de la personne, soit qu’il n’y a plus lieu d’avoir de douleurs puisqu’il n’y a plus de membre réel[14].
D'autres utilisations thérapeutiques sont mises en place par la neuroplasticité autodirigée. Le patient atteint de lésions cérébrales (stress post-traumatique, accident vasculaire cérébral, troubles obsessionnels compulsifs) est incité à réaliser des expériences dirigées qui augmentent l'activité neuronale, et façonnent certaines parties de son cerveau afin de réduire ces lésions[17].
Histoire
En 1848, Phineas Gage fut victime d'un traumatisme crânien qui détruisit la majeure partie de son lobe frontal gauche et changea profondément sa personnalité. La description de ce cas d'école en neurologie amena la première évidence qu'une altération du cerveau pouvait modifier le comportement.
L'idée de plasticité neuronale fut proposée, pour la première fois, en 1890 par William James dans Principes de psychologie. Néanmoins elle fut négligée, durant près de cinquante ans, par la suite.
Durant le XXe siècle, le consensus était que certaines zones du cerveau, comme le néocortex, étaient immuables après l'enfance et plus particulièrement après une période critique de maturation du réseau. Seules certaines zones, comme l'hippocampe, siège de la mémoire, étaient réputées susceptibles de plasticité.
C’est avec Santiago Ramón y Cajal, prix Nobel de médecine en 1906, que cette idée de plasticité est théorisée et utilisée sommairement[2].
C’est Geoffrey Raisman qui est considéré par la communauté scientifique comme le père de la plasticité neuronale à travers son article de 1969. En effet, il permet « d’établir pour la première fois et de manière définitive », la capacité qu’a le cerveau à constituer de nouvelles synapses à la suite d’une lésion chez l’adulte[2].
Neurobiologie
Un des principes fondamentaux du fonctionnement de la neuroplasticité est lié au concept d'élagage synaptique, l'idée que les connexions entre les neurones sont constamment éliminées lorsqu'elles ne sont pas utilisées. À l'inverse, ce mécanisme renforce les connexions très utilisées. Cela a pour conséquence de renforcer les réseaux de neurones qui sont synchronisés et de les séparer des autres neurones qui appartiennent à d'autres cartes corticales.
D'un point de vue morphologique, il s'agit de l'apparition, de la disparition, ou de la réorientation de structures comme des dendrites, des épines dendritiques[18], voire d'axones. On observe cette plasticité par imagerie. On peut aussi mesurer les effets physiologiques de cette plasticité par l'utilisation de la technique de patch clamp en plusieurs endroits simultanément sur des neurones en contact.
Plasticité intrinsèque
Cette plasticité se définit par les modifications de l'excitabilité neuronale en fonction de l'« expérience » du neurone. Lorsque l'excitabilité est augmentée, le neurone répondra plus facilement à un potentiel d'action et à l'inverse, si l'excitabilité diminue, le neurone sera moins sensible aux potentiels d'action présynaptiques, ce qui se traduira dans les deux cas par un changement de la fréquence à laquelle le neurone déchargera en réponse à une stimulation[19],[20].
Que cela soit celle des potentiels d'action le long de l'axone, ou celle des potentiels postsynaptiques le long des dendrites, la propagation des signaux nerveux dépend de la composition de la membrane plasmique en canaux ioniques. Un changement de cette composition en canaux ioniques, qu'il soit qualitatif ou quantitatif, changera la manière avec laquelle le signal électrique se propage. Les changements des propriétés électrochimiques de membrane peuvent être à court terme, quand seul l'état des canaux ioniques est transitoirement modifié, ou à long terme, en général quand les canaux ioniques sont remplacés par d'autres. On mesure cette plasticité par des mesures électrophysiologiques. Deux principaux canaux sont généralement impliqués dans cette plasticité : les canaux potassiques (K+) et les canaux sodiums (Na+). D'autres canaux peuvent éventuellement intervenir en fonction du type de neurone étudié. Ces modifications peuvent être décomposées en changements des propriétés passives de la membrane : résistance de la membrane, constante de temps, potentiel de repos, potentiel seuil d'émission d'un potentiel d'action ; et en changements des propriétés actives : fréquence d'émission de potentiels d'action, relation entre courants synaptiques entrants et fréquence de décharges, patron temporel de la décharge.
Cette plasticité a deux fonctions mises en évidence par les expériences en électrophysiologie :
- Elle assure l'homéostasie de l'excitabilité intrinsèque du neurone, ce qui veut dire que le neurone s'adapte aux moindres changements de l'excitation pour toujours produire la même réponse. Notamment lorsque la fréquence d'entrée augmente progressivement, l'excitabilité du neurone baisse de manière à garder la même fréquence de sortie.
- Elle permet sous certaines conditions de potentialiser l'excitabilité du neurone, par exemple après une série de potentiels d'actions à haute fréquence sur une faible durée, le neurone augmente sa fréquence de sortie en augmentant l'excitabilité.
D'un point de vue spéculatif sur les bases cellulaires de la mémoire et de l'apprentissage, la différence entre cette forme de plasticité et la plasticité synaptique est que si cette dernière permettrait théoriquement de retenir une grande quantité d'information (vu le nombre de synapses pouvant être potentiées ou déprimées), seule la modification des propriétés non synaptiques de la membrane permettrait de modifier le codage en fréquence et les caractéristiques temporelles de ce codage.
Notes et références
- « Cahiers jungiens de psychanalyse » François Martin-Vallas, 2009 n°130.
- « Revue d'histoire des sciences » Marion Droz Mendelzweig Armand Colin, 2010/2 - Tome 63
- "Train Your Mind, Change Your Brain: How a New Science Reveals Our Extraordinary Potential to Transform Ourselves" Sharon Begley.
- Le cerveau, comment il se réorganise sans cesse, Les dossiers de La recherche, n°40, Août 2010
- "Manuel de Science et Vie de la Terre 1reS" programme 2001 collection Raymond Tavernier, Claude Lizeaux
- J. Paillard, Réflexion sur l'usage du concept de plasticité en neurobiologie, Journal de Psychologie Normale et Pathologique, n° 1, 33-47. (1976)
- "Cahiers jungiens de psychanalyse" François Martin-Vallas, 2009/3 -N°130
- "François Martin-Vallas, Cahiers jungiens de psychanalyse" 2009/3 -N°130
- "Manuel de Science et Vie de la Terre 1reS, programme 2001" collection Raymond Tavernier, Claude Lizeaux
- J Stiles. Neural Plasticity and Cognitive Development. Developemental Neuropsychologie, 2000. 18(2), 237–272.
- Spicher C, Quintal I, Vittaz. Rééducation sensitive des douleurs neuropathiques - Préface: Serge Marchand (3e édition). Montpellier, Paris : Sauramps Médical, 2015. (ISBN 978 2 84023 981 9)
- "Comment les pattes viennent au serpent. Essai sur l’étonnante plasticité du vivant" Dominique Lambert, René Rezsöhazy, Editions Flammarion, 2004
- "Le cerveau cet artiste" Vilayanur Ramachandran, Eyrolles, 2005.
- "Le cerveau cet artiste" Vilayanur Ramachandran, Eyrolles, 2005
- Le cerveau cet artiste, Vilayanur Ramachandran, Eyrolles, 2005
- Vilayanur Ramachandran, Le cerveau cet artiste, Eyrolles, 2005
- (en) Jeffrey M. Schwartz, Sharon Begley, The Mind and the Brain, Springer Science & Business Media, , p. 94
- De Roo, M., Klauser, P. & Muller, D. LTP promotes a selective long-term stabilization and clustering of dendritic spines. PLoS Biol 6, e219 (2008)
- Daoudal G, Debanne D (2003) Long-term plasticity of intrinsic excitability: learning rules and mechanisms. Learn Mem. 2003 Nov-Dec;10(6):456-65.
- Zhang W, Linden DJ (2003), The other side of the engram: experience-driven changes in neuronal intrinsic excitability. Nat. Rev. Neurosci. 4:885-900.
Articles connexes
- Neurogenèse
- Plasticité synaptique
- Élagage synaptique
- Période critique
- Règle de Hebb
- Hugues Duffau
- Portail des neurosciences