Maraviroc
Le maraviroc est un antagoniste compétitif du récepteur CCR5. Il est utilisé pour prévenir l'entrée du virus VIH-1 dans ses cellules cibles. En bref, il se lie au CCR5 cellulaire pour empêcher sa liaison avec la gp120 virale ce qui empêche la fusion nécessaire à l’entrée du virus. Il est commercialisé sous le nom de Selzentry et Celsentri (en dehors des États-Unis). Il est disponible en France depuis le 18/09/2007 sous forme de comprimé dosé à 150 mg et 300 mg sous le nom de marque de Celsentri®[4], marque française propriété de PFIZER PRODUCTS INC. Il est inscrit sur la Liste I des substances vénéneuses et sa prescription est restreinte à la médecine hospitalière[5]. La vente est réservée à la Pharmacie hospitalière avec rétrocession au public possible[6]. Il est le premier médicament sur le marché à cibler une composante de la cellule hôte plutôt que le virus lui-même. Il est une bonne alternative pour les gens infectés qui sont résistants à d’autres types de molécules. Son haut potentiel antiviral et son action prolongée sur les récepteurs font de lui un médicament prometteur.
| Maraviroc | |
 | |
| Identification | |
|---|---|
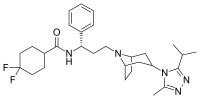
| Nom UICPA | 4,4-difluoro-N-{(1S)-3-[3-(3-isopropyl- 5-méthyl-4H-1,2,4-triazol-4-yl)-8-azabicyclo[3.2.1]oct-8-yl]-1- phénylpropyl}cyclohexanecarboxamide |
| No CAS | |
| No ECHA | 100.124.927 |
| Code ATC | J05 |
| DrugBank | DB04835 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule brute | C29H41F2N5O [Isomères] |
| Masse molaire[1] | 513,6655 ± 0,0274 g/mol C 67,81 %, H 8,05 %, F 7,4 %, N 13,63 %, O 3,11 %, |
| Données pharmacocinétiques | |
| Biodisponibilité | 23 %[2] |
| Métabolisme | hépatique |
| Demi-vie d’élim. | 16 h[3] |
| Considérations thérapeutiques | |
| Voie d’administration | orale |
| Unités du SI et CNTP, sauf indication contraire. | |
Origine
En 1984, des chercheurs ont découvert que le virus du VIH utilisait le récepteur CD4 pour entrer dans sa cellule cible. Après quelques expériences, ils ont remarqué que la liaison du virus à ce récepteur n'était pas suffisante pour que le virus entre dans la cellule. Quelques années plus tard, ils ont découvert l'association à un corécepteur (soit CCR5 ou CXCR4). Ces deux interactions sont nécessaires pour l’infection de la cellule cible. Comme il existe dans la population une mutation naturelle dans le CCR5 qui protège les gens contre l'infection, les compagnies pharmaceutiques se sont penchées sur cette cible. Le maraviroc a été découvert par les scientifiques de la compagnie Pfizer. Ils ont balayé leur banque de molécules à la recherche d'un composé qui irait se lier au CCR5. Ils en ont ressorti un composé qui se nomme imidazopyridine (UK 107,543). Par la suite, ils ont fait diverses manipulations de ce composé pour qu'il soit plus spécifique au CCR5, qu'il ait une meilleure biodisponibilité pour que la molécule soit prise oralement et qu'elle soit mieux absorbée, bref qu'elle soit plus efficace. Une des molécules qu’ils en ont tirées est le maraviroc (UK-427,857). Ce composé a un poids moléculaire de 514 g/mol, il est modérément lipophile et il est basique. Après différentes études cliniques, le maraviroc a été approuvé en août 2007 par la Fédération américaine des aliments et des drogues (FDA).
Mutation Delta 32
Ce qui a mis sur la piste des antagonistes des récepteurs CCR5 comme maraviroc, est la mutation naturelle qui se retrouve dans la population caucasienne. Elle est retrouvée de 15 à 20 % à l’état hétérozygote chez cette population et à 1 % à l’état homozygote. Cette mutation confère une résistance aux souches de VIH-1 qui utilisent le CCR5 comme corécepteur. En effet, cette mutation est une délétion de 32 nucléotides qui résulte en une protéine CCR5 tronquée qui ne sera pas exprimée à la surface des cellules exprimant habituellement ce récepteur. L’état homozygote confère donc une très grande protection contre l’infection même si certaines exceptions peuvent survenir. La mutation hétérozygote (quant à elle) entraîne une progression plus lente de la maladie.
Mécanisme d’action
Comme mentionné plus tôt, le VIH utilise un corécepteur pour infecter les cellules. Ce corécepteur peut être de deux natures : soit CCR5 soit CXCR4. Ce sont des récepteurs de chimiokines. Les chimiokines sont de petites protéines solubles qui jouent un rôle dans l’attraction des leucocytes selon un gradient de concentration durant la réponse inflammatoire. On divise leurs récepteurs en deux classes selon la position des cystéines (CC ou CXC). La reconnaissance de ces récepteurs est faite chez le virus par une portion de la gp120 de la membrane virale nommée V3 qui est d’environ 35 acides aminés. Les virus CXCR4 sont caractérisés par un acide aminé chargé positivement aux positions 11 et/ou 25 dans cette boucle V3, tandis que le virus CCR5 n’en a pas. Selon cette boucle, le virus utilise soit CCR5 soit CXCR4 pour l’interaction avec la cellule et cela détermine son tropisme. Il est possible pour la même particule virale d’utiliser les deux récepteurs (tropisme mixte). Dans le cas du maraviroc, il se lie sélectivement au récepteur CCR5. Il empêche donc l’entrée des virus de ce tropisme. Il n’a aucun effet sur les virus à tropisme CXCR4 ou à tropisme mixte. Dès lors, il est essentiel de faire le test de tropisme avant d’ajouter le maraviroc au traitement. De plus, le maraviroc est utilisé contre le VIH-1 seulement. Il a aussi été testé sur divers sous-types de ce virus et il est efficace autant sur le sous-type B que sur les sous-types non-B. Il n’y a pas non plus de restriction par rapport à l’emplacement géographique de la provenance du virus.
Tropisme
La plupart des virus, qui sont transmis lors de l’infection au VIH, sont des virus à CCR5 tropisme. Ce sont eux qui domineront durant la majeure partie de la maladie. Ils sont la population présente durant la phase asymptomatique. Il y aura apparition du tropisme CXCR4 environ dans 60 % des cas d’infection dans les phases les plus tardives de la maladie. Par contre, on ne peut pas associer la présence de ce dernier tropisme avec l’aggravation de la maladie. Le laboratoire Monogram Biosciences[7] en Californie (États-Unis) commercialise un test prédictif de la sensibilité potentielle d'un malade aux différents traitements anti-VIH dont le maraviroc (Trofile® pour les malades ayant plus de 1000 copies du virus dans le sang circulant et Trofile® DNA pour les malades prouvés, atteints par le VIH mais ayant une charge virale indétectable).
Résistance
Les constantes mutations du virus, qui entraînent la résistance aux diverses molécules sur le marché, sont un grand défi pour la science. Malheureusement, le maraviroc n’échappe pas à ces résistances. La résistance naturelle au maraviroc n’est pas tellement présente puisqu’il a un large spectre d’action. Par contre, une résistance peut apparaître à la suite du traitement. Il existe deux mécanismes utilisés par le virus pour faire des mutations. Le plus utilisé est d’avoir plusieurs mutations dans la boucle V3 de la gp120 et ailleurs dans cette même protéine. Ces mutations résulteraient en l’entrée du virus par interaction avec le CCR5 même si le maraviroc y serait lié.
Le deuxième mécanisme serait l’échappement au maraviroc par le changement vers le CXCR4 tropisme. En effet, il serait possible pour le CCR5 de muter en faisant divers changements dans sa portion V3 de sa gp120 qui entraîneraient une reconnaissance de CXCR4 plutôt que de CCR5. Ceci diminue son activité virale. On ne sait toutefois pas à quelle fréquence cela survient. Une des difficultés vient de l’apparition du CXCR4 tropisme qui existe dans le cours normal de l’infection chez environ 60 % des cas. Il est donc difficile de voir une corrélation entre l’administration du maraviroc et le changement de tropisme par mutation du CCR5 vers le CXCR4. Il serait possible que les virus CXCR4 soient déjà présents mais en très faible quantité pour qu’ils ne soient pas détectés par le test de tropisme et que ces virus soient sélectionnés à cause du maraviroc. À ce moment, le trop grand nombre de CXCR4 pourrait faire échouer le traitement. Durant les études cliniques (MOTIVATE 1 et 2), chez les personnes recevant du maraviroc, en comparaison avec le groupe ayant reçu un placebo, le compte de cellule CD4 était meilleur même si à la fin de l’essai, il y avait des CXCR4 tropismes. De plus, chez les personnes recevant le traitement, il y avait moins de clones CCR5. Ceci indique l’efficacité du maraviroc.
Monographie
Description
Les comprimés sont de forme ovale, biconvexe et ont une couleur bleue. Les comprimés contiennent soit 150 mg, soit 300 mg de maraviroc.
Administration
La dose habituelle de maraviroc est de 300 mg deux fois par jour. Ces recommandations ont été faites à la suite d'une étude clinique (MOTIVATE 1 et 2) qui a démontré que c’est à cette dose que la réponse virologique était la meilleure. On donnera la même dose pour des gens qui prennent d’autres types d’antiviraux. On ajuste la dose en fonction des autres médicaments qui sont administrés en concomitance. On diminuera la dose à 150 mg deux fois par jour si on l’administre avec un inhibiteur du CYP3A4 puisque le médicament sera métabolisé moins vite et donc restera plus longtemps actif dans le corps. Au contraire, on augmentera la dose à 600 mg deux fois par jour si on l’administre avec un inducteur du CYP3A4 puisque le médicament sera métabolisé plus vite et donc n’aura pas le temps de faire son action. Aucun test n’a été fait chez les enfants, par conséquent le maraviroc ne doit pas leur être administré.
Absorption
La biodisponibilité d’une dose de 100 mg est de 23 %. Il faut environ 0,5 à 4 heures pour que le maraviroc atteigne sa concentration maximale dans le plasma. Ce médicament peut être pris avec ou sans nourriture.
Distribution
Son volume de distribution est de 194 litres. Le maraviroc présente une affinité modérée pour l’albumine. Il se lie à environ 76 % des protéines plasmatiques humaines. Il est environ 10 % de la concentration plasmatique libre du liquide céphalorachidien selon des données recueillies chez les rats.
Biotransformation
Le maraviroc est surtout métabolisé par le foie, plus précisément par le cytochrome P450 (CYP3A4) s’y trouvant. Les métabolites qui en découlent ne sont pas actifs contre le VIH.
Élimination
La demi-vie du maraviroc est d’environ 14 à 18 heures. On retrouve dans l’urine 20 % du médicament et dans les selles on retrouve 78 % de ce dernier.
Effets indésirables
Le maraviroc a une très grande affinité pour les récepteurs CCR5 et donc entraîne très peu d’effets secondaires. Les effets indésirables rencontrés le plus fréquemment sont : la diarrhée, les nausées et les céphalées. Tous étaient d’intensité légère à modérée. Les études cliniques (MOTIVATE 1 et 2, MERIT) n’ont pas révélé d’hépatotoxicité. Sans une trop grande incidence, il augmente les infections aux virus de l’herpès, les infections hautes du tractus respiratoire, les sinusites et les infections à l’influenza en comparaison avec le groupe recevant le placebo. Le blocage des récepteurs CCR5 peut amener la diminution de l’immunité et augmente les risques de développement de tumeurs. Durant les études cliniques, on a révélé un plus grand nombre de développement symptomatique du virus du Nil chez les gens ayant une mutation delta 32. Le blocage du CCR5 doit donc être surveillé.
Études cliniques
Pour l’instant, comme il n’y a pas de vaccin de disponible sur le marché pour enrayer la maladie, il existe trois façons possibles de réduire la transmission du VIH. La première façon est celle qui a été décrite jusqu’à maintenant, c’est-à-dire le traitement des gens infectés pour diminuer le taux de virions dans les sécrétions. Plusieurs études sont en cours pour toujours améliorer les molécules, en connaître parfaitement leurs mécanismes et leurs effets nocifs ou indésirables. La deuxième façon est la prophylaxie post-exposition qui peut se faire grâce à certaines molécules prises oralement. La troisième façon est la prophylaxie pré-exposition, c’est-à-dire avant d’être en contact avec le virus. Elle peut se faire soit topique (par exemple par des gels vaginaux) soit oralement.
Cette dernière façon est une avenue possible de développement pour le maraviroc. En effet, des recherches sont en cours pour savoir si le maraviroc pourrait être un bon médicament à être utilisé en prévention par les gens à risque d’infection. La preuve a été faite chez des primates donc un essai clinique a été effectué chez des femmes. Elles ont reçu 1 dose de 300 mg de maraviroc deux fois par jour pendant les jours 1 à 6 et une dose de 300 mg le matin du 7e jour. Par la suite, le fluide cervicovaginal, du tissu vaginal et du plasma sanguin ont été recueillis. Il a été établi que le maraviroc est, parmi les 17 antiviraux testés, celui qui a la plus grande concentration dans le fluide cervicovaginal. De plus, cette concentration était disponible chez 50 % des femmes une heure après l’administration et chez 100 % des femmes deux heures après l’administration. Il a aussi été démontré que la liaison du maraviroc avec des protéines était 10 fois moins élevée dans le fluide cervicovaginal que dans le plasma sanguin ce qui laisse supposer que le maraviroc est disponible pour un effet pharmacologique. Par contre, l’affinité avec le CCR5 n’a pas été démontrée dans cette étude. En bref, la conclusion de cette étude est que le maraviroc était présent en grande concentration dans la voie génitale chez la femme.
Comme il a été vu dans la section tropisme, les virus qui sont transmis d’un individu à l’autre sont des virus CCR5 tropisme. Il serait donc avantageux de pousser les recherches dans cette voie et de pouvoir mener à l’administration du maraviroc pour la prévention de la transmission hétérosexuelle.
Autres effets
Le CCR5 a un rôle probable dans la progression de l'athérome. Dans un modèle animal d'athérome induit par le ritonavir, l'ajout de maraviroc permet de freiner la progression des lésions artérielles[8].
Bibliographie
- Maraviroc: The First of a New Class of Antiretroviral Agents, R. D. MacArthur et R. M. Novak, Oxford journals, Vol. 47, Issue 2, p. 236-241.
- Maraviroc for Previously Treated Patients with R5 HIV-1 Infection, Roy M. Gulick et plusieurs autres, 2 octobre 2008, The New England Journal of Medicine, Vol. 359 No.14, p. 1429-1439.
- Subgroup Analyses of Maraviroc in previously Treated R5 HIV-1 Infection, Gerd Fätkenheuer et plusieurs autres, 2 octobre 2008, The New England Journal of Medicine, Vol. 359 No.14, p. 1442-1455.
- Emergence of CXCR4-Using Human Immunodeficiency Virus Type 1 (HIV-1) Variants in a Minority of HIV-1-Infected Patients following Treatment with the CCR5 Antagonist Maraviroc Is from a Pretreatment CXCR4-Using Virus Reservoir, M. Westby, M. Lewis, J. Whitcomb, M. Youle, A. L. Pozniak, I. T. James, T. M. Jenkins, M. Perros et E. Van der Ryst, mai 2006, Journal of Virology, Vol. 80 No.10, p. 4909-4920.
- Reduced Maximal Inhibition in Phenotypic Susceptibility Assays Indicates that Viral Strains Resistant to the CCR5 Antagonist Maraviroc Utilize Inhibitor-Bound Receptor for Entry, M. Westby, C. Smith-Burchnelle, J. Mori, M. Lewis, M. Mosley, M. Stockdale, P. Dorr, G. Ciaramella et M. Perros, mars 2007, Journal of Virology, Vol. 81 No. 5, p. 2359-2371.
- Maraviroc (UK-427,857), a Potent, Orally Bioavailable, andSelective Small-Molecule Inhibitor of Chemokine Receptor CCr5 with Broad-Spectrum Anti-Human Immunodefiency Virus Type 1 Activity , P. Dorr, M. Westby, S. Dobbs, P. Griffin, B. Irvine, M. Macartney, J. Mori, G. Rickett, C. Smith-Burchnell, C. Napier, R. Webster, D. Armour, D. Price, B. Stammen, A. Wood et M. Perros, novembre 2005, Antimicrobial Agents and Chemotherapy, Vol. 49 No.11, p. 4721-4732.
- Récepteurs de chimiokines et entrée du VIH, M. Alizon, novembre-décembre 1997, Virologie, Vol. 1 No. 6.
- Comment CCR5 et CD4, les deux composants du récepteur cellulaire du virus du SIDA (VIH), sont amenés à s’associer, S. Marullo, Institut de Cochin, (Page consultée le 20 avril 2011) [En ligne], adresse URL : http://cochin.inserm.fr/l_actualite/evenements-des-annees-precedentes/comment-ccr5-et-cd4-les-deux-composants-du
- Maraviroc Concentrates in the Cervicovaginal Fluid and Vaginal Tissue of HIV-Negative Women, J. Dummond, K. B. Patterson, A. L. Pecha, R. E. Werner, E. Andrews, B. Damle, R. Tressler, J. Worsley et A. D. M. Kashuba, (Page consultée le 20 avril 2011) [En ligne], adresse URL : https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2751766/
- Chemokine receptor expression in the human ectocervix: implications for infection by the human immunodeficiency virus type-1, G.R. Yeaman, S. Asin, S. Weldon, D. J. Demian, J. E. collins, J. L. Gonzalez, C. R. Wira, M. W. Fanger et A. L. Howell, Immunology, Vol. 113 (4).
- Monographie de Celsentri, Compendium des produits et spécialités pharmaceutiques
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Abel S, Russell D, Whitlock LA, Ridgway CE, Nedderman AN, Walker DK, « Assessment of the absorption, metabolism and absolute bioavailability of maraviroc in healthy male subjects », British Journal of Clinical Pharmacology, vol. 65, no Suppl 1, , p. 60–7 (PMID 18333867, PMCID 2311408, DOI 10.1111/j.1365-2125.2008.03137.x)
- (en) Abel S, Back DJ, Vourvahis M, « Maraviroc: pharmacokinetics and drug interactions », Antiviral Therapy, vol. 14, no 5, , p. 607–18 (PMID 19704163)
- INPI No 3429735 classe 38
- Circulaire cadre DGS/DSS/DH/DAS no 97/166 relative au nouveau dispositif de dispensation et de prise en charge des antirétroviraux.
- Arrêté du 10 octobre 2008 modifiant l'arrêté du 17 décembre 2004 modifié fixant la liste prévue à l'article L. 5126-4 du code de la santé publique (JO du 15/10/2008).
- « Providing Information to Help Patients Get the Most from Antiretroviral Therapy », sur www.monogramvirology.com (consulté le 8 septembre 2016)
- Cipriani S, Francisci D, Mencarelli A et al. Efficacy of the CCR5 antagonist maraviroc in reducing early, ritonavir-induced atherogenesis and advanced plaque progression in mice, Circulation, 2013;127:2114-2124
- Portail de la virologie
- Portail de la pharmacie
- Portail de la chimie