Métabolisme du fer
Le métabolisme du fer est l'ensemble des réactions chimiques visant à l'homéostase du fer. Le fer est indispensable pour la majorité des êtres vivants, en intervenant dans les réactions biochimiques de la vie cellulaire. Il est utilisé pour transporter l'oxygène dans les globules rouges.
Le fer est absorbé par voie digestive, en pouvant se présenter sous deux formes : le fer héminique (viandes et poissons) beaucoup mieux absorbé que le fer non héminique (végétaux et produits laitiers).
Chez l'homme, la majorité du fer utilisé (70%) est incorporé à l'hémoglobine (transport de l'oxygène par les globules rouges) ; 20 % dans la myoglobine des cellules musculaires ; 10 % dans les autres cellules de l'organisme qui ont toutes besoins de fer. L'essentiel de ce fer (95%) est utilisé en circuit fermé par recyclage. L'homme absorbe et excrète relativement peu de fer.
Le métabolisme du fer est déterminé par des cellules digestives, sanguines et hépatiques, en rapport avec des protéines spécifiques de transport, stockage, et régulation. Depuis les années 1990, les approches de génétique moléculaire permettent d'en détailler le mécanisme.
Les besoins en fer varient selon l'âge et le sexe. Ils sont les plus élevés lors de la grossesse et lors de la croissance du tout petit enfant.
Tout déséquilibre du métabolisme du fer, d'origine génétique ou environnementale, est nuisible que ce soit par déficit ou par surcharge
Aspects historiques
Utilisation médicinale du fer
L'usage thérapeutique du fer est mentionné en médecine égyptienne vers l'an 1500 av. J.-C.[1], dans le Papyrus médical de Berlin (Bln 88). Il est utilisé comme remède à appliquer sur les morsures venimeuses : le fer est pilé (réduit en limaille – parcelles de fer provenant du limage –) dans de l'eau provenant de la crue du Nil[2].
Sous la Rome Antique, la limaille ou poudre de fer peut être avalée dans du vin ou du vinaigre, ce qui suggère l'existence de carence en fer. En médecine arabe et médecine médiévale, le fer peut être pris aussi sous la forme de sirop[1].
En 1681, Thomas Sydenham mentionne l'effet du fer sur la chlorose (terme historique désignant très probablement l'anémie ferriprive, par carence en fer) : « le pouls gagne en force et en fréquence (...), le teint n'est plus pâle comme la mort, mais vif et haut en couleur »[1].
En 1831, le médecin Jean-Pierre Blaud (1773-1859) invente la pilule Blaud[3], première formulation moderne du fer, à base de sulfate ferreux et de carbonate de potassium, qu'il présente en 1832 comme un traitement de la chlorose qui « redonne au sang sa qualité perdue, à savoir celle d'être une substance colorante »[1].
Méthodes d'études
Le métabolisme du fer a été étudié en trois grandes étapes.
Au XIXe siècle, les études d'anatomo-pathologie, de cytochimie et d'histochimie, ont permis une première approche de la répartition normale et pathologique du fer dans l'organisme. Par prélèvement sanguin ou biopsie d'organe, il devient possible de distinguer entre autres, les anémies par défaut de fer, comme les surcharges en fer, en particulier au niveau du foie (sidérose hépatique ou hépatosidérose)
Au cours du XXe siècle, la dynamique du métabolisme du fer a pu être approchée par la technique d'utilisation des isotopes (isotopes de fer radioactif, médicaux ou biologiques, à demi-vie courte). Ces méthodes ont permis de mesurer la vitesse du passage du radio-fer dans le sang, l'absorption intestinale du fer, son devenir dans les organes, en particulier dans la moelle osseuse chez les précurseurs des globules rouges[4].
À partir des années 1990, le savoir fait un nouveau bond, avec la biologie moléculaire et surtout la génétique moléculaire (entre autres utilisation de souris transgéniques) qui permettent d'approcher la génétique et le métabolisme complexe du fer à l'échelle moléculaire.
Importance et rôle du fer
Monde vivant
Le fer est un élément indispensable pour la majorité des êtres vivants, notamment pour le transport de l'oxygène, et en particulier pour le transport et l'échange des électrons (Fe2+ ↔ Fe3+) lors des réactions d'oxydo-réduction (respiration cellulaire et fonctionnement enzymatique)[5].
Cependant à l'état libre, le fer est également très toxique, car les radicaux libres de fer altèrent les structures cellulaires. Les atomes de fer sont toujours utilisés et « contrôlés » en restant liés à diverses molécules et protéines spécifiques pour leur absorption, transport, stockage, utilisation et excrétion. Ce sont autant d'étapes du métabolisme du fer[6].
Certaines algues et bactéries des eaux ferrugineuses sont très riches en fer, elles oxydent le fer ferreux Fe2+ en fer ferrique Fe3+ pour trouver l'énergie nécessaire à l'assimilation du CO2[7]. Presque tous les micro-organismes ont besoin de fer, notamment pour leur cytochrome.
Quand il y a peu de fer disponible dans le milieu, la plupart des micro-organismes sécrètent des sidérophores, petites molécules de captation et transport de fer. Le complexe ainsi formé se lie alors à un récepteur de la membrane cellulaire. Le fer pénétrant dans la cellule est réduit en fer ferreux Fe2+. Il existe plusieurs voies et mécanismes d'absorption pour obtenir une quantité suffisante de fer[8].
Chez les végétaux supérieurs, le fer est indispensable à la formation de la chlorophylle, bien que n'entrant pas dans la composition de sa structure[7].
Humains
De façon générale, le métabolisme du fer « fonctionne à l'économie ». L'essentiel du fer de l'organisme tourne en circuit fermé, par recyclage. En situation d'équilibre, les humains absorbent et excrètent relativement peu de fer. Du point de vue évolutif, ce métabolisme serait l'adaptation à une pression de sélection exercée par l'environnement (plus ou moins riche en fer), et par les micro-organismes pathogènes qui utilisent le fer circulant des organismes supérieurs qu'ils parasitent[9] (voir la régulation négative par hepcidine).
L'organisme humain contient de 30 à 40 mg de fer par kg de poids, soit autour de 3 à 5 g chez un adulte. Il en perd quotidiennement 1 à 2 mg en moyenne par les sécrétions et desquamation intestinales et cutanées (éliminations des cellules mortes superficielles), la sueur et l'urine, auxquelles il faut ajouter le sang menstruel[6].
Chez l'homme, il n'existe pas de régulation de cette excrétion, la principale régulation s'opère au niveau de l'absorption digestive du fer, et cette absorption est relativement limitée par rapport aux autres mammifères. Cette étape intestinale est cependant essentielle, car c'est par là que l'organisme humain, à l'état normal, bloque un excès de fer ou compense ses pertes, en adaptant l'absorption selon les possibilités et ses besoins[6].
La majorité du fer utilisé (70%) est incorporé à l'hémoglobine (transport de l'oxygène par les globules rouges) ; 20 % dans la myoglobine des cellules musculaires ; 10 % dans les autres cellules de l'organisme qui ont toutes besoins de fer. La répartition du fer dans l'organisme est aussi strictement contrôlée à partir de la biodisponibilité en fer du secteur sanguin (fer plasmatique) et de son stockage hépatique[5].
Au total il existe 4 types cellulaires principaux qui déterminent le métabolisme du fer[9] :
- les entérocytes, cellules intestinales qui absorbent le fer.
- les érythroblastes, cellules-souches ou précurseurs des globules rouges, qui captent et transportent le fer utilisable.
- les macrophages, qui récupèrent et « recyclent » le fer des globules rouges en fin de vie.
- les hépatocytes, cellules du foie qui stockent le fer, et qui jouent un rôle de « gestion du stock ».
La circulation de fer entre ces quatre types cellulaires est assuré par des protéines spécifiques. Dans les années 1970-1980, on n'en connaissait que deux : la ferritine et la transferrine. En 2006, plus de 20 protéines ont été identifiées à différentes étapes du métabolisme du fer[10], dont l'hepcidine (hormone de régulation du fer dans l'organisme) et les protéines régulatrices du fer (régulation intra-cellulaire)[5].
Tout déséquilibre du métabolisme du fer, d'origine génétique ou environnementale, est nuisible que ce soit par déficit ou par surcharge[5].
Absorption digestive
Pour la teneur des aliments, voir la section Aliments riches en fer.
Les apports alimentaires moyens sont de 15-20 mg par jour lors d'un régime équilibré. Ils sont largement supérieurs aux besoins réels de l'organisme (sauf parfois en situation de grossesse), qui perd habituellement de façon incompressible 1 à 2 mg de fer par jour en moyenne. À l'état normal, seul le fer alimentaire nécessaire (compensant les pertes) est absorbé.
L'absorption intestinale se situe principalement dans le grêle au niveau du duodénum et du jéjunum. Elle est régulée en fonction de la quantité de fer dans l'organisme, de l'intensité de la production de globules rouges (érythropoïèse), et elle dépend de la nature du fer alimentaire.
Le fer ne peut être transporté dans sa forme minérale que dans sa forme ferreuse.
Fer alimentaire
Il existe deux types de fer alimentaire :
- le fer héminique, ainsi nommé car il est lié à l'hème, métalloprotéine que l'on trouve dans les viandes et les poissons.
- le fer non héminique, qui se trouve dans les céréales, les fruits, les légumes secs, les légumes et les produits laitiers.
Le rendement d'absorption de ces deux types de fer est très différent : celui du fer héminique est de 10 à 30 %, très supérieur à celui du fer non héminique (1 à 5 %). Le fer héminique représente les 2 tiers du fer absorbé alors qu'il ne constitue que le tiers des apports alimentaire (régime occidental standard).
De plus, l'absorption du fer héminique est très peu influencée par les autres aliments, alors que ce n'est pas le cas du fer non héminique. Par exemple l'absorption du fer non héminique se fait au mieux en présence de vitamine C, alors qu'elle est entravée par les tanins (thé vert), ovalbumine (blanc d'œuf), caséine du lait, protéines de soja[6]...
Dans l'estomac, les protéines héminiques (hémoglobine, myoglobine) sont découpées par l'acide gastrique, et l'hème (porteur de fer) ainsi libéré est capté par les cellules (entérocytes) du duodénum et du jéjunum.
Avant son absorption proprement dite, le fer non héminique (fer inorganique ou minéral ferrique) doit être réduit et libéré de ses complexes. Ce processus est facilité par l'oxydation de la vitamine C.
Absorption par les entérocytes
Seule une faible fraction (10-20 %) du fer ingéré est absorbée par l'intestin grêle. Elle se fait au niveau des entérocytes en 3 étapes : captation du fer de la lumière intestinale au sommet de la cellule (pole apical), puis transfert intracellulaire vers la base de la cellule, et libération dans le secteur sanguin par franchissement du pole basal.
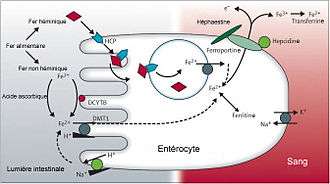
Le fer héminique serait capté par le récepteur de l'hème HCP1 (Heme Carrier Protein 1), une fois dans l'entérocyte, le fer est libéré de son noyau hème par une hème oxygénase. La captation du fer non héminique fait intervenir la ferriréductase, Dcytb (Duodenal cytochrome b) qui réduit le fer ferrique alimentaire en fer ferreux[5].
Deux protéines au moins, insérées dans la membrane apicale de l'entérocyte. contrôlent cette absorption : les transporteurs spécifiques Nramp2 ( Natural resistance-associated macrophage protein 2) appelé aussi DMT1 (dimetal transporter 1), et HFE (protéine dont le gène muté induit une hémochromatose) liée à la β 2 microglobuline[6].
Une fois que le fer est entré dans l'entérocyte, il forme un premier stock dynamique. Selon les besoins de l'organisme, soit il est retenu (lorsque le statut en fer est correct) sous forme de ferritine, puis éliminé à la mort de l'entérocyte (desquamation cellulaire), soit il est libéré à la face basale de ces cellules, vers la circulation sanguine
Le fer destiné à être libéré par l'entérocyte est pris en charge par le transporteur ferroportine sous sa forme ionique ferreuse Fe2+, qui lui fait franchir le pole basal. Il est immédiatement oxydé par l'héphaestine (ferrioxydase synthétisée par le foie) et qui le transforme dans sa forme ferrique Fe3+ au niveau de la membrane basale de l'entérocyte[5].
La sortie du fer de l'entérocyte est contrôlée par une hormone synthétisée par le foie, l'hepcidine, qui bloque et dégrade la ferroportine.
Transport et stockage
Dans tout l'organisme, le transport et la distribution du fer dans tout l'organisme se fait principalement par la transferrine, alors que le stockage se fait sous forme de ferritine.
Fer circulant
Le fer circulant a deux origines : le « nouveau » fer (5 %) libéré par l'entérocyte, et le fer « recyclé » (95 %) libéré par les macrophages[6]. La concentration en fer dans le plasma est de 12 à 25 μmol/L[5].
Le Fe3+ libéré par l'entérocyte est fixé par la transferrine (ou sidérophilline) qui est son transporteur plasmatique, pouvant lier théoriquement deux ions ferriques. En état normal (situation d'équilibre), la capacité de fixation de la transferrine circulante est suffisante pour empêcher ou limiter toute concentration délétère de fer plasmatique[9]. Le taux de transferrine dans le plasma est de 2 à 4 g/L[5].
En situation pathologique de surcharge en fer, la transferrine est saturée à partir de 30% en plus de sa capacité moyenne. Le fer additionnel libéré dans la circulation se lie à des petites molécules de bas poids moléculaire, c'est le fer non non lié à la transferrine dont une fraction possède une activité redox toxique pour la vie cellulaire[9].
De la même façon, la transferrine fixe le fer libéré par les macrophages du système réticulo-endothélial. Les macrophages ont récupéré ce fer, surtout au niveau de la rate, en phagocytant les cellules vieillies (surtout globules rouges) et desquamées. En situation d'équilibre, les macrophages libèrent environ 25 mg par jour de fer recyclé qui est immédiatement ré-utilisé du fait que le pool de fer lié à la transferrine circulante représente moins de 3 mg. Ce recyclage s'effectue une dizaine de fois par jour[9].
Le fer utilisable est distribué dans tout l'organisme, principalement la moelle osseuse (pour l'hémoglobine) pour 70 %, puis les muscles (pour la myoglobine). pour 20 %[5].
Stockage du fer
Le fer est stocké sous la forme de ferritine. Le stockage le plus important est celui des cellules du foie ou hépatocytes. Les hépatocytes jouent aussi un rôle déterminant produisant l'hepcidine, hormone régulant le niveau du fer absorbé et libéré dans la circulation. Voir la section régulations.
Métabolisme intracellulaire
La pénétration du fer dans les cellules autres que les entérocytes se fait par captation de la transferrine, grâce aux récepteurs de la transferrine.
Chaque récepteur peut fixer deux molécules de transferrine donc quatre atomes de fer. Le complexe Fe3+ - transferrine est internalisé par endocytose. La diminution du pH dans la vésicule d'endocytose permet la libération et la réduction du Fer sous l'action d'une ferriréductase[5].
Le fer réduit en forme ferreuse est transporté par la protéine Nramp2/DMT1 vers le cytoplasme ; tandis que le récepteur à la transferrine est recyclé vers la membrane plasmique, de nouveau disponible pour capter le fer. Ce cycle dure dure environ dix minutes. La moelle osseuse, par le biais des érythroblastes (précurseurs des globules rouges), capterait ainsi près de vingt mille atomes de fer par minute[6].
Le fer libre est extrêmement réactif dans les cellules. Il doit ainsi être stocké lié à une protéine de stockage.
Une fois entré dans une cellule, les atomes de fer peuvent être utilisés pour les besoins suivants :
- métabolisation directe (synthèse d'agrégat fer-soufre par exemple) ;
- fixation à la ferritine, protéine de stockage intracellulaire ;
- fixation à des facteurs de transcription et activation des gènes sensibles au fer, par un système de protéine régulatrice du fer et d'élément de réponse au fer.
- création d'hème dans les précurseurs des globules rouges (cellules de l'érythropoïèse).
Régulations
La régulation du métabolisme du fer se fait par des signaux impliquant la tension en oxygène et les besoins systémiques de fer. L'hormone principale qui régule l'absorption intestinale de fer est l'hepcidine synthétisée par le foie.
Lorsque les niveaux de stockage hépatique de fer et du fer circulant sont suffisants, l'hepcidine est exprimée. Elle a pour propriété de bloquer la ferroportine, donc l'entrée de fer dans le secteur sanguin au niveau duodénal (entérocytes) et splénique (macrophages). L'hepcidine joue un rôle « hyposidérémique » (elle tend à abaisser le niveau de fer, lorsqu'il est plus que suffisant)[11].
Lorsque, pour diverses raisons, l'érythropoïèse (production de globules rouges) augmente, l'hepcidine décroit, ce qui augmente l'absorption digestive de fer.
Dans des situations d'hypoxie (insuffisance d'oxygène), par exemple liées à une anémie, la production d'hepcidine est inhibée et l'absorption digestive de fer accrue.
De façon générale, la production d'hepcidine est plus influencée par l'activité de l'érythropoïèse que par le statut en fer[9]. Ainsi lorsqu'une anémie coexiste avec une surcharge en fer, le signal hypoxie/anémie est prédominant sur celui du statut en fer, ce qui permet d'expliquer l'aggravation de la surcharge en fer dans ce type d'anémie[12].
Pathologies liées au statut en fer
Ce sont celles de la carence ou au contraire de la surcharge.
Carences en fer
Voir aussi :
La carence en fer serait apparu chez l'homme avec l'avènement de l'agriculture, lors d'un régime alimentaire centré sur les céréales (fer non héminique prédominant avec déficit associé en vitamine C). Un déficit est susceptible de se manifester surtout chez la femme enceinte, ou dans les deux sexes après un saignement traumatique ou d'origine digestive chronique[13],[14].
Le plus souvent la carence est due à une insuffisance d'apport (ou à un déséquilibre par des pertes), plus rarement à une maladie par malabsorption ou après intervention digestive (en particulier chirurgie de l'obésité[15]).
Un déficit prolongé peut entrainer une anémie ferriprive ; chez l'enfant, une diminution des performances cognitives ; chez la femme enceinte, un risque plus élevé de prématurité et de mortalité infantile et maternelle ; des perturbations immunitaires et de la résistance au froid ont été aussi signalées[13].
La carence en fer peut s'observer partout dans le monde. Chez l'enfant, la carence d'apport est la principale cause d'anémie dans les pays en développement. Dans les pays industrialisés, un déficit relatif en fer (sans anémie) peut aussi se voir chez les enfants et les femmes enceintes.
Cependant, un déficit en fer peut aussi avoir un effet protecteur contre des infections bactériennes ou parasitaires (comme le paludisme), dont la virulence est atténuée. En effet ces micro-organismes utilisent le fer circulant de leur hôte[13]. La question de la supplémentation en fer des enfants ayant une infection chronique (paludisme, maladie diarrhéique...) avec anémie relative est donc discutée[16].
Surcharges en fer
Elles peuvent être d'origine génétique, voir :
Les autres surcharges peuvent être le fait de[17] :
- Transfusions sanguines répétées.
- Augmentation de l'absorption digestive : maladie hématologique, traitement martial, apport diététique (comme les boissons alcoolisées riche en fer et le fer provenant des ustensiles de cuisine chez les Bantous au XXe siècle[18]).
- Maladies d'organes particuliers (surcharge tissulaire) : hépatiques (comme la cirrhose alcoolique), pulmonaires (sidérose par inhalation de poussières de fer), rénales, implications dans la maladie de Parkinson[19], certaines formes de tumeurs (très rares)...
Besoins et apports
Il faut distinguer les besoins de fer, les apports alimentaires en fer, et la teneur des aliments riches en fer.
Besoins
Les besoins physiologiques en fer varient selon son âge et le sexe. Chez l'adulte des deux sexes, les besoins en fer sont déterminés par les pertes obligatoires de fer (autour de 1 mg de fer par jour). Pour les femmes, de la puberté à la ménopause, il faut ajouter les pertes en fer liées à la menstruation qui représentent de 12 à 15 mg par mois, soit 0,4 à 0,8 mg par jour. Les besoins totaux des femmes approchent les 2 mg par jour, soit près du double de ceux des hommes[20].
Du fait de la croissance (notamment de la masse des globules rouges), les besoins en fer de l'enfant par kilo de poids de corps sont supérieurs à ceux de l'adulte[21], par exemple, les besoins d'un enfant de un an sont 8 à 10 fois supérieurs à ceux d'un adulte (par kg de poids corporel)[20]. Les enfants sont donc une population à risque de carence en fer[22] . Chez l'adolescente, l'apparition des règles augmente le besoin de fer.
Le besoin de fer augmente considérablement durant la grossesse, jusqu'à 2,5 à 5 mg par jour, selon le niveau des réserves en fer au début de la grossesse[20].
Enfin tous les saignements, y compris les minimes mais répétés, augmentent les besoins de fer.
Apports recommandés
Les apports recommandés en fer alimentaire diffèrent des besoins compte tenu d'un rendement d'absorption variable. Ils sont donc très largement supérieur aux besoins (voir supra, section absorption digestive). Par apport recommandé, on entend une ration destinée à couvrir les besoins de 95 % des individus avec une variation interindividuelle de 15 %[6], compte tenu du régime alimentaire habituel d'une population[20].
Pour la population française, ces apports recommandés en fer sont estimés à 9 mg par jour pour les hommes (13 pour les adolescents) et de 14 mg par jour pour les femmes (16 pour les adolescentes)[23],[6]. Chez les femmes, l'apport est plus élevé à cause des règles.
Lors d'une grossesse, les apports recommandés sont de 20 mg à 30 mg par jour (pic au 3e trimestre). Le fer est généralement puisé dans les réserves de l'organisme, les besoins sont couverts par une alimentation équilibrée à condition que la ration alimentaire atteigne au moins 2000 kcal par jour. Une carence en fer peut survenir lors de grossesses multiples, d'allaitement prolongé, d'activité physique intense, de régime carencé... Il n'y a pas de justification à une supplémentation systématique en fer au cours de la grossesse, sauf cas particulier sur avis médical[24].
Pour la population américaine, la recommandation pour les femmes entre 19 et 50 ans est fixée à 18 mg, selon les Apports nutritionnels conseillés indiqués par le Département de l'Agriculture des États-Unis [25].
Bien que le fer des végétaux soit moins biodisponible, les apports en fer des végétariens sont le plus souvent identiques à ceux des non-végétariens. L'incidence de l'anémie par carence en fer n'est pas plus fréquente chez les végétariens que chez les non-végétariens[26].
Teneur des aliments riches en fer
Les deux tableaux suivants listent les aliments les plus riches en fer héminique et non héminique[27][réf. insuffisante]. Dans ces deux tableaux, les portions sont parfois différentes des 100 g habituels, pour des raisons de pertinence.
| Aliment | Portion | Fer | % recommandation [Quoi ?] |
|---|---|---|---|
| palourde | 100 g | 28 mg | 155 % |
| foie de porc | 100 g | 18 mg | 100 % |
| rognon d'agneau | 100 g | 12 mg | 69 % |
| huître cuite | 100 g | 12 mg | 67 % |
| seiche | 100 g | 11 mg | 60 % |
| foie d'agneau | 100 g | 10 mg | 57 % |
| pieuvre | 100 g | 9,5 mg | 53 % |
| moule | 100 g | 6,7 mg | 37 % |
| foie de bœuf | 100 g | 6,5 mg | 36 % |
| cœur de bœuf | 100 g | 6,4 mg | 35 % |
| Aliment | Portion | Fer | % recommandation [Quoi ?] |
|---|---|---|---|
| sucre de fleur de coco non raffiné[28][réf. obsolète] | 100 g | 34 mg | 242 % |
| soja | 250 ml | 9,3 mg | 52 % |
| haricots jaunes crus | 100 g | 7 mg | 39 % |
| lentilles | 250 ml | 7 mg | 39 % |
| flocons de maïs[27] | 30 g | 5 mg[27] | 28 % |
| falafel | 140 g | 4,8 mg | 27 % |
| graines de soja | 250 ml | 4,7 mg | 26 % |
| graines de sésame toastées | 30 g | 4,4 mg | 25 % |
| spiruline | 15 g | 4,3 mg | 24 % |
| racine de gingembre | 30 g | 3,4 mg | 19 % |
| épinard | 85 g | 3 mg | 17 % |
Cet autre tableau présente une liste plus étendue d'aliments, avec leur teneur en fer pour 100 g :
| Aliment | Teneur en fer (mg/100 g) |
|---|---|
| Algue laitue de mer | 5 à 200 |
| Spiruline et Varech | 100 |
| Basilic séché | 42 |
| Ortie | 41 |
| Boudin noir cuit | 20 |
| Foie de porc | 15 |
| Gingembre | 14 |
| Cacao | 10 à 12 |
| Biscotte complète Foie d'agneau ou de bœuf Persil Graine de sésame ou de citrouille | 10 |
| Fèves Lentille sèche | 9,0 |
| Clovisse (Palourde) | 8 |
| Foie de lapin | 7,9 |
| Haricot blanc sec | 7,5 |
| Pois chiche | 7,2 |
| Rognon de bœuf | 7,0 |
| Lentille cultivée Jaune d'œuf Moule Abricot sec | 6,0 |
| Huîtres, moules | 5,5 |
| Foie de veau Noix de cajou | 5,0 |
| Amande Noisettes séchées | 4,5 |
| Noix de coco sèche | 3,6 |
| Pruneau | 3,4 |
| Raisin sec | 3,3 |
| Pissenlit | 3,2 |
| Épinard | 2,7 |
| Œuf entier | 2,3 |
| Figue sèche, noix sèche Pain de seigle, viande | 2,0 |
La légende du fer dans les épinards
Contrairement aux croyances populaires, l'épinard n'est pas la meilleure source de fer alimentaire. En effet, il ne compte que 2,7 mg de fer pour 100 g de feuilles fraîches. Il en possède moins, par exemple, que les lentilles ou les haricots.
L'origine de cette croyance du taux élevé de fer dans les épinards aurait deux sources possibles. La première est une publication du chimiste allemand E. von Wolf datant de 1870 qui, en raison d'une erreur typographique sur une décimale, attribuait à l'épinard dix fois sa teneur réelle en fer[29],[30]. La seconde est une publication d'un autre chimiste allemand, Gustav von Bunge, qui, en 1890, trouvait 35 mg de fer pour 100 g mais dans l'épinard séché réduit en poudre[31]. La vérité sur la teneur en fer de ce légume vert fut rétablie par d'autres chimistes allemands en 1937[29] mais resta confidentielle jusqu'à ce que T.J. Hamblin fasse part de cette « supercherie » dans le British Medical Journal en 1981[32]. Mais à bien des égards, ce mythe de l'épinard comme le légume riche en fer par excellence est encore vivace aujourd'hui[31], car rendu très populaire par le personnage de Popeye.
Notes et références
- (en) Alfred Jay Bollet, Anemia, Cambridge University Press, (ISBN 0-521-33286-9), p. 572-573dans The Cambridge World History of Human Disease, K.F. Kiple (dir.).
- Thierry Bardinet, Les papyrus médicaux de l'Egypte pharaonique, Fayard, coll. « Penser la médecine », (ISBN 2-213-59280-2), p. 420.
- Maurice Bouvet, « Les pilules de Blaud », Revue d'histoire de la pharmacie, vol. 43, no 145, , p. 118–123 (DOI 10.3406/pharm.1955.8499, lire en ligne)
- Maurice Tubiana, Isotopes, 2009, Encyclopedia Universalis, (ISBN 978-2-35856-034-4), p. 109-110Les Essentiels d'Universalis, vol. 14.
- Olivier Loréal, « Métabolisme du fer », La Revue du Praticien, vol. 56, no 19, , p. 2111-2117.
- Jean-Luc Lafond, « Métabolisme du fer », La Revue du Praticien, vol. 50, no 9, , p. 945-949.
- Yves Najean, Fer (métabolisme du), t. VII, Encyclopedia Universalis, , p. 878-883.
- Prescott, Microbiologie, De Boeck, (ISBN 978-2-8041-6012-8), p. 109-110.
- (en) Robert E. Fleming, « Iron Overload in Human Disease », The New England Journal of Medicine, vol. 366, no 4, , p. 348-352.
- Yves Deugnier, « Surcharges en fer », La Revue du Praticien, vol. 56, no 19, , p. 2109-2110.
- Pierre Brissot, « Surcharges en fer », La Revue du Praticien, vol. 65, , p. 1305-1311.
- Axel Kahn, « Cibler l'hepcidine », Le Concours Médical, vol. 126, no 20, , p. 1119-1122.
- Bernard Grosbois, « Avant-propos », La Revue du Praticien, vol. 50, no 9, , p. 943-944.
- Gilles Deluc (préf. Henri de Lumley), La nutrition préhistorique, Pilote 24, (ISBN 2-9501983-8-4), p. 119-120.
- Jean-Louis Schlienger, Diététique en pratique médicale courante, Elsevier Masson, (ISBN 978-2-294-75384-8), p. 127.
- (en) Peter Gluckman, Principles of Evolutionary Medicine, Oxford University Press, (ISBN 978-0-19-923639-8), p. 273.
- Frédéric Galactéros, « Les surcharges en fer secondaires », La Revue du Praticien, vol. 50, no 9, , p. 983-987.
- M. Bourel, « Physiopathologie et classification des hémochromatoses », La Revue du Praticien, vol. 27, no 7, , p. 339-350
- « L'excès de fer dans les cellules nerveuses impliqué dans la maladie de Parkinson », sur INSERM, (consulté le 26 juillet 2015).
- Serge Hercberg, « Epidémiologie du déficit en fer », La Revue du Praticien, vol. 50, no 9, , p. 957-960.
- « Bibliothèque électronique de données factuelles pour les interventions nutritionnelles (eLENA) », sur www.who.int, (consulté le 1er mai 15)
- « Bibliothèque électronique de données factuelles pour les interventions nutritionnelles (eLENA) », sur www.who.int, (consulté le 5 janvier 15)
- Ambroise Martin, apport nutritionnel conseillé pour la population française, Parin, Tec&Doc, , 605 p.
- J.-L. Schlienger 2014, op. cit., p. 43.
- (en) « Dietary Reference Intakes (DRIs): Recommended Dietary Allowances and Adequate Intakes, Elements » [[https://web.archive.org/web/20130906180147/http://www.iom.edu/Activities/Nutrition/SummaryDRIs/~/media/Files/Activity%20Files/Nutrition/DRIs/5_Summary%20Table%20Tables%201-4.pdf archive du <time class="nowrap" datetime="2013-09-06" data-sort-value="2013-09-06">6 septembre 2013</time>]], sur Institute of Medicine of the National Academies (Food and Nutrition Board), (consulté le 5 mars 2015).
- J.-L. Schlienger 2014, op. cit., p. 20.
- Top Aliments - Fer. Top Aliments.
- http://www.nutri-naturel.com/edulcorants/228-sucre-de-coco-bio-500g-3760087360837.html
- (en) Gregory McNamee, Movable Feasts : The History, Science, and Lore of Food, Greenwood Publishing Group, , 194 p. (ISBN 0275989313).
- Jean-François Bouvet, Du fer dans les épinards et autres idées reçues, Seuil, coll. « Science ouverte », (ISBN 2020235080 et 978-2020235082).
- (en) Tom P. Coultate, Food : The Chemistry of Its Components, Royal Society of Chemistry, , 5e éd. (ISBN 0854041117).
- (en) T.J. Hamblin, « Fake! », British Medical Journal (Clin Res Ed), vol. 283, no 6307, , p. 1671--1674 (PMCID PMC1507475, lire en ligne).
Annexes
Articles connexes
Lien externe
- Table de composition nutritionnelle des aliments sur le site Ciqual de l'ANSES (Agence Nationale de sécurité sanitaire de l'alimentation, de l'environnement et du travail). Sélectionner « constituants » et indiquer « fer ».
- Portail de la médecine
- Portail de la biochimie
- Portail de la physiologie