Sulfure de baryum
Le sulfure de baryum est un composé inorganique de formule BaS. C'est un important précurseur d'autres composés du baryum, par exemple le carbonate de baryum (BaCO3) et le pigment lithopone (ZnS/BaSO4)[8]. Comme les autres chalcogénures de métal alcalino-terreux, BaS est un émetteur à courte longueur d'onde pour les afficheurs électroniques[9]. Il est incolore, bien que comme beaucoup de sulfures, il est le plus souvent obtenu sous des formes impures colorées.
Ne doit pas être confondu avec Sulfate de baryum.
| Sulfure de baryum | |
| |
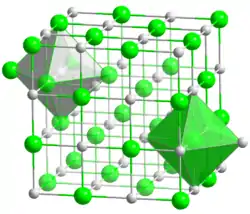
| structure cristalline __ Ba2+ __ S2− |
|
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.040.180 |
| No CE | 244-214-4 |
| PubChem | 6857597 |
| ChEBI | 32590 |
| SMILES | |
| InChI | |
| Apparence | cristaux cubiques incolores[1] avec une odeur d'œuf pourri[2] |
| Propriétés chimiques | |
| Formule | BaS |
| Masse molaire[3] | 169,392 ± 0,012 g/mol Ba 81,07 %, S 18,93 %, |
| Propriétés physiques | |
| T° fusion | 2 227 °C[2] 2 235 °C[4] |
| T° ébullition | se décompose |
| Solubilité | 73,5 g·L-1[2] |
| Masse volumique | 4,36 g·cm-3[2] |
| Thermochimie | |
| ΔfH0solide | −460 kJ·mol-1[5] |
| Cristallographie | |
| Système cristallin | cubique |
| Symbole de Pearson | cF8 |
| Classe cristalline ou groupe d’espace | Fm3m, no 225 |
| Structure type | Halite |
| Paramètres de maille | 639 pm[6] |
| Propriétés optiques | |
| Indice de réfraction | 2,155[réf. nécessaire] |
| Précautions | |
| SGH[2] | |
   Danger |
|
| NFPA 704[7] | |
| Composés apparentés | |
| Autres cations | Sulfure de magnésium Sulfure de calcium Sulfure de strontium |
| Autres anions | Oxyde de baryum Carbonate de baryum |
| Unités du SI et CNTP, sauf indication contraire. | |
Découverte et production
BaS a été préparé pour la première fois par l'alchimiste italien Vincenzo Cascariolo (Vincentius / Vincentinus Casciarolus / Casciorolus), 1571-1624) par la réduction de BaSO4 (sous la forme du minéral baryte)[10]. Il est actuellement fabriqué par une version améliorée du procédé de Casciarolo utilisant du coke à la place de charbon de bois et d'une panure de farine. Le procédé de thermo-sulfato réduction utilisé est également appelé réaction carbothermique :
- BaSO4 + 2 C → BaS + 2 CO2
et aussi :
- BaSO4 + 4 C → BaS + 4 CO
Du sulfure de baryum de haute pureté peut aussi être produit en petites quantités en chauffant du carbonate de baryum vers 1 000 °C dans un courant suffisamment important de sulfure d'hydrogène et d'hydrogène[6] :
- BaCO3 + H2S → BaS + H2O + CO2
Propriétés
BaS cristallise dans une structure de type cubique à faces centrées similaire à celle du chlorure de sodium (NaCl), avec des centres octaédriques Ba2+ et S2−.
Le point de fusion observé du sulfure de baryum est très sensible aux impuretés[4].
Le sulfure de baryum présente un risque d'inflammation, ou de déflagration, s'il est mis en contact avec des agents oxydants forts comme du dioxyde de plomb, du peroxyde de chlore, du chlorate de potassium ou du nitrate de potassium[2]. Il réagit avec le fluor, le pentoxyde de phosphore, les acides, l'eau et l'air humide (dégagement de sulfure d'hydrogène dans ces trois derniers cas)[2].
Phosphorescence
D'après Harvey (1957)[11], en 1603, le cordonnier et alchimiste italien Vincenzo Cascariolo utilisa de la barytine (BaSO4), trouvée au pied du mont Paterno près de Bologne, lors de l’un de ses essais infructueux pour fabriquer de l’or. Après avoir broyé et calciné le minéral en conditions réductrices sur du charbon de bois, il obtint un matériaux à la luminescence persistante qui fut baptisé Lapis Boloniensis, ou pierre de Bologne[12],[13],[14]. La phosphorescence du composé fabriqué par Casciarolo en fit une curiosité[15],[16],[17]. La nature exacte de l'élément actif contenu à l'état de trace dans cette barytine et responsable de la luminescence de BaS reste inconnue, mais la matrice de sulfure de baryum, comme celle d'autres sulfures (CaS, SrS, ZnS), est propice au phénomène de luminescence.
Toxicité
BaS est toxique, comme les sulfures apparentés, tels que le sulfure de calcium (CaS), qui dégagent du sulfure d'hydrogène toxique par hydrolyse au contact avec l'eau.
Références
- (de) Entrée Bariumsulfid sur Römpp Online. Georg Thieme Verlag, consultée le 14 juillet 2014.
- Entrée « Bariumsulfid » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 31 août 2019 (JavaScript nécessaire).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Stinn, C., Nose, K., Okabe, T. et al. Metall and Materi Trans B (2017) 48: 2922. https://doi.org/10.1007/s11663-017-1107-5
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor and Francis, , 90e éd., 2804 p. (ISBN 9781420090840, présentation en ligne), p. 6
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, (ISBN 3-432-87813-3), S. 927.
- Fiche Sigma-Aldrich du composé Barium sulfide, consultée le 31 août 2019.
- Holleman, A. F.; Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001. (ISBN 0-12-352651-5).
- Vij, D. R.; Singh, N. "Optical and electrical properties of II-VI wide gap semiconducting barium sulfide" Proceedings of SPIE (1992), 1523 (Conf. Phys. Technol. Semicond. Devices Integr. Circuits, 1992), 608-12.
- F. Licetus, Litheosphorus, sive de lapide Bononiensi lucem in se conceptam ab ambiente claro mox in tenebris mire conservante, Utini, ex typ. N. Schiratti, 1640. See http://www.chem.leeds.ac.uk/delights/texts/Demonstration_21.htm
- Harvey E. Newton (1957). A History of Luminescence: From the Earliest Times until 1900. Memoirs of the American Physical Society, Philadelphia, J. H. FURST Company, Baltimore, Maryland (USA), Vol. 44, Chapter 1, pp. 11-43.
- (en) Luminescence applications in biological, chemical, environmental and hydrological sciences, Marvin C. Goldberg, , 255 p.
- Philippe F. Smet, Iwan Moreels, Zeger Hens et Dirk Poelman, « Luminescence in Sulfides: A Rich History and a Bright Future », Materials, vol. 3, no 4, , p. 2834–2883 (ISSN 1996-1944, DOI 10.3390/ma3042834)
- Hardev Singh Virk, « History of Luminescence from Ancient to Modern Times », sur ResearchGate, (consulté le )
- « Lapis Boloniensis », www.zeno.org
- Lemery, Nicolas, Traité universel des drogues simples, (lire en ligne)
- Ozanam, Jacques, Montucla, Jean Etienne et Hutton, Charles, Recreations in mathematics and natural philosophy .., (lire en ligne)
- Portail de la chimie
