Pyruvate synthase
Une pyruvate synthase, ou pyruvate:ferrédoxine oxydoréductase, est une oxydoréductase qui catalyse la réaction :
- CoA + pyruvate + 2 ferrédoxines oxydées acétyl-CoA + CO2 + 2 ferrédoxines réduites + 2 H+.
| N° EC | EC |
|---|---|
| N° CAS | |
| Cofacteur(s) | Fe-S ; TPP |
| IUBMB | Entrée IUBMB |
|---|---|
| IntEnz | Vue IntEnz |
| BRENDA | Entrée BRENDA |
| KEGG | Entrée KEGG |
| MetaCyc | Voie métabolique |
| PRIAM | Profil |
| PDB | RCSB PDB PDBe PDBj PDBsum |
| GO | AmiGO / EGO |
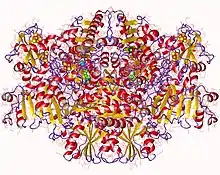
Cette enzyme est une protéine fer-soufre qui contient des clusters [4Fe-4S] et a pour cofacteur de la thiamine pyrophosphate. Elle intervient notamment dans les métabolismes du pyruvate, du propionate, du butyrate, et prolonge la voie de Wood-Ljungdahl vers la biosynthèse des trioses phosphate. Elle a une structure dimérique dont chaque monomère est formé d'une ou plusieurs chaînes polypeptidiques[1]. Chaque monomère contient six domaines liant une molécule de thiamine pyrophosphate et trois clusters [4Fe-4S][2].
L'amixicile, un inhibiteur enzymatique de la pyruvate synthase, pourrait présenter un intérêt pharmaceutique contre les infections à Helicobacter pylori et Clostridium difficile[3],[4].
Notes et références
- (en) Marcus I. Gibson, Percival Yang-Ting Chen et Catherine L. Drennan, « A structural phylogeny for understanding 2-oxoacid oxidoreductase function », Current Opinion in Structural Biology, vol. 41, , p. 54-61 (PMID 27315560, PMCID 5381805, DOI 10.1016/j.sbi.2016.05.011, lire en ligne)
- (en) Percival Yang-Ting Chen, Heather Aman, Mehmet Can, Stephen W. Ragsdale et Catherine L. Drennan, « Binding site for coenzyme A revealed in the structure of pyruvate:ferredoxin oxidoreductase from Moorella thermoacetica », Proceedings of the National Academy of Sciences of the United States of America, vol. 115, no 15, , p. 3846-3851 (PMID 29581263, PMCID 5899475, DOI 10.1073/pnas.1722329115, lire en ligne)
- (en) Cirle A. Warren, Edward van Opstal, T. Eric Ballard, Andrew Kennedy, Xia Wang, Mary Riggins, Igor Olekhnovich, Michelle Warthan, Glynis L. Kolling, Richard L. Guerrant, Timothy L. Macdonald et Paul S. Hoffman, « Amixicile, a Novel Inhibitor of Pyruvate:Ferredoxin Oxidoreductase, Shows Efficacy against Clostridium difficile in a Mouse Infection Model », Antimicrobial Agents and Chemotherapy, vol. 56, no 8, , p. 4103-4111 (PMID 22585229, PMCID 3421617, DOI 10.1128/AAC.00360-12, lire en ligne)
- (en) Paul S. Hoffman, Alexandra M. Bruce, Igor Olekhnovich, Cirle A. Warren, Stacey L. Burgess, Raquel Hontecillas, Monica Viladomiu, Josep Bassaganya-Riera, Richard L. Guerrant et Timothy L. Macdonald, « Preclinical Studies of Amixicile, a Systemic Therapeutic Developed for Treatment of Clostridium difficile Infections That Also Shows Efficacy against Helicobacter pylori », Antimicrobial Agents and Chemotherapy, vol. 58, no 8, , p. 4703-4712 (PMID 24890599, PMCID 4136022, DOI 10.1128/AAC.03112-14, lire en ligne)
- Portail de la biochimie