Graphyne
Le graphyne est un allotrope du carbone. Sa structure est similaire à celles du graphène ou du graphane, c'est-à-dire un monofeuillet d'atomes de carbone liés par liaisons sp2 d'un atome d'épaisseur. Il peut être vu comme un réseau de cycles benzéniques connectés entre eux par des ponts acétylène. En fonction du contenu des groupes acétylène, le graphyne peut être considéré comme une hybridation mixte spn, où 1 < n < 2[1],[2], et donc différer de celle du graphène (considérée comme une pure hybridation sp2) et de celle du diamant (pure sp3).
L'existence du graphyne a été conjecturée avant 1960[3] et fait l'objet d'attention particulière depuis la découvertes des fullerènes.
Même s'il n'a pour l'instant été synthétisé qu'en très petites quantités[réf. nécessaire], il a été montré que les structures périodiques du graphyne et de ses analogues nitrure de bore analogues devraient être stables, sur la base de calculs théoriques utilisant des courbes de dispersion de phonon (en) et température finies ab initio, et des simulations en dynamique moléculaire mécanique quantique[4].
Du graphdiyne (graphyne avec des groupes diacétylène) a déjà été synthétisé sur des substrats de cuivre[5]. En 2012, il a été promu comme un concurrent au graphène, du fait de ses cônes de Dirac dépendants de l'orientation[6],[7]. Le graphdiyne présente une structure de type nanotoile caractérisée par des pores triangulaires régulièrement distribués, ce qui lui donne l'apparence d'une membre nanoporeuse. De fait, la taille effective de ces pores correspond presque aux diamètre de Van der Walls de l'atome d'hélium, ce qui pourrait faire du graphdiyne une membrane bidimensionnelle idéale pour la séparation chimique et isotopique de l'hélium[8]. Des possibilités d'utilisation de membranes à base de graphdiyne comme tamis bidimensionnelle pour la filtration et la purification d'eau ont aussi été postulées[9].
Structure
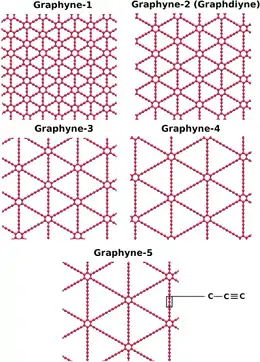
Le graphyne n'a pour l'instant pas été synthétisé en quantité suffisante pour être étudié, mais des modèles informatiques permettent de prédire certaines propriétés, sur la base de la géométrie de sa structure cristalline. Les géométries proposées sont des dérivés de celle du graphène, en remplaçant les liaisons carbone-carbone classiques par des liaisons acétylène[10]. Il a été théorisé que le graphyne puisse exister selon différentes géométries, du fait des arrangements multiples des carbones sp et sp2. Parmi elles, on trouve les géométries hexagonale et cubique[11], mais la plus prometteuse en termes d'applications est la structure rectangulaire du 6,6,12-graphyne.
Propriétés
Les modèles du graphyne qu'il possède potentiellement des cônes de Dirac sur les atomes de carbone liés doublement et triplement. Du fait de ce cônes de Dirac, il existe un point unique du niveau de Fermi où les bandes de conduction et de valence se rencontrent de façon linéaire. L'avantage de ce type configuration est que les électrons se comportent comme s'ils n'avaient pas de masse, avec des énergies proportionnelles au quantités de mouvement des électrons. Comme le graphène, le graphyne hexagonal a des propriétés électriques isotropes. Cependant, du fait de la symétrie de sa géométrie rectangulaire (théorique), le 6,6,12-graphyne aurait des propriétés qui dépendraient de la direction dans le plan du matériau[11]. Cette caractéristique unique de symétrie permet au graphyne d'être auto-dopé, c'est-à-dire d'avoir deux cône de Dirac différents, légèrement au-dessus et en dessous du niveau de Fermi[11]. Les échantillons synthétisés à ce jour présentent un point de fusion de 250 à 300 °C, et une faible réactivité vis-à-vis de l'oxygène, de la chaleur et de la lumière[10].
Applications futures
Les propriétés anisotropes du 6,6,12-graphyne pourraient le rendre utilisable comme réseau de diffraction électrique à l'échelle nanométrique[12]. Ceci pourrait mener au développement de transistors plus rapides, et de composés électriques nanométriques[11],[13],[14].
Notes et références
- R.B. Heimann, S.E. Evsvukov et Y. Koga, « Carbon allotropes: a suggested classification scheme based on valence orbital hybridization », Carbon, vol. 35, nos 10–11, , p. 1654–1658 (DOI 10.1016/S0008-6223(97)82794-7)
- Andrey N. Enyashin et Alexander L. Ivanovskii, « Graphene Allotropes », Physica Status Solidi (b), vol. 248, no 8, , p. 1879–1883 (DOI 10.1002/pssb.201046583)
- A.T. Balaban, C.C. Rentia et E. Ciupitu, Rev. Roum. Chim., , p. 231
- V. Ongun Özçelik et S. Ciraci, « Size Dependence in the Stabilities and Electronic Properties of α-Graphyne and Its Boron Nitride Analogue », The Journal of Physical Chemistry C, vol. 117, no 5, , p. 2175 (DOI 10.1021/jp3111869, lire en ligne)
- Guoxing Li, Yuliang Li, Huibiao Liu, Yanbing Guo, Yongjun Li et Daoben Zhu, « Architecture of graphdiyne nanoscale films », Chemical Communications, vol. 46, no 19, , p. 3256–3258 (DOI 10.1039/B922733D, lire en ligne)
- Daniel Malko, Christian Neiss, Francesc Viñes et Andreas Görling, « Competition for Graphene: Graphynes with Direction-Dependent Dirac Cones », Phys. Rev. Lett., vol. 108, no 8, , p. 086804 (DOI 10.1103/PhysRevLett.108.086804, Bibcode 2012PhRvL.108h6804M)
- Michael Schirber, « Focus: Graphyne May Be Better than Graphene », Physics, vol. 5, no 24, (DOI 10.1103/Physics.5.24, Bibcode 2012PhyOJ...5...24S, lire en ligne)
- Massimiliano Bartolomei, Estela Carmona Novillo, Marta I. Hernández, José Campos Martínez, Fernando Pirani et Giacomo Giorgi, « Graphdiyne Pores: "Ad Hoc" Openings for Helium Separation Applications », Journal of Physical Chemistry C, vol. 118, no 51, , p. 29966–29972 (DOI 10.1021/jp510124e, lire en ligne)
- Massimiliano Bartolomei, Estela Carmona Novillo, Marta I. Hernández, José Campos Martínez, Fernando Pirani, Giacomo Giorgi et Koichi Yamashita, « Penetration Barrier of Water through Graphynes’ Pores: First-Principles Predictions and Force Field Optimization », Journal of Physical Chemistry Letters, vol. 5, no 4, , p. 751–755 (DOI 10.1021/jz4026563, lire en ligne)
- Bog G. Kim et Hyoung Joon Choi, « Graphyne: Hexagonal network of carbon with versatile Dirac cones », Physical Review B, vol. 86, no 11, , p. 115435 (DOI 10.1103/PhysRevB.86.115435, Bibcode 2012PhRvB..86k5435K, arXiv 1112.2932)
- Belle Dumé, « Could graphynes be better than graphene? », Physics World, Institute of Physics, (lire en ligne)
- Debjyoti Bardhan, « Novel new material graphyne can be a serious competitor to graphene »,
- J. Cartwright, « Graphyne could be better than graphene »,
- « Graphyne Better Than Graphene? »,
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Graphyne » (voir la liste des auteurs).
Voir aussi
- Portail de la chimie
- Portail des micro et nanotechnologies
- Portail des sciences des matériaux