Photosynthèse
La photosynthèse (du grec φῶς phōs « lumière » et σύνθεσις sýnthesis « combinaison ») est le processus bioénergétique qui permet à des organismes (comme les bactéries photoautotrophes) de synthétiser de la matière organique en utilisant l'énergie lumineuse. Elle apparaît il y a plus de 3,7 milliards d'années chez des bactéries sulfato-réductrices[1].
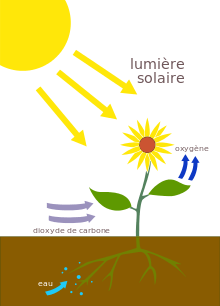

Elle désigne en particulier la photosynthèse oxygénique apparue chez les cyanobactéries il y a 2,45 milliards d’années, qui a produit un bouleversement écologique majeur en faisant évoluer l'atmosphère alors riche en méthane, en l'actuelle, composée essentiellement d'azote (78,08 %) et de dioxygène (20,95%)[2]. Cette aptitude a été ensuite transmise aux eucaryotes photosynthétiques (algues, plantes, etc.) par endosymbioses successives[3]. Des glucides, par exemple des oses tels que le glucose, sont synthétisés à partir du dioxyde de carbone CO2 et de l'eau H2O avec libération d'oxygène O2 comme sous-produit de l'oxydation de l'eau. C'est la photosynthèse oxygénique qui maintient constant le taux d'oxygène dans l'atmosphère terrestre et fournit toute la matière organique ainsi que l'essentiel de l'énergie utilisées par la vie sur Terre[4].
Tous les organismes photosynthétiques ne réalisent pas la photosynthèse de la même façon, mais ce processus commence toujours par l'absorption de l'énergie lumineuse par des protéines appelées centres réactionnels qui contiennent des pigments photosynthétiques appelés chlorophylles. Chez les plantes, ces protéines se trouvent dans la membrane des thylakoïdes, des structures incluses dans les chloroplastes, présents essentiellement dans les feuilles, tandis que chez les bactéries elles sont incluses dans la membrane plasmique. Au cours de ces réactions dépendantes de la lumière, une partie de l'énergie lumineuse sert à exciter des électrons d'une substance donneuse, le plus souvent de l'eau, électrons qui servent à leur tour à produire du nicotinamide adénine dinucléotide phosphate réduit (NADPH) ainsi que de l'adénosine triphosphate (ATP).
Chez les plantes, les algues et les cyanobactéries, les glucides sont produits par une série de réactions indépendantes de la lumière appelées cycle de Calvin, mais certaines bactéries utilisent d'autres voies métaboliques pour réaliser la fixation du carbone, comme le cycle de Krebs inverse. Dans le cycle de Calvin, le CO2 atmosphérique est fixé sur des composés organiques tels que le ribulose-1,5-bisphosphate. Les composés formés sont ensuite réduits et convertis par exemple en glucose à l'aide du NADPH et de l'ATP formés à la suite des réactions dépendantes de la lumière. La photosynthèse est ainsi la principale voie de transformation du carbone minéral en carbone organique. En tout, les organismes photosynthétiques assimilent chaque année entre 100 et 115 milliards de tonnes de carbone en biomasse[5],[6].
Les premiers organismes photosynthétiques sont probablement apparus très tôt au cours de l'évolution et devaient sans doute utiliser des réducteurs tels que l'hydrogène H2 et le sulfure d'hydrogène H2S au lieu de l'eau[7]. Les cyanobactéries sont apparues plus tard, et l'excès d'oxygène alors libéré dans l'environnement aurait contribué à la « Grande Oxydation » il y a environ 2,4 milliards d'années[8], rendant possible l'évolution des êtres vivants vers des formes de vie plus complexes. Aujourd'hui, la puissance moyenne captée par la photosynthèse à l'échelle du globe avoisine 130 térawatts[9],[10],[11], ce qui équivaut à environ six fois la consommation énergétique de l'humanité[12].
Vue générale
Principe
Les organismes photosynthétiques sont photoautotrophes, ce qui signifie qu'ils sont capables de synthétiser leurs biomolécules directement à partir de composés minéraux — le plus souvent le dioxyde de carbone CO2 et l'eau H2O — à l'aide de l'énergie lumineuse reçue du soleil. Cependant, tous les organismes capables d'utiliser l'énergie lumineuse pour leur métabolisme ne sont pas nécessairement photosynthétiques : les organismes dits photohétérotrophes synthétisent leurs biomolécules à partir de composés organiques, et non pas de CO2, comme sources de carbone[4].
Chez les plantes, les algues, les cyanobactéries et plusieurs taxons de bactéries (bactéries sulfureuses vertes, bactéries non sulfureuses vertes), la photosynthèse libère de l'oxygène O2. C'est ce qu'on appelle la photosynthèse oxygénique. Bien qu'il y ait des différences dans la biosynthèse réalisée par ces organismes, les mécanismes généraux restent tout à fait semblables d'une espèce à l'autre. Il existe cependant des bactéries qui possèdent une photosynthèse anoxygénique, laquelle consomme du CO2 mais ne libère pas d'O2.
Le dioxyde de carbone est converti en glucides à travers un processus appelé fixation du carbone. Il s'agit de réactions d'oxydoréduction endothermiques, de sorte que ce processus a besoin d'une part d'électrons pour réduire le CO2 en sucres et d'autre part d'énergie pour rendre ces réactions thermodynamiquement favorables. La photosynthèse est globalement la réciproque de la respiration cellulaire, au cours de laquelle des composés organiques tels que le glucose sont oxydés en dioxyde de carbone et en eau afin de libérer de l'énergie et de produire des coenzymes réductrices. Cependant, ces deux processus impliquent des réactions chimiques différentes réalisées dans des compartiments cellulaires différents.
La photosynthèse se déroule en deux phases : lors de la première, les réactions dépendantes de la lumière captent l'énergie lumineuse et l'utilisent pour produire une coenzyme réductrice, le NADPH, et une coenzyme qui stocke l'énergie chimique, l'ATP, tandis que, lors de la seconde phase, les réactions indépendantes de la lumière utilisent ces coenzymes pour absorber et réduire le dioxyde de carbone.
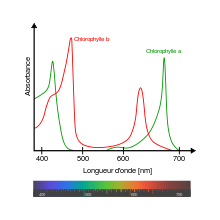
La plupart des organismes photosynthétiques oxygéniques utilisent la lumière visible, cependant ils ne sont actifs qu'à certaines longueurs d'onde (c'est-à-dire qu'ils absorbent ces longueurs d'onde par leurs pigments photosynthétiques) pour la chlorophylle a, le spectre d'action comprend les bleus et les rouges (longueurs d'onde autour 440 et de 680nm), d'autres pigments absorbant d'autres longueurs d'onde comme la chlorophylle b, les xanthophylles, ou encore les carotènoïdes, jouent un rôle dans la photosynthèse, aussi certains organismes photosynthétiques utilisent le proche infrarouge ou, plus particulièrement, le rouge lointain[14],[15] (autour de 800 nm de longueur d'onde).
On relèvera enfin que, si la photosynthèse est un processus biologique spécifique aux plantes, aux algues et à certains microorganismes (dont des protistes et des bactéries), il existe également un animal, la limace de mer Elysia chlorotica, connu pour être le siège d'un processus de photosynthèse se déroulant dans des chloroplastes qu'il ne produit pas lui-même mais qu'il absorbe avec les algues dont il se nourrit.
Donneurs d'électrons
L'équation globale de la photosynthèse peut s'écrire :
- 2n CO2 + 2n AH2 + photons → 2(CH2O)n + 2n AO, où A représente un donneur d'électrons.
Dans la photosynthèse oxygénique, l'eau est le donneur d'électrons, dont la dissociation libère de l'oxygène tandis que de l'eau est reformée à partir d'un atome d'oxygène du dioxyde de carbone :
- 2n CO2 + 4n H2O + photons → 2(CH2O)n + 2n O2 + 2n H2O.
On simplifie généralement l'équation en éliminant 2n H2O dans les deux termes, ce qui donne :
- 2n CO2 + 2n H2O + photons → 2(CH2O)n + 2n O2.
La photosynthèse anoxygénique utilise d'autres composés que l'eau comme donneur d'électrons. Ainsi, les bactéries pourpres sulfureuses utilisent le sulfure d'hydrogène H2S :
- 2n CO2 + 4n H2S + photons → 2(CH2O)n + 4n S + 2n H2O.
Les bactéries sulfureuses vertes sont par exemple capables d'utiliser le sulfure d'hydrogène H2S, le thiosulfate S2O32– et le soufre élémentaire S0 comme donneurs d'électrons, tandis que les bactéries vertes non sulfureuses peuvent utiliser l'hydrogène H2. Certains microorganismes sont capables d'utiliser l'arsénite AsO33– pour réduire le dioxyde de carbone CO2 en monoxyde de carbone CO avec formation d'arséniate AsO43–, ce qui peut être représenté par l'équation suivante[16],[17] :
- CO2 + (AsO33–) + photons → (AsO43–) + CO.
Parmi les donneurs d'électrons rencontrés chez les organismes photosynthétiques, on peut encore relever le fer ferreux Fe2+, les ions nitrite NO2–, voire des composés organiques tels que des acides et des alcools simples, par exemple l'acide acétique CH3COOH et l'éthanol CH3CH2OH.
Organites et membranes de la photosynthèse
Chloroplastes et thylakoïdes
Chez les bactéries photosynthétiques, les protéines qui absorbent la lumière pour la photosynthèse sont incluses dans des membranes cellulaires, ce qui représente l'arrangement le plus simple pour ces protéines[18]. Cette membrane peut cependant être repliée en feuillets cylindriques appelés thylakoïdes[19] ou en vésicules sphériques de membranes intracytoplasmiques[20]. Ces structures peuvent remplir la majeure partie de l'intérieur d'une cellule, offrant ainsi une très grande surface membranaire pour permettre à la bactérie d'absorber davantage de lumière[19].
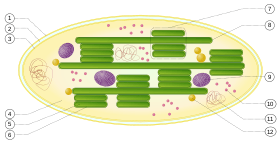
(1) membrane externe ;
(2) espace intermembranaire ;
(3) membrane interne ;
(4) stroma ;
(5) lumen du thylakoïde ;
(6) membrane du thylakoïde ;
(7) granum (empilement de thylakoïdes) ;
(8) thylakoïde ;
(9) amidon ;
(10) ribosome ;
(11) ADN chloroplastique ;
(12) plastoglobule (gouttelette lipidique).
Chez les plantes et les algues, la photosynthèse se déroule dans des organites appelés chloroplastes. Une cellule typique de plante contient environ dix à cent chloroplastes. Ces derniers sont enveloppés par une membrane interne et une membrane externe de nature phospholipidique et séparées par un espace intermembranaire. L'intérieur du chloroplaste est constitué d'un fluide aqueux appelé stroma. Dans le stroma se trouvent des thylakoïdes empilés en grana où siège la photosynthèse. Les thylakoïdes sont en forme de disques aplatis délimités par une membrane contenant l'espace thylakoïde ou lumen. La photosynthèse se déroule précisément dans la membrane des thylakoïdes, qui contient des complexes protéiques membranaires intégraux et périphériques ainsi que les pigments qui absorbent l'énergie lumineuse et constituent les photosystèmes.
Les plantes absorbent la lumière essentiellement grâce à des pigments appelés chlorophylles, ce qui explique leur couleur verte. Outre les chlorophylles, elles utilisent des carotènes et des xanthophylles[21]. Les algues utilisent également de la chlorophylle, mais avec divers autres pigments tels que la phycocyanine, les carotènes, et les xanthophylles chez les algues vertes, la phycoérythrine chez les algues rouges et la fucoxanthine chez les algues brunes et les diatomées, ce qui donne une grande variété de couleurs.
Ces pigments sont rassemblés chez les plantes et les algues dans des structures appelées antennes collectrices au sein desquelles les pigments sont organisés pour optimiser leur coopération.
Bien que toutes les cellules de plantes vertes possèdent des chloroplastes, l'énergie lumineuse est absorbée essentiellement par les feuilles, hormis chez certaines espèces adaptées à un ensoleillement fort et à une forte aridité, telles que les euphorbes et les cactus chez lesquelles le principal organe photosynthétique est la tige. Les cellules des tissus intérieurs d'une feuille — le mésophylle — peut contenir entre 450 000 et 800 000 chloroplastes par millimètre carré. La surface de la feuille est recouverte d'une cuticule cireuse et imperméable qui protège la feuille de l'excès d'évaporation d'eau et réduit l'absorption de la lumière bleue et ultraviolette afin de limiter l'échauffement de la plante. L'épiderme transparent permet à la lumière de le traverser pour mieux atteindre le mésophylle, où se déroule l'essentiel de la photosynthèse.
Pyrénoïdes
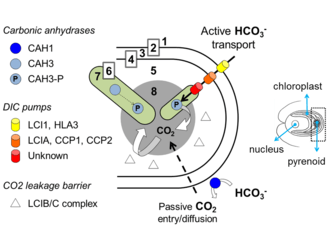
Les algues sont des organismes confinés aux environnement aqueux, même dans leurs biotopes terrestres. Il s'ensuit une difficulté pour elles à se procurer des quantités suffisantes de dioxyde de carbone afin de réaliser une photosynthèse efficace. En effet, le CO2 diffuse 10 000 fois plus lentement dans l'eau que dans l'air, et le CO2 dissous s'équilibre avec le bicarbonate HCO3–, ce qui en limite encore davantage les quantités disponibles pour la photosynthèse. Dans l'eau de mer, l'essentiel du CO2 dissous l'est sous forme de bicarbonate, ce qui permet aux molécules de Rubisco des algues marines de ne fonctionner qu'au quart de leur vitesse maximum.
De très nombreuses algues, ainsi que les plantes terrestre de l'embranchement des anthocérotes, disposent de sous-organites (microcompartiments) appelés pyrénoïdes présents dans leurs chloroplastes pour y concentrer le dioxyde de carbone autour de leur Rubisco[22]. Le contenu (matrice) de ces pyrénoïdes est essentiellement constitué de Rubisco[23] et est souvent traversé par des thylakoïdes qui se prolongent dans le stroma du chloroplaste.
Les pyrénoïdes sont souvent entourés d'une gaine d'amidon, synthétisé à l'extérieur du chloroplaste[24]. Chez Chlamydomonas, un complexe à haut poids moléculaire de deux protéines (LCIB/LCIC) forme une couche concentrique supplémentaire autour du pyrénoïde, à l'extérieur de la gaine d'amidon, dont on suppose actuellement qu'elle agit comme une barrière confinement du CO2 autour du pyrénoïde[25].
Les pyrénoïdes sont des structures très plastiques dont l'apparence est fortement corrélée à l'activité de concentration du dioxyde de carbone : chez Chlamydomonas en environnement riche en CO2, les pyrénoïdes sont petits et leur matrice manque de structure[26].
Carboxysomes

Les cyanobactéries possèdent des organites particuliers appelés carboxysomes qui concentrent le CO2 autour de la Rubisco afin d'en accroître le rendement. L'anhydrase carbonique présente dans ces carboxysomes libère le CO2 stocké dans le cytosol sous forme d'ions bicarbonate HCO3– concentrés dans la cellules de cyanobactérie par un transport actif à travers la membrane plasmique, qu'ils ne peuvent franchir dans l'autre sens en raison de leur charge électrique. Ces ions sont eux-mêmes formés à l'extérieur de la cellule à partir du CO2 dissous sous l'action d'autres anhydrases carboniques situées dans le milieu extracellulaire. Une fois dans le cytosol, les ions HCO3– ne libèrent que très lentement du CO2 sans l'action d'anhydrases carboniques, et diffusent donc vers les carboxysomes, où ils sont traités par des anhydrases carboniques avant d'être fixés par des molécules de Rubisco[27].
Réactions directement dépendantes de la lumière
La photosynthèse comprend deux ensembles de réactions distincts[28] :
- des réactions directement dépendantes de la lumière, dites « phase lumineuse » ou « phase claire », dont l'équation générale d'une photophosphorylation non cyclique chez les plantes vertes peut s'écrire[29] :
- des réactions non directement dépendantes de la lumière, dites « phase obscure », « phase sombre » ou « phase biochimique », dont l'équation générale chez les plantes vertes peut s'écrire :
Chez les plantes, les réactions directement dépendantes de la lumière se déroulent au sein des membranes des thylakoïdes à l'intérieur des chloroplastes et permettent la production d'ATP, la plupart du temps couplée à la production de NADPH par oxydation de l'eau.
Toutes les longueurs d'onde ne sont pas utilisées pour la photosynthèse. Le spectre d'action photosynthétique dépend des pigments accessoires : chez les plantes vertes par exemple, le spectre d'action provient des chlorophylles et des caroténoïdes, avec des pics d'absorption pour la lumière bleu-violet et rouge ; chez les algues, le spectre d'action se superpose au spectre d'absorption de phycobilines pour la lumière bleu-vert, ce qui permet à ces algues de se développer dans des eaux plus profondes, qui absorbent les longueurs d'onde plus grandes utilisées par les plantes vertes. Les longueurs d'onde qui ne sont pas absorbées sont celles qui donnent leur couleur aux organismes photosynthétiques : algues vertes, algues rouges, bactéries pourpres.
Les réactions directement dépendantes de la lumière peuvent être cycliques ou non cycliques.
Photophosphorylation non cyclique
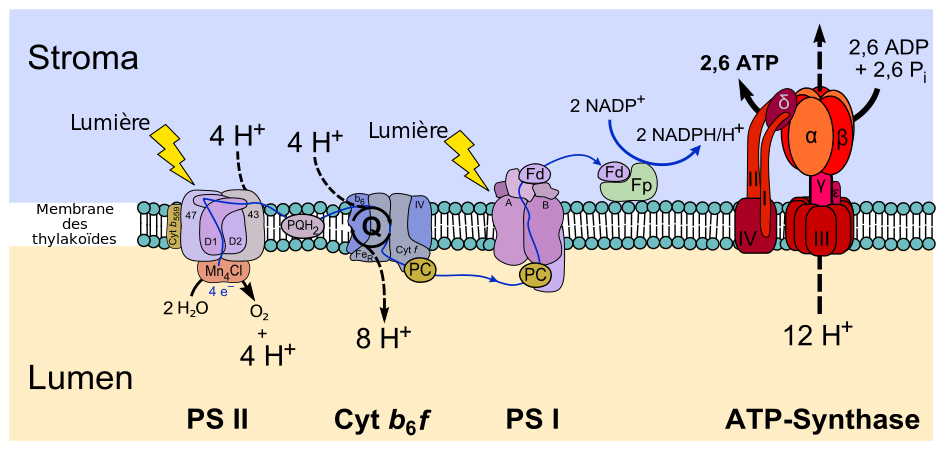
La photophosphorylation non cyclique consiste en un flux d'électrons depuis une molécule d'eau vers une molécule de NADP+ à travers une série d'enzymes membranaires et de protéines transporteuses avec génération d'un gradient de concentration en protons à travers la membrane des thylakoïdes au niveau du complexe cytochrome b6f. Ce gradient de concentration de protons génère un gradient électrochimique utilisé par l'ATP synthase pour réaliser la phosphorylation de l'ADP en ATP, ce qu'on appelle un couplage chimiosmotique. Ainsi, au cours de la photophosphorylation non cyclique, l'eau H2O est oxydée en oxygène O2 au niveau du photosystème II — plus précisément, du complexe d'oxydation de l'eau — et le NADP+ est réduit en NADPH par la ferrédoxine-NADP+ réductase.
Plus précisément, l'absorption d'un photon par une molécule de chlorophylle P680 du photosystème II conduit à l'excitation d'un électron, qui acquiert suffisamment d'énergie pour être cédé à un accepteur d'électrons par un phénomène de séparation de charges photoinduite. L'accepteur d'électrons primaire est une molécule de chlorophylle dépourvue d'atome de magnésium central appelée phéophytine. De là, l'électron excité passe sur une plastoquinone puis à travers le complexe cytochrome b6f avant d'être transporté sur une plastocyanine jusqu'à un photosystème I. Celui-ci contient un dimère de chlorophylle P700 capable d'exciter un électron par absorption d'un photon, électron transmis par la suite à une ferrédoxine, qui le cède à une ferrédoxine-NADP+ réductase pour réduire une molécule de NADP+ en NADPH.
Complexe d'oxydation de l'eau
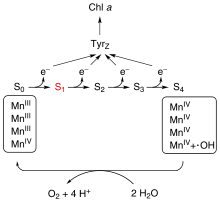
L'eau H2O est la source d'électrons de la photosynthèse chez les plantes et les cyanobactéries. Deux molécules d'eau sont oxydées par quatre réactions successives de séparation de charges dans le photosystème II pour donner une molécule de dioxygène O2, quatre protons H+ et quatre électrons e–. Chacun des quatre électrons transite par un résidu de tyrosine jusqu'au P680 qui sert de donneur d'électrons primaire du centre réactionnel du photosystème II.
L'oxydation de l'eau est catalysée par un cluster oxométallique comprenant quatre cations de manganèse et un cation de calcium. Cette structure, appelée complexe d'oxydation de l'eau (Oxygen-Evolving Complex), se lie à deux molécules d'eau et permet les quatre oxydations successives aboutissant à la libération d'une molécule d'O2 et de quatre H+, ces derniers contribuant à l'établissement du gradient électrochimique à travers la membrane des thylakoïdes. Le photosystème II est la seule enzyme connue capable d'oxyder l'eau de cette façon. L'oxygène libéré est en fait un déchet, utilisé cependant par la majorité des êtres vivants pour leur respiration cellulaire, y compris les organismes photosynthétiques[31].
Schéma en Z
Le « schéma en Z » représente les variations d'énergie des électrons au cours de la photophosphorylation non cyclique :
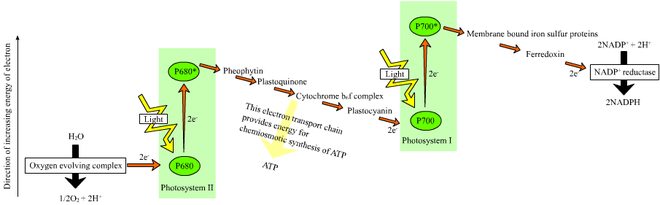
On peut le tracer précisément à partir des valeurs du potentiel d'oxydoréduction E°' des différents couples rédox[32] :
| Couple rédox | Potentiel d'oxydoréduction (V) |
|---|---|
| H2O / O2 | + 0,82 |
| P680 / P680+ | + 0,9 |
| P680* / P680 | - 0,8 |
| Phéophytine réduite / oxydée | - 0,6 |
| Plastoquinone réduite / oxydée | 0 |
| Complexe cytochrome b6f | - 0,2 et + 0,2 |
| P700 / P700+ | + 0,4 |
| P700* / P700 | -1,3 |
| Ferrédoxine réduite / oxydée | - 0,42 |
| NADPH / NADP+ | - 0,32 |
Photophosphorylation cyclique
La photophosphorylation cyclique ne fait intervenir que le photosystème I, le complexe cytochrome b6f et la plastocyanine ; le photosystème I absorbe l'énergie lumineuse, ce qui permet d'exciter un électron, transféré à un complexe cytochrome b6f auquel il cède son énergie en générant un gradient électrochimique utilisé par une ATP synthase pour produire de l'ATP, avant de revenir au photosystème I via une plastocyanine. Ces réactions ne produisent ni O2 ni NADPH.
Réactions non directement dépendantes de la lumière
Il existe diverses voies métaboliques de fixation du carbone. Celles des organismes photosynthétiques reposent dans presque tous les cas sur le cycle de Calvin, et son équation générale chez les plantes vertes peut s'écrire de la façon suivante :
Certains microorganismes peuvent utiliser à la place le cycle de Krebs inverse[33], tandis que d'autres possèdent des voies de fixation du carbone différentes telles que la voie de Wood-Ljungdahl ou encore le cycle du 3-hydroxypropionate et ses diverses variantes.
La fixation du carbone par le cycle de Calvin diffère selon les plantes en fonction du mécanisme de concentration du dioxyde de carbone autour de la Rubisco afin d'optimiser l'activité carboxylase de cette enzyme en limitant son activité oxygénase responsable de la photorespiration :
- la fixation du carbone en C3 consiste à fixer le CO2 directement par le cycle de Calvin ;
- la fixation du carbone en C4 fait intervenir des composés en C4 pour transporter le dioxyde de carbone, préalablement fixé par une enzyme ayant une plus forte affinité pour le CO2 que la Rubisco, vers les cellules où se trouve cette dernière ;
- le métabolisme acide crassulacéen (CAM) accumule le dioxyde de carbone pendant la nuit et le stocke sous forme de composés en C4 qui libèrent le CO2 dans la journée pour fixation du carbone à l'aide du NADPH et de l'ATP produits par les réactions directement dépendantes de la lumière.
Fixation du carbone en C3
-3-Phosphoglyceric_acid_(3PG)_Structural_Formula_V.1.svg.png)
à 3 atomes de carbone (en bleu).
Chez les plantes en C3, la fixation du carbone débute directement par le cycle de Calvin. On parle de « plantes en C3 » en référence au 3-phosphoglycérate, molécule à trois atomes de carbone formée par condensation du dioxyde de carbone CO2 sur du ribulose-1,5-bisphosphate par la Rubisco :
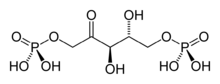
+ CO2 + H2O → 2 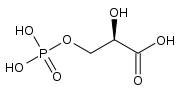
D-ribulose-1,5-bisphosphate 3-phospho-D-glycérate Ribulose-1,5-bisphosphate carboxylase/oxygénase (Rubisco) – EC
Le 3-phosphoglycérate formé est utilisé pour synthétiser essentiellement des glucides. Le 3-phosphoglycérate est réduit en glycéraldéhyde-3-phosphate à l'aide du NADPH et de l'ATP produits par les réactions directement dépendantes de la lumière.
Cinq molécules de glycéraldéhyde-3-phosphate sur six sont utilisées pour régénérer du ribulose-1,5-bisphosphate, tandis qu'une molécule de glycéraldéhyde-3-phosphate sur six est utilisée pour produire des hexoses phosphate, lesquels sont utilisés à leur tour pour produire du saccharose, de l'amidon et de la cellulose. La fixation du carbone par le cycle de Calvin produit ainsi des intermédiaires qui sont ensuite utilisés pour synthétiser des glucides ainsi que des précurseurs de lipides et d'acides aminés ; ils peuvent également être utilisés par la cellule comme composés énergétiques oxydés par respiration cellulaire.
Ces réactions ne dépendent de la lumière que de façon indirecte, car elles requièrent l'ATP et le NADPH produits par les réactions directement dépendantes de la lumière, de sorte qu'elles ne se déroulent que le jour bien qu'elles n'aient pas besoin de photons.
Les plantes en C3 tendent à se développer dans les environnement riches en eaux souterraines où le rayonnement solaire et la température sont modérés et la concentration de CO2 de l'ordre de 200 ppm ou plus[34]. Apparues au cours du Mésozoïque et du Paléozoïque, elles sont apparues avant les plantes en C4 et représentent aujourd'hui environ 95 % de la biomasse végétale. Elles perdent par transpiration 97 % de l'eau absorbée par leurs racines[35]. Le riz et l'orge, par exemple, sont des plantes en C3.
Les plantes en C3 ne peuvent pas pousser dans les zones trop chaudes parce que l'activité oxygénase de la Rubisco augmente avec la température par rapport à l'activité carboxylase, c'est-à-dire que la photorespiration devient prépondérante sur la fixation du carbone, ce qui conduit à une perte nette de carbone et d'azote par la plante. Dans les zones sèches, les plantes en C3 referment leurs stomates pour limiter leurs pertes en eau, mais cela a également pour effet de limiter l'entrée du dioxyde de carbone dans les feuilles et donc la concentration en CO2 dans ces dernières : cela réduit le ratio CO2/O2 et donc augmente la photorespiration.
Fixation du carbone en C4
Chez les plantes en C4, la fixation du carbone débute par la formation d'oxaloacétate, molécule comportant quatre atomes de carbone formée dès la première étape du processus par fixation du CO2 sur du phosphoénolpyruvate par la phosphoénolpyruvate carboxylase, une enzyme à l'activité carboxylase plus efficace que celle de la Rubisco :
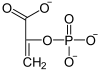
+ HCO3- → Pi + 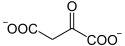
Phosphoénolpyruvate Oxaloacétate Phosphoénolpyruvate carboxylase – EC
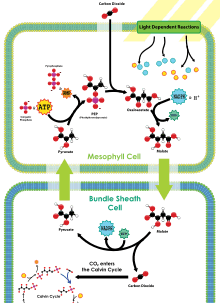
La fixation du CO2 sur le phosphoénolpyruvate se déroule au niveau des cellules du mésophylle (partie supérieure du schéma ci-contre), tissu situé entre les nervures des feuilles, et l'oxaloacétate formé y est converti en malate par la malate déshydrogénase à NADP+ ou en aspartate par l'aspartate aminotransférase. C'est sous cette forme que le CO2 fixé circule vers les cellules des gaines périvasculaires (partie inférieure du schéma ci-contre), où le CO2 est libéré pour être mis à disposition de la Rubisco et rejoindre le cycle de Calvin : dans ces cellules, la Rubisco est en effet isolée de l'oxygène atmosphérique et est donc saturée en dioxyde de carbone issu de la décarboxylation du malate ou de l'aspartate, ce qui l'oriente presque exclusivement vers son activité carboxylase ; la photorespiration est fortement réduite en augmentant la pression partielle de CO2 autour de la Rubisco, dont l'activité oxygénase est ainsi limitée.
Ce type de photosynthèse est notamment présent chez des graminées d'origine tropicale et aride, comme la canne à sucre, le maïs ou le sorgho. La fermeture de leurs stomates plus longtemps permet à ces plantes de limiter les pertes d'eau, mais présente l'inconvénient d'abaisser rapidement la pression partielle en CO2 dans la feuille ; la voie en C4 permet précisément de compenser ce phénomène et même de concentrer le CO2 là où la fixation du carbone a lieu, ce qui en optimise le rendement.
Les plantes en C4 représentent aujourd'hui environ 5 % de la biomasse végétale et 3 % des espèces de plantes connues[36],[37]. En dépit de leur relative rareté, elles sont cependant responsables d'environ 30 % de la fixation du carbone sur Terre[38].
De nombreuses espèces de différentes familles de plantes sont en C4. Opuntia ficus-indica est un exemple chez les Cactaceae. Le maïs est une plante en C4, qui consomme 400 litres d'eau par kilogramme de matière sèche produite (avec une température optimale de 30 °C), contre 1 500 litres pour le blé[39] ; pour autant, sa consommation à l'hectare est supérieure à celle du blé en raison d'un rendement plus élevé.
Métabolisme acide crassulacéen (CAM)
Le métabolisme acide crassulacéen (CAM, de l'anglais Crassulacean Acid Metabolism) est caractéristique des plantes qui poussent en environnement aride[40]. Il permet de limiter les pertes d'eau diurnes par transpiration en maintenant les stomates fermés pendant la journée et en ne les ouvrant que la nuit[41]. C'est donc la nuit que le dioxyde de carbone peut être absorbé par la plante et fixé sous forme d'acide organique à quatre atomes de carbone tels que le malate ou l'aspartate, comme pour les plantes en C4. Mais, à la différence de ces dernières, les composés en C4 ainsi formés la nuit sont stockés dans les vacuoles des cellules pour être utilisés par le cycle de Calvin dans la journée, alors que, chez les plantes en C4, ces composés formés dans les cellules du mésophylle pendant la journée migrent dans la foulée vers les cellules des gaines périvasculaires pour y être utilisés par le cycle de Calvin.
Le stockage nocturne des composés en C4 dans des vacuoles est rendu nécessaire par le fait que le cycle de Calvin ne peut fonctionner que le jour : il requiert en effet de l'énergie métabolique (ATP) et du pouvoir réducteur (NADPH), qui sont produits par les réactions directement dépendantes de la lumière.
Ce mécanisme existe également chez un certain nombre de plantes aquatiques[42]. Il répond cette fois à la limitation de la disponibilité en CO2 pendant la journée, par exemple du fait de la consommation de ce gaz dissous par les autres plantes.
Efficacité énergétique de la photosynthèse
L'efficacité énergétique de la conversion de l'énergie solaire en énergie biochimique par la photosynthèse chez les plantes avoisine généralement 3 à 6 %[43]. La lumière absorbée qui n'est pas convertie en énergie métabolique est essentiellement dissipée sous forme de chaleur, une petite fraction (1 à 2 %[44]) étant réémise par fluorescence de la chlorophylle à une plus grande longueur d'onde — donc, plus rouge que la lumière incidente.
L'efficacité énergétique des plantes varie en fonction de la longueur d'onde de la lumière incidente, de l'intensité lumineuse, de la température et de la pression partielle de dioxyde de carbone dans l'atmosphère, et peut varier de 0,1 à 8 %[45]. La décomposition typique des pertes d'énergie globales au cours du processus de photosynthèse par les plantes terrestres peut être résumée comme suit[46] :
- 47 % de l'énergie incidente ne peut être absorbée par la chlorophylle, dont le domaine actif couvre les longueurs d'onde comprises entre 400 et 700 nm, ce qui ne laisse que 53 % de l'énergie incidente ;
- 30 % de l'énergie reçue dans l'intervalle de longueurs d'onde de 400 à 700 nm n'atteint pas les centres réactionnels dans les chloroplastes, ce qui ne laisse que 37 % de l'énergie incidente ;
- 24 % de l'énergie reçue par les centres réactionnels est perdue par le fait que seule la fraction d'énergie correspondant à 700 nm de chaque photon est absorbée, le supplément d'énergie correspondant aux longueurs d'onde inférieures n'étant pas utilisé, ce qui ne laisse que 28,2 % de l'énergie incidente ;
- 68 % de l'énergie absorbée par les centres réactionnels est perdue au cours de la conversion en glucose, ce qui ne laisse que 9 % de l'énergie incidente ;
- 35 à 45 % du glucose ainsi produit est consommé par photorespiration, ce qui laisse moins de 5 à 6 % de l'énergie incidente.
Cas particuliers de photosynthèse
Animaux et photosynthèse
La limace de mer, Elysia chlorotica, est le premier animal découvert capable d'utiliser la photosynthèse pour produire de l'énergie. Cette photosynthèse est effectuée par les chloroplastes de sa principale source de nourriture, l'algue Vaucheria litorea. Ils sont séquestrés par l'épithélium digestif de la limace pendant plusieurs mois selon un phénomène de kleptoplastie, poursuivant leur fonctionnalité de réaliser la photosynthèse. Cependant, les chloroplastes de Vaucheria litorea ont transféré une grande partie de leurs gènes nécessaires à la photosynthèse vers le noyau des cellules de cette algue au cours de l'évolution[47]. La photosynthèse est néanmoins maintenue chez la limace de mer grâce au transfert d'un gène nécessaire à la photosynthèse depuis le noyau de l'algue vers le génotype de la limace[47].
De nombreux autres animaux peuvent établir une symbiose avec une algue : vers plats, coraux, anémones de mer, éponges, limaces de mer, etc. La salamandre maculée est toutefois le seul vertébré connu à ce jour (2011) qui établisse une symbiose avec une algue, en l'occurrence au sein de ses œufs avec Oophila amblystomatis[48],[49],[50].
Photosynthèse artificielle
La reproduction artificielle des réactions de photosynthèse fait l'objet de nombreuses recherches, qui se focalisent en général sur l'une ou l'autre des deux phases de la photosynthèse.
Ainsi, une équipe du National Renewable Energy Laboratory rapporte en 1998 avoir créé un dispositif permettant de dissocier l'oxygène et l'hydrogène de l'eau à partir d'énergie solaire[51]. Le dispositif est cependant instable et fabriqué à partir de matériaux rares. Une équipe du MIT indique en 2011 être parvenue à des résultats similaires, cette fois avec un dispositif stable et à partir de matériaux courants et bon marché[52].
Une équipe de l'université de Kyoto annonce quant à elle en 2007 un procédé capable de capter le CO2 atmosphérique 300 fois plus efficacement que les plantes[53],[54], à partir de dioxyde de manganèse.
En mars 2011, une équipe D. Nocera et al. du MIT dirigée par le Dr D. Nocera a annoncé avoir réussi à fabriquer une feuille artificielle, faite de matériaux durables et peu coûteux, permettant de décomposer l'eau en oxygène et hydrogène, à l'aide de la lumière du soleil afin de créer de l'électricité propre[55]. Les catalyseurs utilisés par Nocera, permettant d'accélérer le processus d’électrolyse de l'eau, ont été réalisés à partir de cobalt (ou de nickel [5]), et fonctionnent à pH 7, à température ambiante et sous pression atmosphérique[56].
Découverte et observation du mécanisme
- Dans l'Antiquité, Aristote pensait que le sol fournissait aux plantes les éléments dont elles ont besoin.
- Au XVIIe siècle, Jan Baptist van Helmont démontre qu'un saule planté en bac a pris 77 kg en 5 ans alors que le sol contenu dans le bac ne diminue que de 57 g ; il attribue la différence à l'action de l'eau.
- Au XVIIIe siècle, plusieurs scientifiques mettent en évidence les notions de respiration et de production d’oxygène par les plantes et l'importance de la lumière dans ce dernier phénomène. Ce sont d’abord deux chimistes anglais : Stephen Hales en 1727, qui pense que l'air et la lumière contribuent à la croissance des plantes, et Joseph Priestley entre 1771 et 1777 qui met en évidence le rejet d’oxygène. À leur suite, Jan Ingen-Housz, médecin et botaniste hollandais, établit en 1779 le rôle de la lumière dans la production d’oxygène par les plantes. Puis Jean Senebier, un pasteur suisse, à partir des travaux d’Antoine Lavoisier sur la composition de l'air, comprend que les plantes consomment du dioxyde de carbone et rejettent du dioxygène lors de cette phase.
- Au début du XIXe siècle, Nicolas Théodore de Saussure démontre la consommation d’eau lors de la photosynthèse. La chlorophylle est isolée par des chimistes français en 1817, Pierre Joseph Pelletier et Joseph Bienaimé Caventou.
- Au milieu du XIXe siècle les grandes lignes du mécanisme sont comprises, transformation de l'énergie lumineuse, consommation d’eau et de dioxyde de carbone, production d’amidon et rejet de dioxygène. L'expérience cruciale d’Engelmann (1882), où des bactéries servent d’indicateur de la production d’oxygène, montre clairement le rôle de la couleur de la lumière.
- C'est au cours du XXe siècle que l'explication plus détaillée du processus s’établit. Le début du siècle voit la description de la structure chimique de la chlorophylle puis la découverte de l'existence des types a et b. Robert Emerson établit en 1932[57] que 2 500 molécules de chlorophylle sont nécessaires pour émettre 1 molécule d'O2. Dans les années 1930, les travaux de Robert Hill permettent d'y voir plus clair. À l'issue de ses expériences, la photosynthèse se présente comme une réaction d'oxydo-réduction au cours de laquelle le carbone passe d'une forme oxydée à une forme réduite : CO2 → HCHO ; et l'oxygène d'une forme réduite à une forme oxydée : H2O → O2
- On a récemment découvert du nanoplancton qui vit à des profondeurs où il n'y a pratiquement plus de lumière. Certaines algues marines (cryptophytes, dont rhodomonas sp. et chroomonas sp.), à température ambiante et en condition d'illumination défavorable, sont capables, grâce à des « antennes » protéiques, et semble-t-il grâce à des protéines (bilines) utilisées en plus de la chlorophylle, de mieux capter la lumière et d'utiliser la cohérence quantique pour optimiser leur utilisation du rayonnement solaire incident. Cela leur permet de conduire plus de 95 % des photons jusqu'à leur « but »[58]. Ce phénomène pourrait exister chez d'autres végétaux, voire être courant.
- En 2010, des chercheurs du département de chimie de l'Université de Göteborg, en collaboration avec des équipes de l'École polytechnique Chalmers et d’autres universités européennes, ont observé grâce aux puissants rayons X de l'European Synchrotron Radiation Facility, les mouvements des atomes au sein de protéines engagées dans un processus de photosynthèse. L'expérience qui a fourni des informations en trois dimensions sur des mouvements de l’ordre de 1,3 angström de molécules, pourrait servir à créer des dispositifs faisant de la photosynthèse artificielle afin de produire l’énergie du futur à partir de la lumière du Soleil[59].
Production d'oxygène et captage d'énergie
_Pont-Avent_aout_2016_bulles_oxyg%C3%A8ne.jpg)
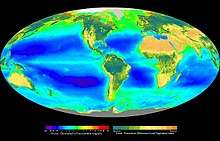
À l’échelle planétaire, ce sont les algues et le phytoplancton marin qui produisent le plus d’oxygène, suivi des forêts. On a longtemps cru que les mers froides et tempérées étaient les seules à avoir un bilan positif en termes d’oxygène, mais une étude de 2009[60] montre que les océans subtropicaux oligotrophes sont également producteurs d’oxygène, bien qu'ayant une production saisonnière irrégulière. Ces océans jouent donc un rôle en termes de puits de carbone. Pour le sud de l'hémisphère nord, la production d’oxygène est basse en début d’hiver, augmente jusqu’en août pour redescendre à l'automne[réf. à confirmer][61]. De même on a longtemps cru que l'oxygène n'était produit que dans les couches très superficielles de l’océan, alors qu'il existe également[58] du nanoplancton, vivant généralement à grande profondeur, photosynthétique. Dans les zones de dystrophisation ou dans les zones mortes de la mer, ce bilan peut être négatif.
Le flux d’énergie capté par la photosynthèse (à l’échelle planétaire) est immense, approximativement 100 térawatts[62] : qui est environ de 10 fois plus élevé que la consommation énergétique mondiale (intégrée sur un an)[Note 1]. Ce qui signifie qu'environ un peu moins du millième de l’insolation reçue par la Terre est captée par la photosynthèse et fournit pratiquement toute l’énergie de la biosphère.
Perturbation du processus de photosynthèse
Le processus de production d'oxygène peut être inhibé par des causes externes, avec par exemple une pollution particulaire importante (aérosols ou dépôts secs ou humides) qui peut interférer avec les rayons solaires (les bloquer éventuellement) ou nuire aux échanges feuille/atmosphère ; de même pour la turbidité de l'eau pour les plantes aquatiques.
Certains pesticides détruisent des mécanismes biochimiques, enzymatiques ou métaboliques élémentaires nécessaires à la photosynthèse, de même que certains phytopathogènes.
Notes
- Qui s’élève à environ 10 à 12 térawatts.
Références
- (en) Minik T Rosing, Robert Frei, « U-rich Archaean sea-floor sediments from Greenland indications of >3700 Ma oxygenic photosynthesis », Earth Planet. Sci. Lett., vol. 217, nos 3-4, , p. 237–244 (DOI 10.1016/S0012-821X(03)00609-5).
- « Air », sur olivier.fournet.free.fr (consulté le 21 août 2018)
- (en) Howard Gest, « History of the word photosynthesis and evolution of its definition », Photosynthesis Research, vol. 73, nos 1-3, , p. 7-10 (PMID 16245098, DOI 10.1023/A:1020419417954, lire en ligne)
« Photosynthesis is a series of processes in which electromagnetic energy is converted to chemical energy used for biosynthesis of organic cell materials; a photosynthetic organism is one in which a major fraction of the energy required for cellular syntheses is supplied by light »
— Gest 1993
- (en) Donald A. Bryant et Niels-Ulrik Frigaard, « Prokaryotic photosynthesis and phototrophy illuminated », Trends in Microbiology, vol. 14, no 11, , p. 488-496 (PMID 16997562, DOI 10.1016/j.tim.2006.09.001, lire en ligne)
- (en) Christopher B. Field, Michael J. Behrenfeld, James T. Randerson et Paul Falkowski, « Primary Production of the Biosphere: Integrating Terrestrial and Oceanic Components », Science, vol. 281, no 5374, , p. 237-240 (PMID 9657713, DOI 10.1126/science.281.5374.237, lire en ligne)
- McGraw-Hill Encyclopedia of Science & Technology, vol. 13, New York, McGraw-Hill, (ISBN 0-07-144143-3), « Photosynthesis ».
- (en) John M. Olson, « Photosynthesis in the Archean Era », Photosynthesis Research, vol. 88, no 2, , p. 109-117 (PMID 16453059, DOI 10.1007/s11120-006-9040-5, lire en ligne)
- (en) Roger Buick, « When did oxygenic photosynthesis evolve? », Philosophical Transactions of the Royal Society B, Biological Sciences, vol. 363, no 1504, , p. 2731-2743 (PMID 18468984, PMCID 2606769, DOI 10.1098/rstb.2008.0041, lire en ligne)
- (en) Kenneth H. Nealson et Pamela G. Conrad, « Life: past, present and future », Philosophical Transactions of the Royal Society B, Biological Sciences, vol. 354, no 1392, , p. 1923-1939 (PMID 10670014, PMCID 1692713, DOI 10.1098/rstb.1999.0532, lire en ligne)
- Whitmarsh J, Govindjee, Singhal GS (éditeur), Renger G (éditeur), Sopory SK (éditeur), Irrgang KD (éditeur) et Govindjee (éditeur), Concepts in photobiology: photosynthesis and photomorphogenesis, Boston, Kluwer Academic Publishers, (ISBN 0-7923-5519-9, lire en ligne), « The photosynthetic process », p. 11–51 :
« 100 x 1015 grams of carbon/year fixed by photosynthetic organisms which is equivalent to 4 x 1018 kJ/yr = 4 x 1021J/yr of free energy stored as reduced carbon; (4 x 1018 kJ/yr) / (31,556,900 sec/yr) = 1.27 x 1014 J/yr; (1.27 x 1014 J/yr) / (1012 J/sec / TW) = 127 TW. »
- Steger U, Achterberg W, Blok K, Bode H, Frenz W, Gather C, Hanekamp G, Imboden D, Jahnke M, Kost M, Kurz R, Nutzinger HG, Ziesemer T, Sustainable development and innovation in the energy sector, Berlin, Springer, (ISBN 3-540-23103-X, lire en ligne), p. 32 :
« The average global rate of photosynthesis is 130 TW (1 TW = 1 terawatt = 1012 watt). »
- (en) « World Consumption of Primary Energy by Energy Type and Selected Country Groups, 1980–2004 » [xls], Energy Information Administration, (consulté le 20 janvier 2007)
- (en) Purificación López-García & David Moreira, "Tracking microbial biodiversity through molecular and genomic ecology", Research in Microbiology, Vol.159, No.1, January-February 2008, p.67–73. DOI:10.1016/j.resmic.2007.11.019
- (en) « Scientists discover unique microbe in California's largest lake » (consulté le 20 juillet 2009)
- (en) Dennis J. Nürnberg, Jennifer Morton, Stefano Santabarbara, Alison Telfer, Pierre Joliot, Laura A. Antonaru, Alexander V. Ruban, Tanai Cardona, Elmars Krausz, Alain Boussac, Andrea Fantuzzi et A. William Rutherford, « Photochemistry beyond the red limit in chlorophyll f–containing photosystems », Science, American Association for the Advancement of Science (AAAS), vol. 360, no 6394, , p. 1210-1213 (ISSN 0036-8075, DOI 10.1126/science.aar8313, lire en ligne)
- (en) Anaerobic Photosynthesis, Chemical & Engineering News, 86, 33, 18 août 2008, p. 36
- (en) Kulp TR, Hoeft SE, Asao M, Madigan MT, Hollibaugh JT, Fisher JC, Stolz JF, Culbertson CW, Miller LG, Oremland RS, « Arsenic(III) fuels anoxygenic photosynthesis in hot spring biofilms from Mono Lake, California », Science, vol. 321, no 5891, , p. 967-70 (PMID 18703741, DOI 10.1126/science.1160799, Bibcode 2008Sci...321..967K, lire en ligne)
- (en) Christine L Tavano et Timothy J Donohue, « Development of the bacterial photosynthetic apparatus », Current Opinion in Microbiology, vol. 9, no 6, , p. 625-631 (PMID 17055774, PMCID 2765710, DOI 10.1016/j.mib.2006.10.005, lire en ligne)
- (en) Conrad W. Mullineaux, « The thylakoid membranes of cyanobacteria: structure, dynamics and function », Australian Journal of Plant Physiology, vol. 26, no 7, , p. 671-677 (DOI 10.1071/PP99027, lire en ligne)
- (en) Melih K. Şener, John D. Olsen, C. Neil Hunter et Klaus Schulten, « Atomic-level structural and functional model of a bacterial photosynthetic membrane vesicle », PNAS, vol. 104, no 40, , p. 15723-15728 (PMID 17895378, PMCID 2000399, DOI 10.1073/pnas.0706861104, Bibcode 2007PNAS..10415723S, lire en ligne)
- Campbell NA, Williamson B, Heyden RJ, Biology Exploring Life, Upper Saddle River, NJ, Pearson Prentice Hall, (ISBN 0-13-250882-6, lire en ligne).
- (en) Murray R. Badger, T. John Andrews, S. M. Whitney, Martha Ludwig, David C. Yellowlees, W. Leggat et G. Dean Price, « The diversity and coevolution of Rubisco, plastids, pyrenoids, and chloroplast-based CO2-concentrating mechanisms in algae », Revue canadienne de botanique, vol. 76, no 6, , p. 1052-1071 (DOI 10.1139/b98-074, lire en ligne)
- (en) Robert H. Holdsworth, « The isolation and partial characterization of the pyrenoid protein of Eremosphaera viridis », Journal of Cell Biology, vol. 51, no 2, , p. 499-513 (PMID 5112653, PMCID 2108136, DOI 10.1083/jcb.51.2.499, lire en ligne)
- (en) Sarah Wilson, John West, Jeremy Pickett-Heaps, Akiko Yokoyama et Yoshiaki Hara, « Chloroplast rotation and morphological plasticity of the unicellular alga Rhodosorus (Rhodophyta, Stylonematales) », Phycological Research, vol. 50, no 3, , p. 183-191 (DOI 10.1046/j.1440-1835.2002.00272.x, lire en ligne)
- (en) Takashi Yamano, Tomoki Tsujikawa, Kyoko Hatano, Shin-ichiro Ozawa, Yuichiro Takahashi et Hideya Fukuzawa, « Light and Low-CO2-Dependent LCIB–LCIC Complex Localization in the Chloroplast Supports the Carbon-Concentrating Mechanism in Chlamydomonas reinhardtii », Plant & Cell Physiology, vol. 51, no 9, , p. 1453-1468 (PMID 20660228, DOI 10.1093/pcp/pcq105, lire en ligne)
- (en) Mamta Rawat, Margaret C. Henk, Lara L. Lavigne et James V. Moroney, « Chlamydomonas reinhardtii mutants without ribulose-1,5-bisphosphate carboxylase-oxygenase lack a detectable pyrenoid », Planta, vol. 198, no 2, , p. 263-270 (DOI 10.1007/BF00206252, lire en ligne)
- (en) Murray R. Badger et G. Dean Price, « CO2 concentrating mechanisms in cyanobacteria: molecular components, their diversity and evolution », Journal of Experimental Botany, vol. 54, no 383, , p. 609-622 (PMID 12554704, DOI 10.1093/jxb/erg076, lire en ligne)
- (en) R. E. Blankenship, Molecular mechanisms of Photosynthesis, Blackwell Science Ltd, , 328 p..
- Raven PH, Evert RF, Eichhorn SE, Biology of Plants, New York, W.H. Freeman and Company Publishers, , 7e éd. (ISBN 0-7167-1007-2), p. 124–127.
- (en) Bessel Kok, Bliss Forbush et Marion McGloin, « Cooperation of charges in photosynthetic O2 evolution – I. A linear four step mechanism », Photochemistry and Photobiology, vol. 11, no 6, , p. 457-475 (PMID 5456273, DOI 10.1111/j.1751-1097.1970.tb06017.x, lire en ligne)
- (en) Yulia Pushkar, Junko Yano, Kenneth Sauer, Alain Boussac et Vittal K. Yachandra, « Structural changes in the Mn4Ca cluster and the mechanism of photosynthetic water splitting », PNAS, vol. 105, no 6, , p. 1879-1884 (PMID 18250316, PMCID 2542863, DOI 10.1073/pnas.0707092105, Bibcode 2008PNAS..105.1879P, lire en ligne)
- 12 - Le Schéma en Z, sur le site de l'UFR de biologie de l'université Pierre-et-Marie-Curie à Paris, France.
- (en) M. C. W. Evans, Bob B. Buchanan et Daniel I. Arnon, « A new ferredoxin-dependent carbon reduction cycle in a photosynthetic bacterium », PNAS, vol. 55, no 4, , p. 928-934 (PMID 5219700, PMCID 224252, DOI 10.1073/pnas.55.4.928, lire en ligne)
- C. Michael Hogan. 2011. "Respiration". Encyclopedia of Earth. Eds. Mark McGinley and C. J. Cleveland. National Council for Science and the Environment. Washington, D.C.
- (en) J. A. Raven et D. Edwards, « Roots: evolutionary origins and biogeochemical significance », Journal of Experimental Botany, vol. 52, no supplément 1, , p. 381-401 (PMID 11326045, DOI 10.1093/jexbot/52.suppl_1.381, lire en ligne)
- Rowan Sage et Russell Monson, C4 Plant Biology, (ISBN 0-12-614440-0, lire en ligne), p. 228–229.
- (en) W. J. Bond, F. I. Woodward et G. F. Midgley, « The global distribution of ecosystems in a world without fire », New Phytologist, vol. 165, no 2, , p. 525-538 (PMID 15720663, DOI 10.1111/j.1469-8137.2004.01252.x, lire en ligne)
- (en) Colin P Osborne et David J Beerling, « Nature's green revolution: the remarkable evolutionary rise of C4 plants », Philosophical Transactions of the Royal Society B, Biological Sciences, vol. 361, no 1465, , p. 173-194 (PMID 16553316, PMCID 1626541, DOI 10.1098/rstb.2005.1737, lire en ligne)
- http://www.snv.jussieu.fr/vie/dossiers/eau/eaugestion/eauagriculture.html L'eau et les activités agricoles
- (en) Ana Herrera, « Crassulacean acid metabolism and fitness under water deficit stress: if not for carbon gain, what is facultative CAM good for? », Annals of Botany, vol. 103, no 4, , p. 645-653 (DOI 10.1093/aob/mcn145, lire en ligne)
- (en) I. P. Ting, « Crassulacean Acid Metabolism », Annual Review of Plant Physiology, vol. 36, , p. 595-622 (DOI 10.1146/annurev.pp.36.060185.003115, lire en ligne)
- (en) Jon E. Keeley, « CAM photosynthesis in submerged aquatic plants », The Botanical Review, vol. 64, no 2, , p. 121-175 (DOI 10.1007/BF02856581, lire en ligne)
- (en) Kazuhisa Miyamoto, « Chapter 1 - Biological energy production », Renewable biological systems for alternative sustainable energy production (FAO Agricultural Services Bulletin - 128), FAO - Food and Agriculture Organization of the United Nations, (consulté le 2 février 2014)
- (en) Kate Maxwell et Giles N. Johnson, « Chlorophyll fluorescence—a practical guide », Journal of Experimental Botany, vol. 51, no 345, , p. 659-668 (DOI 10.1093/jexbot/51.345.659, lire en ligne)
- (en) Govindjee & Rajni Govindjee, « What is Photosynthesis? », université de l'Illinois à Urbana-Champaign.
- David Oakley Hall, K. K. Rao et Institute of Biology, Photosynthesis, Cambridge University Press, (ISBN 978-0-521-64497-6, lire en ligne).
- (en) Mary E. Rumpho, Jared M. Worful, Jungho Lee, Krishna Kannan, Mary S. Tyler, Debanish Bhattacharya, Ahmed Moustafa et James R. Manhart, « Horizontal gene transfer of the algal nuclear gene psbO to the photosynthetic sea slug Elysia chlorotica », PNAS, vol. 105, no 46, , p. 17867-17871 (DOI 10.1073/pnas.0804968105)
- (en) Anna Petherick, « A solar salamander – Photosynthetic algae have been found inside the cells of a vertebrate for the first time », Nature, (DOI 10.1038/news.2010.384, lire en ligne)
- (en) Anna Petherick, « Salamander's egg surprise – Algae enjoy symbiotic relationship with embryos », Nature, vol. 466, no 7307, , p. 675 (PMID 20686543, DOI 10.1038/466675a, lire en ligne)
- (en) Victor H. Hutchinson et Carl S. Hammen, « Oxygen Utilization in the Symbiosis of Embryos of the Salamander, Ambystoma maculatum and the Alga, Oophila amblystomatis », The Biological Bulletin, vol. 115, no 3, , p. 483-489 (DOI 10.2307/1539111, JSTOR 1539111, lire en ligne)
- (en) Oscar Khaselev et John A. Turner, « A Monolithic Photovoltaic-Photoelectrochemical Device for Hydrogen Production via Water Splitting », Science, vol. 280, , p. 425 (résumé)
- (en) « Debut of the first practical “artificial leaf” », sur American Chemical Society, .
- Barbara Ngouyombo, ambassade de France au Japon, « Bulletin électronique Japon 435 »
- « Photosynthèse artificielle pour réduire la pollution atmosphérique », sur techno-science.net
- (en) Samir Bensaid, Gabriele Centi, Edoardo Garrone, Siglinda Perathoner et Guido Saracco, « Towards Artificial Leaves for Solar Hydrogen and Fuels from Carbon Dioxide », ChemSusChem, vol. 5, no 3, , p. 500-521 (PMID 22431486, DOI 10.1002/cssc.201100661, lire en ligne)
- http://sciencetonnante.wordpress.com/2011/04/26/la-photosynthese-artificielle-de-l%E2%80%99energie-a-partir-de-soleil-et-d%E2%80%99eau/
- Gerald Karp, Biologie Cellulaire et Moléculaire, De Boeck Université, , 872 p. (ISBN 2-8041-4537-9, lire en ligne), p. 225
- (en) Elisabetta Collini, Cathy Y. Wong, Krystyna E. Wilk, Paul M. G. Curmi, Paul Brumer et Gregory D. Scholes, « Coherently wired light-harvesting in photosynthetic marine algae at ambient temperature », Nature, vol. 463, , p. 644-647 (DOI 10.1038/nature08811, résumé)
- futura-sciences.com du 12 mai 2010, A l'ESRF, on a photographié des atomes en pleine photosynthèse !
- (en) S. Riser et K. Johnson, « Net production of oxygen in the subtropical ocean », Nature, no 451, , p. 323-5 (DOI 10.1038/nature06441, lire en ligne) (étude conduite sur 3 ans).
- « Les océans subtropicaux aussi sont producteurs d’oxygène », Science et Avenir, , p. 19
- (en) Kenneth H. Nealson et Pamela G. Conrad, « Life: past, present and future », Philosophical Transactions of The Royal Society of London B Biological Sciences, vol. 354, no 1392, , p. 1923–39 (PMID 10670014, PMCID 1692713, DOI 10.1098/rstb.1999.0532, résumé)
Voir aussi
Articles connexes
- Chaînes alimentaires
- Phytoplancton
Liens externes
- [flash] (en) « la photosynthèse »
- « La Photosynthèse », sur le site de l'Université Pierre et Marie Curie - Très complet sur la photosynthèse.
Bibliographie
- Jack Farineau, Jean-François Morot-Gaudry (2018) La photosynthèse ; Processus physiques, moléculaires et physiologiques, Ed Quae, 460pp (ISBN 978-2-7592-2667-2)
- Portail de la biologie
- Portail de la botanique
- Portail de la chimie
_Formula_V.1.png)
_Structure_V.1.png)