Chimiosmose
En biochimie, la chimiosmose est le couplage de la phosphorylation de l'ADP en ATP par l'ATP synthase en utilisant l'énergie libérée par la dissipation d'un gradient de concentration de cations — généralement de protons H+ — à travers une membrane. Ce phénomène est à la base de la phosphorylation oxydative dans la respiration cellulaire et de la photophosphorylation dans la photosynthèse.

L'ATP synthase est l'enzyme qui, dans les systèmes biologiques, fonctionne par chimiosmose. C'est une protéine membranaire intégrale présente chez tous les eucaryotes dans la membrane mitochondriale interne et, chez les plantes, dans la membrane des thylakoïdes, ainsi que chez la plupart des procaryotes (bactéries et archées).
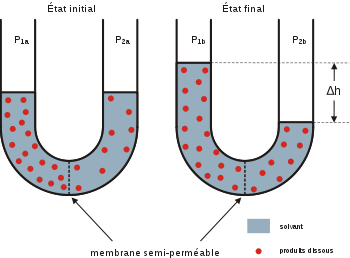
La découverte de la chimiosmose est due au biochimiste britannique Peter Mitchell qui reçut pour cela le prix Nobel de chimie en 1978[1]. C'est lui qui forgea le terme « chimiosmose » pour souligner l'analogie avec l'effet d'un gradient de concentration d'un soluté autour d'une membrane semiperméable, appelé osmose.
Théorie chimiosmotique
Histoire
C'est en 1961 que le biochimiste britannique Peter Mitchell a publié sa théorie chimiosmotique[2]. Cette théorie suggère essentiellement que l'ATP des cellules est formé au cours de la respiration cellulaire à partir du gradient électrochimique généré à travers la membrane mitochondriale interne en utilisant l'énergie du NADH et du FADH2 issus de la dégradation de molécules riches en énergie telles que les glucides et les acides gras.

Cette théorie introduisit une rupture radicale avec les conceptions en vigueur jusqu'au début des années 1960, qui supposaient que l'énergie libérée par les transferts d'électrons était emmagasinée par un intermédiaire stable susceptible de la libérer pour phosphoryler l'ADP en ATP, de sorte que les travaux de Mitchell furent accueillis sans grand enthousiasme par ses pairs. Il ne fut cependant jamais possible d'identifier de composé riche en énergie susceptible de coupler le transfert des électrons à haut potentiel par la chaîne respiratoire avec la formation d'ATP à partir d'ADP, tandis qu'il y eut de plus en plus d'observations expérimentales mettant en évidence le pompage de protons par les complexes enzymatiques de la chaîne respiratoire, de sorte que le consensus finit par basculer en faveur de la théorie chimiosmotique.
Principe
La dégradation de ces molécules — par exemple par glycolyse dans le cas du glucose ou par β-oxydation dans le cas des acides gras — conduit généralement à la formation d'acétyl-CoA, qui est oxydé dans la matrice mitochondriale des eucaryotes par le cycle de Krebs. Ce dernier produit des coenzymes réduites[3] — NADH et FADH2 — possédant des électrons à haut potentiel de transfert. Ces électrons sont cédés à la chaîne respiratoire, constituée chez les eucaryotes de principalement quatre complexes enzymatiques intervenant séquentiellement pour transférer ces électrons de proche en proche jusqu'à la réduction finale d'une molécule d'oxygène O2 en deux molécules d'eau H2O. Trois de ces quatre complexes enzymatiques sont des pompes à protons qui injectent des protons H+ dans l'espace intermembranaire mitochondrial depuis la matrice mitochondriale à travers la membrane mitochondriale interne. Il se forme un gradient de concentration de protons à travers cette membrane, à l'origine d'un gradient électrochimique qui accumule l'énergie potentielle libérée par les réactions d'oxydoréduction successives de la chaîne respiratoire. Le reflux des protons depuis l'espace intermembranaire vers la matrice mitochondriale à travers l'ATP synthase sous l'effet de ce gradient électrochimique a pour effet d'entraîner un rotor moléculaire qui fournit à l'enzyme l'énergie nécessaire pour phosphoryler l'ADP en ATP.
Définitions
Gradient électrochimique
Le mouvement des espèces chimiques à travers une membrane qui leur est perméable résulte de la combinaison de deux phénomènes :
- un gradient de concentration à travers cette membrane tend à faire diffuser les substances du compartiment où leur concentration est la plus élevée vers le compartiment où leur concentration est la plus faible afin d'équilibrer leur concentration dans les deux compartiments ;
- dans le cas des espèces électriquement chargées (ions), une différence de potentiel entre les deux compartiments délimités par la membrane tend à faire diffuser les cations — comme les protons H+ — vers le compartiment où prédominent les espèces chargées négativement et les anions vers le compartiment où prédominent les espèces chargées positivement afin d'équilibrer la charge électrique des deux compartiments.
La résultante de ces gradients de concentration et de potentiel électrique constitue le gradient électrochimique. La part respective des deux composantes du gradient électrochimique varie selon les processus biochimiques considérés : le gradient de concentration de protons contribue à l'essentiel du gradient électrochimique dans les chloroplastes pour la photosynthèse car la charge électrique des protons H+ y est équilibrée notamment par les ions chlorure Cl–, tandis que c'est la différence de potentiel qui contribue à l'essentiel du gradient électrochimique dans les mitochondries pour la respiration cellulaire en raison de la séparation des charges électriques induite par l'injection de protons dans l'espace intermembranaire mitochondrial sans transport concomitant d'anions vers la matrice mitochondriale.
Les bicouches lipidiques composant les membranes biologiques sont imperméables aux ions. C'est ce qui permet d'emmagasiner de l'énergie en combinant ces deux gradients à travers une telle membrane. Seules des protéines membranaires particulières appelées canaux ioniques permettent le transport membranaire contrôlé de certains ions.
Force proton motrice
Par analogie avec la force électromotrice des générateurs électriques, on appelle force proton-motrice d'une chaîne de transport d'électrons — comme la chaîne respiratoire — le gradient électrochimique susceptible d'être généré à travers une membrane par les pompes à protons de cette chaîne lorsque les électrons à haut potentiel de transfert y circulent depuis les donneurs d'électrons jusqu'à l'accepteur final d'électrons. Dans le cadre de la théorie chimiosmotique, la génération d'un tel gradient électrochimique permet d'emmagasiner la variation d'enthalpie libre au cours des réactions d'oxydoréduction de la chaîne de transport d'électrons sous une forme utilisable par l'ATP synthase pour produire de l'ATP à partir d'ADP ; une force proton-motrice d'environ 50 kJ·mol-1 est nécessaire pour permettre à l'ATP synthase de phosphoryler l'ADP en ATP.
Dans les mitochondries, l'énergie libérée par la chaîne respiratoire est convertie en gradient électrochimique entre l'espace intermembranaire mitochondrial et la matrice mitochondriale à travers la membrane mitochondriale interne. Plus précisément, les trois pompes à protons de la chaîne respiratoire — la NADH déshydrogénase (complexe I), la coenzyme Q-cytochrome c réductase (complexe III) et la cytochrome c oxydase (complexe IV) — injectent des protons H+ dans l'espace intermembranaire, ce qui génère un gradient de potentiel d'environ –0,17 V par rapport à la matrice.
Chimiosmose dans les systèmes biologiques
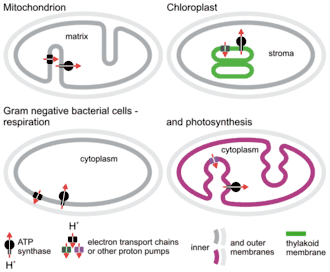
La chimiosmose se rencontre essentiellement dans deux types de processus générateurs d'ATP : la respiration cellulaire et la photosynthèse. Plus précisément, elle permet de coupler thermodynamiquement une chaîne de transport d'électrons avec une ATP synthase : la première « libère » de l'énergie sous forme d'une variation d'enthalpie libre négative (réaction exergonique) au fur et à mesure que des électrons à haut potentiel de transfert circulent d'un réducteur donneur d'électrons vers un oxydant accepteur d'électrons, tandis que la seconde « consomme » de l'énergie sous forme d'une variation d'enthalpie libre positive (réaction endergonique) lors de la phosphorylation de l'ADP en ATP.
Chez les eucaryotes
Chez les eucaryotes, la respiration cellulaire commence dans le cytosol par la dégradation des biomolécules de la cellule et se termine dans les mitochondries par le cycle de Krebs et la phosphorylation oxydative. Le cycle de Krebs se déroule dans la matrice mitochondriale et dégrade l'acétyl-CoA en dioxyde de carbone CO2 et coenzymes réduites NADH et FADH2. Ces coenzymes réduites sont oxydées par la chaîne respiratoire dans la membrane mitochondriale interne pour redonner du NAD+ et du FAD par réduction de molécules d'oxygène O2 en molécules d'eau H2O. L'énergie libérée par ces réactions d'oxydoréduction est convertie en gradient électrochimique à travers la membrane mitochondriale interne afin de permettre à l'ATP synthase de phosphoryler l'ADP en ATP.
La photosynthèse, quant à elle, commence dans les chloroplastes par la photophosphorylation et le cycle de Calvin. La photophosphorylation se déroule dans la membrane des thylakoïdes et fait intervenir une chaîne de transport d'électrons absorbant l'énergie lumineuse pour oxyder des molécules d'eau H2O en molécules d'oxygène O2 et réduire des coenzymes NADP+ en NADPH. Cette chaîne de transport d'électrons génère également un potentiel électrochimique à travers la membrane des thylakoïdes qui permet à l'ATP synthase de phosphoryler l'ADP en ATP. La photosynthèse se poursuit alors dans le stroma des chloroplastes avec les réactions de fixation du carbone par le cycle de Calvin permettant d'absorber une molécule de dioxyde de carbone CO2 sur du ribulose-1,5-bisphosphate pour former deux molécules de 3-phosphoglycérate, à partir desquelles sont synthétisés des oses à trois, quatre, cinq ou six atomes de carbone, voire davantage, ainsi que diverses autres molécules biologiques, selon un métabolisme qui se poursuit dans le cytosol de la cellule.
Chez les procaryotes
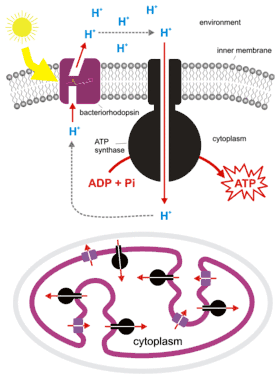
Les bactéries et les archées ont également recours à la chimiosmose pour produire leur ATP.
C'est par exemple le cas d’Escherichia coli[4], dont la membrane plasmique est le siège d'une chaîne respiratoire couplée à la phosphorylation de l'ADP en ATP par l'ATP synthase au moyen d'un gradient électrochimique, de manière analogue à la phosphorylation oxydative dans les mitochondries.
C'est également le cas de bactéries photosynthétiques telles que les cyanobactéries, les bactéries vertes sulfureuses et les bactéries pourpres sulfureuses, dont l'anabolisme repose sur la photophosphorylation : elles captent l'énergie lumineuse au moyen de centres réactionnels dans des photosystèmes de complexité variable selon les espèces, ce qui alimente des chaînes de transport d'électrons plus ou moins longues pour produire des coenzymes réduites telles que le NADPH ainsi qu'un gradient électrochimique susceptible d'actionner une ATP synthase par chimiosmose pour produire de l'ATP. Les bactéries pourpres et les bactéries vertes sulfureuses utilisent chacune un photosystème à base de bactériochlorophylle couplé à une pompe à protons au moyen d'une courte chaîne de transport d'électrons pour réaliser une photosynthèse anoxygénique (en), tandis que les cyanobactéries possèdent deux photosystèmes fonctionnant séquentiellement de manière analogue à ceux des plantes et libérant de l'oxygène O2.
Une archée telle que Halobacterium salinarum met en œuvre une chimiosmose de manière encore plus simple : son photorécepteur est une bactériorhodopsine qui fonctionne elle-même comme une pompe à protons, sans qu'il y ait besoin de faire intervenir une chaîne de transport d'électrons entre complexes enzymatiques distincts ; une ATP synthase intervient parallèlement à cette bactériorhodopsine pour produire de l'ATP en dissipant le gradient électrochimique généré à travers la membrane pourpre de cette halobactérie.
Théorie endosymbiotique
Le fait que la chimiosmose, sur laquelle repose le métabolisme énergétique de tous les êtres vivants, soit mise en œuvre chez les eucaryotes dans des organites qui présentent en eux-mêmes d'étroites analogies avec certains procaryotes, est une indication forte que ces organites et ces procaryotes puissent avoir une origine commune. Il est ainsi communément admis que les mitochondries et les plastes — notamment les chloroplastes — dérivent respectivement d'α-protéobactéries[5] et de cyanobactéries filamenteuses fixant l'azote[6],[7], qui auraient évolué par endosymbiose jusqu'à devenir les organites que nous connaissons aujourd'hui.
Notes et références
- (en) « The Nobel Prize in Chemistry 1978 : Peter D. Mitchell » (consulté le 2 janvier 2016) : « for his contribution to the understanding of biological energy transfer through the formulation of the chemiosmotic theory ».
- (en) Peter Mitchell, « Coupling of Phosphorylation to Electron and Hydrogen Transfer by a Chemi-Osmotic type of Mechanism », Nature, vol. 191, no 4784, , p. 144-148 (PMID 13771349, DOI 10.1038/191144a0, Bibcode 1961Natur.191..144M, lire en ligne)
- (en) Bruce Alberts, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts et Peter Walter, Molecular Biology of the Cell, New York (États-Unis), Garland Sciences, , 4e éd., 1616 p. (ISBN 0-8153-4072-9, lire en ligne)
- (en) Etana Padan, Dan Zilberstein et Hagai Rottenberg, « The proton electrochemical gradient in Escherichia coli cells », European Journal of Biochemistry, vol. 63, no 2, , p. 533-541 (PMID 4325, DOI 10.1111/j.1432-1033.1976.tb10257.x, lire en ligne)
- (en) J. Cameron Thrash, Alex Boyd, Megan J. Huggett, Jana Grote, Paul Carini, Ryan J. Yoder, Barbara Robbertse, Joseph W. Spatafora, Michael S. Rappé et Stephen J. Giovannoni, « Phylogenomic evidence for a common ancestor of mitochondria and the SAR11 clade », Scientific Reports, vol. 1, , p. 13 (PMID 22355532, PMCID 3216501, DOI 10.1038/srep00013, Bibcode 2011NatSR...1E..13T, lire en ligne)
- (en) Oliver Deusch, Giddy Landan, Mayo Roettger, Nicole Gruenheit, Klaus V. Kowallik, John F. Allen, William Martin et Tal Dagan, « Genes of Cyanobacterial Origin in Plant Nuclear Genomes Point to a Heterocyst-Forming Plastid Ancestor », Molecular Biology and Evolution, vol. 25, no 4, , p. 748-761 (PMID 18222943, DOI 10.1093/molbev/msn022, lire en ligne)
- (en) Jesús A. G. Ochoa de Alda, Rocío Esteban, María Luz Diago et Jean Houmard, « The plastid ancestor originated among one of the major cyanobacterial lineages », Nature Communications, vol. 5, , p. 4937 (PMID 25222494, DOI 10.1038/ncomms5937, Bibcode 2014NatCo...5E4937O, lire en ligne)
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Chemiosmosis » (voir la liste des auteurs).
Voir aussi
Articles connexes
Bibliographie
- (en) biochemistry textbook reference, from the NCBI bookshelf- Biochemistry (5th edition), Jeremy M. Berg, John L. Tymoczko, Lubert Stryer (lire en ligne), chap. 18.4 (« A Proton Gradient Powers the Synthesis of ATP »)
- (en) technical reference relating one set of experiments aiming to test some tenets of the chemiosmotic theory- Seiji Ogawa et Tso Ming Lee, « The Relation between the Internal Phosphorylation Potential and the Proton Motive Force in Mitochondria during ATP Synthesis and Hydrolysis », Journal of Biological Chemistry, vol. 259, no 16, , p. 10004-10011 (PMID 6469951)
Liens externes
- Portail de la biochimie
- Portail de la biologie cellulaire et moléculaire