Hémangiome
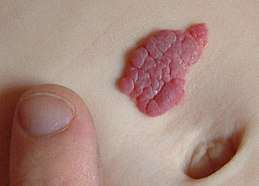
Un hémangiome (parfois appelé hémangiome infantile) est une tumeur bénigne (non cancéreuse) des cellules qui tapissent les vaisseaux sanguins (autrefois nommée « fraise »). C'est une des formes d'angiomes. Lorsqu’il y a hémangiome, ces cellules, appelées cellules endothéliales des vaisseaux se multiplient à un rythme anormalement rapide en formant une masse (« cutanée tubéreuse », « sous-cutanée »… ou « mixte » dans 75 % des cas), associée à une coloration rouge due à la présence importante de sang dans le tissu.
| Spécialité | Oncologie |
|---|
| CISP-2 | S81 |
|---|---|
| CIM-10 | D18.0 |
| ICD-O | 9120/0 |
| DiseasesDB | 30033 |
| MedlinePlus | 001459 |
| eMedicine | 1083849 |
| MeSH | D006391 |
![]()
Épidémiologie
Les hémangiomes constituent en Occident dans la population blanche la tumeur bénigne la plus répandue chez les nouveau-nés et nourrissons (4 à 8 % des nourrissons ont au moins un hémangiome[1]).
Les filles sont plus touchées ainsi que les prématurés ou les enfants issus de grossesse multiple. Le risque est également plus élevé si la mère est plus âgée, en cas de placenta praevia ou de pré-éclampsie[2].
Localisation
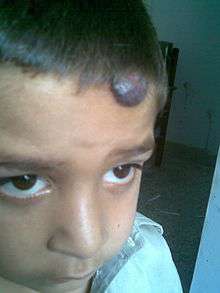
Il concerne la tête et cou (pour 60 % des hémangiomes), le tronc (25 %) et les bras et jambes (15 %).
Environ 80 % sont uniques sur le corps, 20 % apparaissent à des endroits différents sur un même enfant. Ils sont souvent externes, mais peuvent aussi toucher un organe interne (foie, poumons, tube digestif, cerveau…). L’hémangiome interne est plus fréquent quand au moins 4 hémangiomes externes existent.
Causes
Elles sont inconnues. L'origine génétique semble exclue. Les gens à la peau claire ont plus de risque. On ne connaît pas d’aliments ou de médicaments ingérés lors de la grossesse, ni des activités qui seraient facteur de risque (autres que les risques liés à la prématurité).
On peut néanmoins citer des facteurs de risque, tels que la prématurité, le sexe féminin, les prélèvements trophoblastiques (pour un diagnostic prénatal) ou encore l'existence d'une éclampsie chez la mère.
Types
- Hémangiome capillaire : les hémangiomes capillaires (sont également considérés comme des dysplasies tissulaires lors du développement). Ils sont composés de la juxtaposition de nombreux capillaires ayant ou non une lumière centrale où se trouvent des hématies. Ils siègent principalement sur la peau et les muqueuses.
- Hémangiome plan (« tache de vin »)
- Hémangiome nodulaire dermohypodermique
- Hémangiome caverneux (ou « cavernome »), forme de larges cavités kystiques juxtaposées remplies de sang.
- hémangiome facial (ou Dandy Walker)
- Hémangio-endothéliome kaposiforme
- Hémangiome caverneux de la rétine
- Hémangiome hépatique
- PHACE : Il existe une corrélation entre l'importance des hémangiomes de la face et un risque accru de syndrome PHACE[3], avec des anomalies de la fosse postérieure du cerveau, des artères, du cœur, des yeux, chez les nourrissons affectés de grands hémangiomes faciaux. Les manifestations extracutanées et syndromes PHACE (31 % des cas) sont fréquemment associées à une morbidité importante et à des risques accrus, et ce d'autant plus que l'hémangiome du visage était important. 91 % des nourrissons présentaient aussi des anomalies des artères du cerveau et 67 % présentaient des anomalies cardiaques. Les hémangiomes du haut du visage (fronto-temporal ou fronto-nasal) sont plus souvent associés à un syndrome PHACE alors que les hémangiomes maxillaires le sont rarement[3].
Il existe de rares hémangiomes congénitaux, constitués dès la naissance.
S'ils sont multiples et diffus, on parle d'hémangiomatose
Complications
Les hémangiomes peuvent être blessés ou évoluer en ulcères (avec saignements, infection, dans 5 à 10 % des cas et souvent à proximité de la bouche, de la région génitale ou anale). Certaines localisations peuvent obstruer des fonctions vitales telles que la vision, l’ouïe, l’alimentation, la digestion, l’excrétion ou la respiration; ou déformer les traits du visage. Dans 1 % des cas, les complications sont graves et peuvent conduire à la mort par hémorragie interne, insuffisance cardiaque ou dysfonction d’un organe interne.
Évolution
Une phase de croissance dure six à douze mois, voire jusqu’à dix-huit mois, suivie d’une phase d’involution (régression), plus lente (un à sept ans) à la fin de laquelle on ne constate jamais de récidive.
Des veines sont souvent visibles sous la peau autour de la tumeur. La couleur de l’angiome s’atténue naturellement (vers le brun ou bleu-grisâtre) au cours de l’involution, où sa surface diminue.
D’ordinaire, la couleur a disparu vers 7 ans. Des vaisseaux avec une configuration inhabituelle peuvent rester visibles un certain temps.
La régression n’est complète que chez 50 % des enfants âgés de 5 ans, et chez 70 % des enfants de 7 ans[4]. À 10-12 ans, l’involution est terminée. Seul un traitement chirurgical peut alors intervenir. Quand l’involution a été totale, des résidus de tissus graisseux peuvent néanmoins parfois subsister, ainsi qu’une peau plus fine et/ou fripée à cet endroit.
Traitement
La plupart des hémangiomes ne posent qu'un problème esthétiques et sont résolutifs, ne nécessitant aucune prise en charge médicale. Seuls, 10 à 15 % des cas nécessitent un traitement[5].
Le propranolol, un bêtabloquant, donné en phase de croissance de l'hémangiome permet d'en ralentir l'expansion et de favoriser sa régression[6],[7].
L'efficacité du laser reste discutée et semble peut-être meilleure pour les lésions superficielles[8].
Notes et références
- Kilcline C, Frieden IJ, Infantile hemangiomas: how common are they? A systematic review of the medical literature, Pediatr Dermatol, 2008;25:168-73
- Haggstrom AN, Drolet BA, Baselga E et al. Prospective study of infantile hemangiomas: demographic, prenatal, and perinatal characteristics, J Pediatr, 2007;150:291-4
- (en) Anita N. Haggstrom, Maria C. Garzon, Eulalia Baselga, Sarah L. Chamlin, Ilona J. Frieden, Kristen Holland, Sheilagh Maguiness, Anthony J. Mancini, Catherine McCuaig, Denise W. Metry, Kimberly Morel, Julie Powell, Susan M. Perkins, Dawn Siegel, and Beth A. Drolet « Risk for PHACE Syndrome in Infants With Large Facial Hemangiomas » Pediatrics 2010; 126: e418-e426. Abstract
- Bruckner AL, Frieden IJ, Hemangiomas of infancy, J Am Acad Dermatol, 2003;48:477-96
- Léauté-Labrèze C, Prey S, Ezzedine K, Infantile haemangioma: part II. Risks, complications and treatment, J Eur Acad Dermatol Venereol, 2011;25:1254-60
- Drolet BA, Frommelt PC, Chamlin SL et al. Initiation and use of propranolol for infantile hemangioma: report of a consensus conference, Pediatrics, 2013;131:128-40
- Léauté-Labrèze C, Hoeger P, Mazereeuw-Hautier J et al. A randomized, controlled trial of oral propranolol in infantile hemangioma, N Engl J Med, 2015;372:735-746
- Stier MF, Glick SA, Hirsch RJ, Laser treatment of pediatric vascular lesions: port wine stains and hemangiomas, J Am Acad Dermatol, 2008;58:261-85
Voir aussi
Articles connexes
Liens externes
- Portail de la médecine