Trichlorure d'antimoine
Le trichlorure d'antimoine est un composé chimique moléculaire de formule brute SbCl3. C'est un solide mou sans couleur qui était connu comme beurre d'antimoine par les alchimistes. Il a une odeur forte, et, au contact de l'eau, il s'hydrolyse formant de l'oxychlorure et dégageant du chlorure d'hydrogène. Ainsi, les échantillons de SbCl3 doivent être protégés de l'humidité :
| Trichlorure d'antimoine | |

| |
| Identification | |
|---|---|
| Synonymes |
chlorure d'antimoine III |
| No CAS | |
| No ECHA | 100.030.031 |
| Apparence | cristaux incolores, hygroscopiques, d'odeur âcre[1]. |
| Propriétés chimiques | |
| Formule | SbCl3 |
| Masse molaire[2] | 228,119 ± 0,007 g/mol Cl 46,62 %, Sb 53,38 %, |
| Propriétés physiques | |
| T° fusion | 73 °C[1] |
| T° ébullition | 223,5 °C[1] |
| Solubilité | dans l'eau à 25 °C : 100 g·l-1[1] 602g/100cm3 (0 °C) |
| Masse volumique | 3,14 g·cm-3[1] |
| Pression de vapeur saturante | à 49 °C : 133 Pa[1] |
| Thermochimie | |
| ΔvapH° | 45,19 kJ·mol-1 (1 atm, 220,3 °C)[3] |
| Cristallographie | |
| Système cristallin | orthorhombique |
| Précautions | |
| Directive 67/548/EEC | |
 C  N |
|
| Unités du SI et CNTP, sauf indication contraire. | |
SbCl3 forme des complexes avec le chlore par exemple: SbCl52-.
Structure cristalline
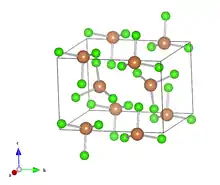

Le trichlorure d'antimoine cristallise dans une structure orthorhombique de groupe d'espace Pnma (a = 8,111 Å, b = 9,419 Å et c = 6,313 Å). Les atomes d'antimoine occupent les positions de Wyckoff 4c (x = 0.490, z = 0.475) et les atomes de chlore les positions 4c (x = 0.072 et z = 0.669) et 8d (x = 0.176, y = 0.071 et z = 0.134), formant des pyramides SbCl3 [4].
Usages
SbCl3 est un réactif pour la détection de la vitamine A et des autres caroténoïdes dans le test de Carr-Price. Le trichlorure d'antimoine réagit avec les caroténoïdes pour former un complexe bleu qui peut être mesuré par colorimétrie.
Le trichlorure d'antimoine a été utilisé pour simuler l'effet trouble de l'absinthe.
Il est aussi utilisé comme catalyseur pour des réactions de polymérisation, de craquage et de chloration ; comme mordant et dans la production d'autres sels d'antimoine. Ses solutions sont utilisées comme réactif chimique pour le chloral, les aromatiques et la vitamine A.
Notes et références
- TRICHLORURE D'ANTIMOINE, fiche(s) de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée(s) le 9 mai 2009
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC Press Inc, , 90e éd., 2804 p., Relié (ISBN 978-1-4200-9084-0)
- A. Lipka, "An X-ray structure redetermination of antimony trichloride", Acta Crystallographica B 35, 3020 (1979)
- Portail de la chimie