Fixation du carbone en C3
La fixation du carbone en C3 est une voie métabolique de fixation du carbone parmi les trois voies de la photosynthèse, les deux autres étant la fixation du carbone en C4 et le métabolisme acide crassulacéen (CAM). On l'appelle ainsi en référence au 3-phosphoglycérate, molécule à trois atomes de carbone formée par condensation du dioxyde de carbone CO2 sur du ribulose-1,5-bisphosphate par l'enzyme Rubisco :
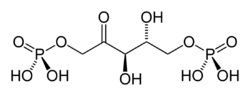
+ CO2 + H2O → 2 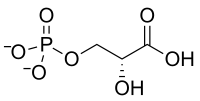
D-ribulose-1,5-bisphosphate 3-phospho-D-glycérate Ribulose-1,5-bisphosphate carboxylase/oxygénase (Rubisco) – EC
Cette réaction a lieu dans toutes les plantes comme première étape du cycle de Calvin. Chez les plantes en C4, le dioxyde de carbone est concentré autour de la Rubisco sous forme de malate.
Les plantes en C3, qui ne réalisent que la fixation du carbone en C3, tendent à se développer dans les environnement riches en eaux souterraines où le rayonnement solaire et la température sont modérés et la concentration de CO2 de l'ordre de 200 ppm ou plus[1]. Les plantes en C3, apparues au cours du Mésozoïque et du Paléozoïque, avant les plantes en C4, représentent encore aujourd'hui environ 95 % de la biomasse végétale. Elles perdent par transpiration 97 % de l'eau absorbée par leurs racines[2].
Les plantes en C3 incluent quelques-unes des sources de calories les plus importantes dans le monde, dont haricot niébé, manioc, soja, riz[3] et orge[4]. Les régions où poussent ces plantes sont souvent chaudes et sèches. Ces plantes ne peuvent pas optimiser leur croissance dans les zones trop chaudes parce que l'activité oxygénase de la Rubisco augmente avec la température par rapport à l'activité carboxylase, c'est-à-dire que la photorespiration devient prépondérante sur la fixation du carbone, ce qui conduit à une perte nette de carbone et d'azote par la plante. Dans les zones sèches, les plantes en C3 referment leurs stomates pour limiter leurs pertes en eau, mais cela a également pour effet de limiter l'entrée du dioxyde de carbone dans les feuilles et donc la concentration en CO2 dans ces dernières : cela réduit le ratio CO2/O2 et donc augmente la photorespiration[3].
Notes et références
- C. Michael Hogan. 2011. "Respiration". Encyclopedia of Earth. Eds. Mark McGinley and C. J. Cleveland. National Council for Science and the Environment. Washington, D.C.
- (en) J. A. Raven et D. Edwards, « Roots: evolutionary origins and biogeochemical significance », Journal of Experimental Botany, vol. 52, no supplément 1, , p. 381-401 (PMID 11326045, DOI 10.1093/jexbot/52.suppl_1.381, lire en ligne, consulté le )
- « The difference between C3 and C4 plants », sur ripe.illinois.edu, Realizing Increased Photosynthetic Efficiency for sustainable increase in crop yield, (consulté en ).
- Étienne Roth (dir.), Bernard (dir.), Georgette Délibrias et al. (préf. Jean Coulomb), Méthodes de datation par les phénomènes nucléaires naturels, Paris, Éditions Masson, coll. « CEA », , 631 p. (ISBN 2-225-80674-8), chap. 15 (« Le carbone 14 »).
- Portail de la biochimie
-3-Phosphoglyceric_acid_(3PG)_Structural_Formula_V.1.svg.png.webp)