Émail dentaire
L'émail est la partie externe de la couronne des dents. Cette substance, qui recouvre la dentine, est la plus dure et la plus minéralisée de l'organisme. Avec la dentine, le cément et la pulpe dentaire, il constitue un des quatre principaux tissus qui constituent la dent. Il est le tissu dentaire normalement visible, supporté par une couche sous-jacente de dentine. Il est composé à 96 % de matière minérale, le reste étant composé d'eau et de matière organique. Sa partie minérale est principalement composée d'un réseau de cristaux d'hydroxyapatite de calcium (Ca10(PO4)6(OH)2). Le fort pourcentage de minéraux dans l'émail est responsable non seulement de sa force, mais aussi de sa friabilité. La dentine, qui est moins minéralisée et moins friable, est indispensable comme support et compense les faiblesses de l'émail.


cementum = cément
La couleur de l'émail va du jaune au gris clair. Comme l'émail est semi-translucide, la couleur de la dentine (ou de tout matériau de réparation dentaire) sous l'émail affecte fortement l'apparence de la dent.
L'émail varie en épaisseur sur la surface de la dent. Il est plus épais au niveau du sommet de la couronne dentaire (plus de 2,5 mm) et plus mince sur la jonction émail-cément (JEC).
Contrairement au cément et aux os, la matrice organique de l'émail ne contient pas de collagène ni de kératine ; il possède à la place des glycoprotéines riches en tyrosine (amélogénines, énamélines et « tuft protein ») dont le rôle est, pense-t-on, d'aider à la croissance de l'émail en servant de cadre de construction, entre autres fonctions. Cette matrice organique contient aussi des polysaccharides.
La composition isotopique de l'émail[1] et l'analyse de la micro-usure dentaire observée à l'échelle microscopique sur l'émail permet aux paléontologues de détecter des différences en fonction de la composition du régime alimentaire[2].
Structure
L'émail est la substance la plus dure du corps humain[3]. Surtout composé de phosphate de calcium et de carbonate de calcium, comprenant moins de 1 % de matières organiques[3], il est formé par la juxtaposition de structures élémentaires appelées cordons ou prismes d'émail. Chaque prisme minéralisé de 4 à 8 µm de diamètre traverse l'émail, de la jonction émail-dentine jusqu'à la surface de la dent.

Ces prismes sont des cristaux d'hydroxyapatite entourés par une gaine de nature organique, imbriqués les uns dans les autres. En coupe transversale, ils ressemblent à un trou de serrure, avec la partie supérieure orientée vers la couronne de la dent et la base orientée vers la racine.
La disposition des cristaux à l'intérieur de chaque prisme est très complexe. Les améloblastes (ou adamantoblastes), cellules qui initient la formation de l'émail, et les prolongements de Tomes influent tous les deux sur la forme des cristaux. Les cristaux d'émail de la tête du prisme sont orientés parallèlement au grand axe de ce dernier alors que ceux de la base divergent légèrement du grand axe.
L'arrangement dans l'espace des prismes d'émail est compris plus clairement que leur structure interne. Les prismes d'émail sont situés en rang le long de la dent, et à l'intérieur de chaque rang, le grand axe du prisme est généralement perpendiculaire à la dentine sous-jacente. Dans les dents définitives, les prismes d'émail proches de la jonction émail-cément (JEC) basculent légèrement vers la racine de la dent.

bas:dentine
La zone située autour du prisme d'émail est constituée d'émail interprismatique. Ce dernier a la même composition que l'émail en prisme ; on fait cependant une distinction histologique entre les deux car l'orientation des cristaux est différente dans chaque cas. La limite où les cristaux d'émail prismatique et les cristaux d'émail interprismatique se touche est appelée gaine prismatique.
L'étude des caractéristiques des microstructure de l'émail dentaire (stries de Retzius, bandes de Hunter-Schreger) permet d'évaluer les modalités du développement dentaire. Les stries de Retzius (en) sont des bandes qui apparaissent sur l'émail quand il est observé en coupe transversale au microscope. Formées par la variation du diamètre des prolongements de Tomes, ces bandes attestent de la croissance de l'émail de façon similaire aux anneaux de croissance d'un arbre. Les perikymaties sont des sillons peu profonds correspondants à la ligne formée par les stries de Retzius à la surface de l'émail. Plus sombre que les autres bandes, la ligne néonatale sépare l'émail formé avant et après la naissance. Les bandes de Hunter-Schreger (en) sont marquées par la succession de bandes parallèles transversales claires (diazonies) et sombres (parazonies) dues à l'orientation des prismes dans la coupe.
Développement

La formation de l'émail fait partie du processus global de formation d'une dent. Quand on observe les tissus de la dent en développement au microscope, on peut distinguer différents amas de cellules, comme l'organe adamantin (Enamel organ), la lame dentaire et la papille dentaire. Les étapes généralement reconnues du développement de la dent sont le stade bourgeon, le stade capuchon, le stade cloche et le stade couronne (ou de calcification). L'émail en formation n'est visible qu'à partir du stade couronne.
L'amélogenèse (ou formation de l'émail) a lieu après le début de l'apparition de la dentine, grâce à des cellules appelées améloblastes. l'émail humain se forme à un taux d'environ 4 µm par jour, débutant au niveau de la future localisation des cupsides de la dent, au 3e ou 4e mois de grossesse environ. Comme dans tous les processus humains, la création de l'émail est complexe, mais peut généralement être divisée en deux étapes. La première étape, appelée stade sécrétoire, implique des protéines et une matrice organique formant un émail partiellement minéralisé. La seconde étape, appelée stade de maturation, complète la minéralisation de l'émail.
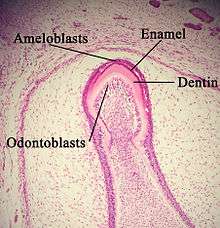
Lors du stade sécrétoire, les améloblastes sont des cellules polarisées en forme de colonne. Les protéines de l'émail sont produites au niveau du reticulum endoplasmique granuleux de ces cellules, puis relâchée dans le milieu extracellulaire où elles forment ce que l'on appelle la matrice de l'émail. Cette matrice sera alors partiellement minéralisée par une enzyme, la phosphatase alcaline. Quand cette première couche est formée, les améloblastes s'éloignent de la dentine, permettant le développement des prolongements de Tomes sur la partie apicale de la cellule. La formation de l'émail continue autour des améloblastes adjacents (ce qui induit la création d'une surface cloisonnée, ou « puits », qui abrite les prolongements de Tomes) et aussi autour de l'extrémité de chaque prolongement de Tomes (ce qui induit le dépôt d'une matrice de l'émail à l'intérieur de chaque puits). La matrice à l'intérieur du puits deviendra à terme le prisme d'émail, et les cloisons deviendront à terme l'émail interprismatique. Le seul facteur de distinction entre les deux est l'orientation des cristaux d'hydroxyapatite.

en=émail
d=dentine
od=odontoblates
p=papille dentaire
Lors de la phase de maturation, les améloblastes transportent des substances utilisées dans la formation de l'émail. L'aspect le plus notable de cette phase au niveau tissulaire est que ces cellules deviennent striées, ou ont une bordure ondulée. Ceci prouve que les améloblastes ont changé leur fonction : de productrice (cf la phase de sécrétion), elles deviennent transporteuses. Les protéines utilisées pour le processus final de minéralisation composent la majorité du matériel transporté. Les protéines impliquées les plus notables sont les amélogénines, améloblastines, enamélines et « tuft proteins ». Pendant ce processus, les amélogénines et améloblastines sont éliminées après usage, mais les énamélines et " tuft proteins " sont laissées dans l'émail. À la fin de cette phase, la minéralisation de l'émail est achevée.
Après la phase de maturation, mais avant que la dent apparaisse dans la bouche, les améloblastes se décomposent. Par conséquent l'émail, contrairement à la plupart des autres tissus du corps, n'a aucun moyen de se renouveler. Après une destruction de l'émail par action des bactéries ou par blessure, ni l'organisme, ni le dentiste ne pourront réparer le tissu de l'émail. L'émail peut de plus être affecté par des processus non pathologiques. La coloration des dents avec le temps peut résulter de l'exposition à des substances telles que le tabac, le café et le thé, mais la couleur de la dent peut aussi s'assombrir graduellement avec l'âge. En effet, l'assombrissement est en partie dû aux matériaux qui s'accumulent au niveau de l'émail, mais est aussi un des effets de la sclérotisation de la dentine sous-jacente. En outre, l'émail devient avec l'âge moins perméable aux fluides, moins soluble dans l'acide, et contient moins d'eau.
| Taux d'émail formé à la naissance | Achèvement de la minéralisation de l'émail | ||
|---|---|---|---|
| Dents Maxillaires Primaires |
Incisive centrale | ⅚ | 1,5 mois après la naissance |
| Incisive latérale | ⅔ | 2,5 mois après la naissance | |
| Canine | ⅓ | 9 mois après la naissance | |
| Prémolaire | Cuspides réunies; émail occlusal complètement minéralisé ; le tissu minéralisé couvre ½ à ¾ de la hauteur de la couronne |
6 mois après la naissance | |
| Molaire | Cuspides réunies; émail occlusal incomplètement minéralisé ; le tissu minéralisé couvre ⅕ à ¼ de la hauteur de la couronne |
11 mois après la naissance | |
| Dents Mandibulaires Primaires |
Incisive centrale | ⅗ | 2,5 mois après la naissance |
| Incisive latérale | ⅗ | 3 mois après la naissance | |
| Canine | ⅓ | 9 mois après la naissance | |
| Prémolaire | Cuspides réunies; émail occlusal complètement minéralisé | 5,5 mois après la naissance | |
| Molaire | Cuspides réunies; émail occlusal incomplètement minéralisé |
10 mois après la naissance | |
Destruction

Carie dentaire
La haute teneur en minéral de l'émail, qui fait de ce tissu le plus dur de tous les tissus humains, le rend aussi susceptible de subir un processus de déminéralisation qui survient souvent sous forme de carie dentaire. La déminéralisation peut survenir pour plusieurs raisons, mais la cause principale du développement des caries est l'ingestion de sucres.
Les sucres des bonbons, des boissons sucrées et même des jus de fruits jouent un rôle important dans la carie dentaire et par conséquent dans la destruction de l'émail. La bouche contient un grand nombre et une grande variété de bactéries, et quand le saccharose, le plus commun des sucres, couvre la surface de la dent, certaines bactéries buccales interagissent avec lui pour former de l'acide lactique, qui diminue le pH dans la bouche. Les cristaux d'hydroxyapatite de l'émail sont alors déminéralisés, permettant une invasion bactérienne plus importante et plus en profondeur dans la dent. La bactérie la plus impliquée dans la carie dentaire est Streptococcus mutans, mais le nombre et les espèces de bactéries varient en fonction de la progression de la destruction dentaire.
En outre, la morphologie de la dent veut que la localisation la plus commune pour un début de carie dentaire se situe dans des entailles, trous et fissures de l'émail. Ceci n'est pas étonnant car ces emplacements sont très difficiles voire impossibles à atteindre avec une brosse à dents, et permettent aux bactéries de s'installer là. Quand la déminéralisation de l'émail a lieu, un dentiste peut utiliser un instrument pointu, comme un crochet de dentiste, et sentir que " ça accroche " à l'emplacement de la carie. Comme l'émail se déminéralise toujours et est incapable d'empêcher les bactéries de s'accrocher, la dentine sous-jacente devient elle aussi atteinte. Quand la dentine, qui supporte l'émail en temps normal, est détruite par une carie ou autre souci de santé, l'émail est incapable de suppléer à sa friabilité et se détache facilement de la dent.
La cariogénicité (capacité à provoquer des caries dentaires) d'un aliment dépend de différents facteurs, comment par exemple la durée pendant laquelle les sucres restent dans la bouche. Ce n'est pas la quantité de sucre ingéré, mais la fréquence de l'ingestion de sucre qui est le principal facteur responsable des caries. Quand le pH dans la bouche diminue par ingestion de sucre, l'émail se déminéralise et reste vulnérable pendant 30 minutes environ. Manger davantage de sucre en une seule fois n'augmente pas la durée de la déminéralisation; de même, manger moins de sucre en une seule prise ne diminue pas la durée de déminéralisation. Ainsi, manger une grande quantité de sucre une seule fois dans la journée est moins néfaste qu'une très petite quantité ingérée à de nombreuses reprises tout au long de la journée. Par exemple, en termes de santé buccale, il est meilleur de manger un seul dessert au diner que de grignoter un sac de bonbons toute la journée.
Bruxisme

Outre les invasions bactériennes, l'émail est soumis à d'autres forces destructrices. Le bruxisme (grincement de dent compulsif) détruit l'émail très rapidement. Le taux d'usure de l'émail, appelé attrition, est de 8 µm par an en temps normal. C'est une erreur commune de croire que l'émail s'use principalement par mastication. En fait, les dents se touchent rarement pendant la mastication. De plus, le contact normal des dents est compensé physiologiquement par le ligament périodontal et la disposition des dents quand la bouche est fermée. Les forces réellement destructrices sont les mouvements de parafonction (tels que la succion qu'elle soit digitale (le plus souvent le pouce) ou d'un objet (tétine ou linge), ou le bruxisme), qui peuvent causer à l'émail des dommages irréversibles.
Autres causes de destruction de l'émail
Les autres processus de destruction non-bactérienne de l'émail comprennent l'abrasion (par des éléments étrangers comme les brosses à dent, ou les épingles ou tuyaux de pipe tenus entre les dents), l'érosion (par des processus chimiques faisant intervenir des acides, par exemple l'action du jus de citron ou le suc gastrique lorsqu'il remonte l'œsophage), et parfois l'abfraction (par des forces de compression ou de tension).
Hygiène buccale et fluor
Nettoyage des dents
L'émail est donc très vulnérable face à la déminéralisation, et les attaques consécutives à l'ingestion de sucre sont quotidiennes. Ainsi, la santé dentaire passe essentiellement par des méthodes préventives visant à réduire la présence de débris alimentaires et de bactéries en contact avec l'émail. On utilise pour cela dans la plupart des pays la brosse à dent, qui réduit le nombre de bactéries et de particules alimentaires sur l'émail. Quelques sociétés isolées n'ayant pas accès à ce genre de matériel utilisent d'autres objets, comme des morceaux de bois fibreux ou pointus, pour le nettoyage des dents. Pour nettoyer la surface de l'émail entre deux dents adjacentes, on peut utiliser du fil dentaire. Ni la brosse à dent, ni le fil dentaire ne peuvent atteindre les creux microscopiques de l'émail, mais de bonnes habitudes d'hygiène buccale et une alimentation pauvre en sucres rapides empêchent généralement suffisamment le développement de la population bactérienne et donc l'apparition de caries dentaires.
Email et fluor
Le fluor se trouve naturellement dans l'eau, mais à des taux très variables. Il est aussi présent dans tous les aliments d'origine marine (poissons, fruits de mer, sel de mer etc.). Le taux de fluor recommandé dans l'eau de boisson est de 1 ppm (partie par million). Le fluor aide à la prévention des caries en se liant aux cristaux d'hydroxyapatite de l'émail, ce qui rend ce dernier plus résistant à la déminéralisation, et donc plus résistant à l'apparition des caries. Cependant, un excès de fluor peut être problématique en provoquant des troubles appelés fluorose dentaire. La fluorose est donc une surexposition au fluor, surtout entre 6 mois et 5 ans, et se manifeste par l'apparition de taches sur les dents. L'aspect des dents devient alors pour le moins inesthétique, même si l'incidence des caries sur ce genre d'émail est très faible. Pour éviter ce problème, on peut utiliser des filtres dans les zones où le taux de fluor dans l'eau du robinet est trop élevé afin de le réduire. Le taux de fluor est considéré comme toxique lorsqu'il dépasse 0,05 mg de fluor par kg de masse corporelle. Le fluor ajouté dans les pâtes dentifrice ou les bains de bouche ne semble avoir qu'un effet limité aussi bien sur la fluorose que sur la prévention des caries. Il semble que seul le fluor ingéré dans l'eau ou le sel fluoré puisse avoir une action réelle[réf. nécessaire], qu'elle soit positive ou négative ; seule la surface de l'émail est atteinte par le fluor des pâtes dentifrice.
Salive
La salive a un rôle protecteur sur l'émail. Elle contient plusieurs éléments protecteurs, régulateurs, agissant individuellement ou s’organisant en véritables systèmes de défense contre les bactéries, mais aussi en apportant des ions nécessaires à la re-minéralisation de la dent, lorsque celle-ci n'est pas trop abîmée.
Effet des techniques dentaires
Réparation dentaire
De nombreuses réparations dentaires nécessitent d'enlever au moins une partie de l'émail. Généralement, le but de cette pratique est d'accéder aux couches sous-jacentes infectées, comme la dentine ou la pulpe dentaire, par exemple dans le cas d'une odontologie conservatrice, d'une endodontie ou de l'installation d'une couronne. L'émail peut aussi avoir disparu avant toute apparition de carie (voir #Destruction).
Mordançage à l’acide
Inventée en 1955, cette technique emploie un mordant dentaire. Elle est couramment utilisée en odontologie conservatrice. En dissolvant les minéraux de l'émail, le mordant enlève 10 µm de la surface de l'émail et implique la création d'une couche poreuse de 5 à 50 µm de profondeur. Ceci rend l'émail rugueux au niveau microscopique et augmentera l'adhérence des matériaux utilisés pour la réparation dentaire nécessitant des collages (composite dentaire).
Les effets du mordançage varient en fonction de la durée de son application, du type de mordant utilisé, et de l'état de l'émail sur lequel le mordançage est appliqué. On pense aussi que les résultats obtenus varieraient en fonction de l'orientation des cristaux de l'émail.
Blanchiment dentaire
Note : on rencontre aussi le terme « blanchissement » malgré son sens habituel passif (blanchissement des cheveux).
Maladies, polluants ou médicaments affectant la qualité de l'émail
- chez le très jeune enfant certains médicaments acides semblent pouvoir attaquer l'émail dentaire encore immature[5].
- chez les très jeunes enfants, des phénomènes de reflux gastro-œsophagien peuvent aussi dégrader l'émail[6].
- chez les enfants de moins de 8 ans, certains médicaments anti-acnéiques peuvent aussi poser problème de et dyschromie et d'hypoplasie de l'émail dentaire (résumé)[7]
- L'amoxicilline peut induire une dyschromie de l'émail dentaire[8]
- Certains perturbateurs endocriniens inhibent aussi la minéralisation de l'émail dentaire (hypominéralisation) ce qui est source d'anomalies de colorations des dents (15 à 18% des enfants de 6 à 9 ans sont touchés par ce phénomène qui semble en augmentation) et d'une hypersensibilité dentaire (risque accru de caries)[9]
Parmi les hypothèse évoquées concernant les sources de perturbateurs figurent notamment un apport de Bisphénol A à partir des résines dentaires ; des traces en sont effectivement retrouvées dans la salive, au moins pour 5 types de résines testées in vitro et in vivo (étude 2017) et avec un pic de relarguage 30 mois après la liaison avec la dent cariée, et avec des taux de relarguage variant selon la marque du composites orthodontiques. Les flux restent inférieurs à la dose de référence pour l'ingestion quotidienne [10] (mais cette dose est discutée). Des perturbateurs endocriniens peuvent aussi être présents dans les dentifrices (facilement avalés par les enfants ou mal rincés)[9].
Le BPA a une action démontrée sur l’amélogenèse (formation de l'émail) chez le rat de laboratoire qui développe des taches opaques jaunes à blanches sur l'émail dentaire lorsqu'exposé au BPA, peut être via une action hormonale sur les améloblastes (cellules qui génèrent l'émai)[9])[11],[12].
Le BPA pourrait perturber l'élimination des protéines de la matrice dentaire. (88) et il affecte les glandes salivaires en induisant une sécheresse buccale pouvant nuire à la durabilité de l'émail[9].
Émail chez les animaux
Voir aussi
- Dent
- Émail
- Dentine
- Carie dentaire
- Amélogenèse
- Améloplastie
- Hydroxyapatite
Bibliographie et sources
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Tooth enamel » (voir la liste des auteurs).
- CHU-ps :Histologie : organes, systèmes et appareils
- Congrès de l'Association Dentaire Française
- Faculté de chirurgie dentaire de Toulouse
- Michael H. Ross, Gordon I. Kaye, and Wojciech Pawlina, Histology: a Text and Atlas, 4th ed. (Baltimore: Lippincott Williams & Wilkins, 2002)
- A. R. Ten Cate, Oral Histology: Development, Structure, and Function, 5th ed. (Saint Louis: Mosby-Year Book, 1998)
- Biology of the Human Dentition
- American Dental Hygienists' Association
- James B. Summitt, J. William Robbins, and Richard S. Schwartz, eds., Fundamentals of Operative Dentistry: A Contemporary Approach, 2nd ed. (Carol Stream, IL: Quintessence Publishing, 2001)
- Major M. Ash and Stanley Nelson, Wheeler’s Dental Anatomy, Physiology, and Occlusion 8th ed. (Philadelphia: W.B. Saunders Co., 2003)
- Brown, LeMay, Burslen, Chemistry The Central Science, (ISBN 0-13-048450-4)
- "Dental Health", British Nutrition Foundation website
- Definitions of Tooth Surface Loss.
- Dean, Arnold, and Elvove, « Domestic water and dental caries », Public Health Reports 52, no. 32 (1942): 1155–79.
- E. Newbrun, Fluorides and dental caries (Springfield, IL: Charles C. Thomas publisher, 1986).
- Edward F. Harris « X-Linked Inheritance », Craniofacial Growth and Development 2002
- Frandson et al., Anatomy and Physiology of Farm Animals, 5th ed. (Baltimore: Lippincott Williams & Wilkins, 1992)
- Chris C. Pinney, The Illustrated Veterinary Guide for Dogs, Cats, Birds, and Exotic Pets (Blue Ridge Summit, PA: TAB Books, 1992)
- Fejerskov : Human dentition and experimental animals
Référence
- La teneur en isotopes stables du carbone et de l'azote reflète notamment le type de plantes consommées (à photosynthèse en C3 ou en C4) et le niveau trophique. L'isotope du Zinc 66Zn est également un indicateur du régime alimentaire, permettant de distinguer les carnivores des herbivores (et encore plus finement les brouteurs des pâtureurs). cf. (en) Klervia Jaouen et al, « Zinc isotope ratios of bones and teeth as new dietary indicators: results from a modern food web (Koobi Fora, Kenya) », Scientific Reports, vol. 6, no 26281, (DOI 10.1038/srep26281).
- (en) P. S. Ungar, R. S. Scott, J. R. Scott, M. F. Teaford, « Dental microwear analysis: Historical perspectives and new approaches », In : J. D. Irish and G. C. Nelson (Eds.), Technique and application in dental anthropology, 2008, p. 389–425.
- Le Corps Humain : comprendre notre organisme et son fonctionnement, Québec Amérique, coll. « Guides de la connaissance », , 128 p. (lire en ligne), p. 107.
- wheeler_enamelformationchart.
- Bouferrache, K., Pop, S., Abarca, M., & Madrid, C. (2010). Le pédiatre et les dents des tout petits. Paediatrica, 21(1), 14-20.
- Madrid, C., Abarca, M., Pop, S., Korsvold, T., & Bouferrache, K. (2010). Lésions buccales du reflux gastro-œsophagien de l'enfant: des réalités et quelques mythes. Revue médicale suisse, (237), 384.
- Faure, S. (2014). Médicaments de l’acné. Actualites pharmaceutiques, 53(538), 57-61.
- Krivine, S., Nobécourt, J., Soualmia, L., Cerbah, F., & Duclos, C. (2009). Construction automatique d'ontologie à partir de bases de données relationnelles: application au médicament dans le domaine de la pharmacovigilance. In IC mai 2009 (p. pp).
- Canivenc-Lavier M-C, Jedeon K, Babajko S. Vers une dentisterie sans perturbateurs endocriniens. In Paris: Réseau Environnement Santé; 2016 [cité 21 nov2016]. http://www.reseau-environnement-sante.fr/wp-content/uploads/2016/05/dossier-de-presse-colloque-dentisterie-sans-PE.pdf.
- Moreira, M. R., Matos, L. G., de Souza, I. D., Brigante, T. A. V., Queiroz, M. E. C., Romano, F. L., ... & Matsumoto, M. A. N. (2017). Bisphenol A release from orthodontic adhesives measured in vitro and in vivo with gas chromatography. American Journal of Orthodontics and Dentofacial Orthopedics, 151(3), 477-483.
- Goldberg M (2016). Perturbateur endocrinien : le bisphénol A. Médecine Buccale. .
- Dure‐Molla M de la, Berdal A (2015) Odontogénétique : cytodifférenciation dentaire et maladies rares associées. Médecine Buccale ; 28(20):10.
- Portail de la médecine