Pramipexole
Le pramipexole (Mirapex, Mirapexin aux États-Unis, Sifrol en Europe) est un agoniste de la dopamine non dérivé de l'ergot de seigle, indiqué pour le traitement à un stade précoce la maladie de Parkinson[2] et le syndrome des jambes sans repos[3].
| Pramipexole | |

| |
| Identification | |
|---|---|
| DCI | Pramipexole |
| Nom UICPA | (S)-N6-propyl-4,5,6,7-tetrahydro-1,3-benzothiazole-2,6-diamine |
| No CAS | |
| No ECHA | 100.124.761 |
| No CE | CSOID0000155649 |
| Code ATC | N04 |
| DrugBank | DB00413 |
| PubChem | |
| ChEBI | 8356 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C10H17N3S [Isomères] |
| Masse molaire[1] | 211,327 ± 0,015 g/mol C 56,83 %, H 8,11 %, N 19,88 %, S 15,17 %, 211,324 g/mol |
| Données pharmacocinétiques | |
| Biodisponibilité | > 90 % |
| Liaison protéique | 15 % |
| Demi-vie d’élim. | 8 à 12 h |
| Excrétion |
Urine (90 %), Selles (≤ 2 %) |
| Considérations thérapeutiques | |
| Classe thérapeutique | Agoniste dopaminergique |
| Voie d’administration | orale |
| Grossesse | Ne doit être utilisé pendant la grossesse qu'en cas de nécessité absolue |
| Conduite automobile | Influence majeure sur la capacité à conduire et à utiliser des machines |
| Caractère psychotrope | |
| Catégorie | Antiparkinsoniens - Dopaminergiques : Agonistes dopaminergiques |
| Mode de consommation |
oral |
| Autres dénominations |
Sifrol |
| Risque de dépendance | Important |
| Unités du SI et CNTP, sauf indication contraire. | |
Chimie
Le pramiprexole peut être synthétisé à partir d'un dérivé de la cyclohexanone selon le processus suivant[4] :
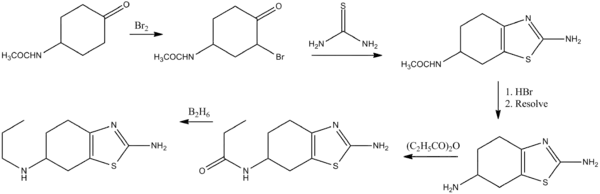
Pharmacologie
Le pramipexole agit comme un agoniste partiel ou complet des récepteurs suivants[5],[6],[Note 1] :
- Récepteurs D2S : Ki = 3,9 nM[Note 2] ; Effet agoniste = 130 %
- Récepteurs D2L : Ki = 2,2 nM ; Effet agoniste = 70%
- Récepteur D3 : Ki = 0,5 nM ; Effet agoniste = 70%
- Récepteur D4 : Ki = 5,1 nM ; Effet agoniste = 42%
Le pramipexole possède également une affinité faible à très faible (500 nM à 10 000 nM)) pour les récepteurs sérotoninergiques a 5-HT1A, 5-HT1B, 5-HT1D et α2-adrénergiques[5],[7].
Il a une affinité négligeable (> 10 000 nM) pour les récepteurs dopaminergiques D1, D5, les récepteurs sérotoninergiques 5-HT2, les récepteurs alpha-1-adrénergiques, béta-adrénergiques, les récepteurs H1 à l'histamine et les récepteurs muscariniques[5],[6].
| pramipexole | |
| Noms commerciaux |
|
|---|---|
| Sels | dichlorhydrate, dichlorhydrate monohydrate |
| Classe | Agoniste de la Dopamine (ATC code N04BC05) |
| Identification | |
| No CAS | |
| No ECHA | 100.124.761 |
| Code ATC | N04BC05 |
| DrugBank | 00413 |
Indications
Maladie de Parkinson et SJSR
En France, en 2013, le pramipexole (Sifrol) a l'AMM dans :
- le traitement des symptômes et signes de la maladie de Parkinson idiopathique, en monothérapie (sans lévodopa) ou en association à la lévodopa, lorsqu’au cours de l’évolution de la maladie, au stade avancé, l’effet de la lévodopa s’épuise ou devient inconstant et que des fluctuations de l’effet thérapeutique apparaissent (fluctuations de type fin de dose ou effets "on-off")[2].
- Le dérèglement du système dopaminergique est une caractéristique importante de cette maladie. Il existe dans certaines structures du cerveau un déficit de dopamine (un neurotransmetteur, molécule servant de messager chimique entre deux neurones, synthétisée dans une terminaison axonale ; le neurotransmetteur est libéré dans la fente synaptique en réponse à un influx nerveux). Les altérations cérébrales ne se limitent pas seulement à la sphère dopaminergique et de nombreux systèmes de neurotransmetteurs (sérotoninergiques, cholinergiques, glutamatergiques, adénosinergiques ou encore adrénergiques) sont également atteints. En agissant comme un agoniste des récepteurs de la dopamine D2, D3, D4, le pramipexole stimule directement ces récepteurs dans le striatum, ramenant ainsi les signaux dopaminergiques nécessaires pour le bon fonctionnement des noyaux gris centraux.
- le traitement symptomatique du syndrome des jambes sans repos (SJSR) chez l'adulte : le traitement est réservé aux formes très sévères compte tenu qu'il expose à des troubles graves du comportement (dépendance aux jeux, comportements répétitifs, achats compulsifs, hypersexualité) et à l'aggravation des symptômes favorisée par des doses élevées et une durée prolongée[8].
Dépression bipolaire
Dans une seule étude contrôlée de 21 patients, le pramipexole a été jugé très efficace dans le traitement de la dépression bipolaire. Le traitement a été initié à 0,125 mg trois fois par jour et augmenté à un taux de 0,125 mg trois fois par jour dans la limite de 4,5 mg par jour jusqu'à ce que l'état des patients ait répondu de façon satisfaisante ou que les effets secondaires soient devenus difficiles à tolérer. La dose finale moyenne était de 1,7 mg ± 0,90 mg par jour. L'incidence de l'hypomanie dans le groupe sous traitement n'était pas plus élevée que dans le groupe témoin[9].
D'autres études semblent confirmer l'effet du pramipexole sur les troubles bipolaires[10],[11].
Algies vasculaires de la face
Le pramipexole est aussi parfois utilisé hors AMM en tant que traitement des algies vasculaires de la face ce qui alimente une controverse[12],[13].
Dysfonction sexuelle induits par les antidépresseurs
Le pramipexole a été proposé pour neutraliser les problèmes de dysfonction sexuelle induits par les neuroleptiques[14].
Fibromyalgies
Le pramipexole est également à l'étude pour le traitement de la fibromyalgie[15].
Effets secondaires
Effets indésirables graves
Le pramipexole peut induire des effets indésirables tels que le jeu pathologique, l'hypersexualité et/ou la boulimie[16] même chez les patients sans antécédents de ces comportements[17].
Ces comportements ont été rapportés chez près de 14 % des patients sous thérapies agonistes dopaminergiques. D'autres comportements compulsifs tels que l'excès de shopping ont été rapportés[18].
Ces effets secondaires peuvent être liés à l'activité du pramipexole sur les récepteurs D3, récepteurs fortement exprimés dans les régions du cerveau impliquées dans l'humeur, le comportement et la récompense[Note 3],[19].
Le pramipexole semble aussi augmenter chez les patients traités pour la maladie de Parkinson les risques de développer un mélanome d'un facteur de 2 à 6 sans que la cause ne puisse être identifiée[20].
Il apparaît aussi un risque fort accru de narcolepsie, ce qui sous-entend un fort suivi du patient afin que, par exemple, cela ne survienne pas lorsqu'il est au volant[20].
Il semble exposer à des insuffisances cardiaques[21].
Il semble avoir un potentiel de pharmacodépendance important (des cas d'utilisation d’antalgique opioïde fort, notamment l'oxycodone et l'hydrocodone, ont été reportés lors de tentative de sevrage du pramipexole hors cadre hospitalier outre-atlantique).[réf. nécessaire]
Autres effets indésirables
Le pramipexole peut aussi provoquer[22] :
- Céphalée
- Hyperalgésie (courbatures et douleurs)
- Nausées et vomissements
- Sédation et somnolence
- Diminution de l'appétit et perte de poids
- Hypotension orthostatique (se traduisant par des vertiges, des étourdissements et, éventuellement, des évanouissements, surtout en position debout)
- Insomnie
- Hallucinations
- Myoclonies
- Fatigue ou faiblesse inhabituelle
Notes et références
Notes
- Voir les définitions du Ki à l'article Inhibiteur enzymatique
- nM = nanomole
- Dans cette classe, le ropinirole a été déremboursé en France le
Références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Avis de la Commission de la transparence HAS,
- Synthèse d'avis HAS, décembre 2012
- (en)C.S. Schneider, J. Mierau, « Dopamine autoreceptor agonists: resolution and pharmacological activity of 2,6-diaminotetrahydrobenzothiazole and an aminothiazole analogue of apomorphine », Journal of medicinal chemistry, vol. 30, no 3, , p. 494-498 (PMID 3820220, lire en ligne, consulté le )
- (en)T. Kvernmo, S. Härtter, E. Burger, « A review of the receptor-binding and pharmacokinetic properties of dopamine agonists », Clinical therapeutics, vol. 28, no 8, , p. 1065-1078 (PMID 16982285, lire en ligne, consulté le )
- (en)A. Newman-Tancredi, D. Cussac, V. Audinot, J.P. Nicolas, F De Ceuninck, J.A. Boutin, M.J. Millan, « Differential actions of antiparkinson agents at multiple classes of monoaminergic receptor. II. Agonist and antagonist properties at subtypes of dopamine D(2)-like receptor and alpha(1)/alpha(2)-adrenoceptor », The Journal of pharmacology and experimental therapeutics, vol. 303, no 2, , p. 805-814 (PMID 12388667, lire en ligne, consulté le )
- (en)M.J. Millan, L. Maiofiss, D. Cussac, V. Audinot, J.A. Boutin, A. Newman-Tancredi, « Differential actions of antiparkinson agents at multiple classes of monoaminergic receptor. I. A multivariate analysis of the binding profiles of 14 drugs at 21 native and cloned human receptor subtypes », The Journal of pharmacology and experimental therapeutics, vol. 303, no 2, , p. 791-804 (PMID 12388666, lire en ligne, consulté le )
- [PDF]Mise au point HAS de décembre 2012
- (en) C.A. Zarate Jr et al., « Pramipexole for bipolar II depression: a placebo-controlled proof of concept study », Biological psychiatry, vol. 56, no 1, , p. 54-60. (PMID 15219473, lire en ligne, consulté le )
- (en) L. Lattanzi et al., « Pramipexole in treatment-resistant depression: a 16-week naturalistic study », Bipolar disorders, vol. 4, no 5, , p. 307-314. (PMID 12479663, lire en ligne, consulté le )
- (en) P. Cassano et al., « Pramipexole in treatment-resistant depression: an extended follow-up », Depression and anxiety, vol. 20, no 3, , p. 131-138. (PMID 15549689, lire en ligne, consulté le )
- (en)M. Ossemann, « Recurrence of cluster headache with pramipexole », Acta neurologica Belgica, vol. 110, no 3, , p. 279-280 (PMID 21114140, lire en ligne, consulté le )
- (en)A. Palmieri, « Chronic cluster headache responsive to pramipexole », Cephalalgia, vol. 26, no 6, , p. 761-762 (PMID 16686920, lire en ligne, consulté le )
- (en)M. Ishitobi, H. Kosaka, K. Shukunami, T. Murata, Y. Wada, « Adjunctive treatment with low-dosage pramipexole for risperidone-associated hyperprolactinemia and sexual dysfunction in a male patient with schizophrenia », Journal of clinical psychopharmacology, vol. 31, no 2, , p. 243-245 (PMID 21364336, lire en ligne [html], consulté le )
- (en)A.J. Holman, R.R. Myers, « A randomized, double-blind, placebo-controlled trial of pramipexole, a dopamine agonist, in patients with fibromyalgia receiving concomitant medications », Arthritis and rheumatism, vol. 52, no 8, , p. 2495-2505 (PMID 16052595, lire en ligne [html], consulté le )
- (en)E.Ch. Wolters, Y.D. van der Werf, O.A. van den Heuvel, « Parkinson's disease-related disorders in the impulsive-compulsive spectrum », Journal of neurology, vol. 255, no Suppl. 5, , p. 48-56 (PMID 18787882, lire en ligne [htlm], consulté le )
- (en)J.M. Bostwick, K.A. Hecksel, S.R. Stevens, J.H. Bower, J.E. Ahlskog, « Frequency of new-onset pathologic compulsive gambling or hypersexuality after drug treatment of idiopathic Parkinson disease », Mayo Clinic proceedings, vol. 84, no 4, , p. 310-306 (PMID 19339647, lire en ligne [htlm], consulté le )
- (en)J.R. Cornelius et al., « Impulse control disorders with the use of dopaminergic agents in restless legs syndrome: a case-control study », Sleep, vol. 33, no 1, , p. 81-87 (PMID 20120624, lire en ligne [htlm], consulté le )
- (en)M.L. Dodd, K.J. Klos, J.H. Bower, Y.E. Geda, K.A. Josephs, J.E. Ahlskog, « Pathological gambling caused by drugs used to treat Parkinson disease », Archives of neurology, vol. 62, no 9, , p. 1377-1381 (PMID 16009751, lire en ligne [htlm], consulté le )
- http://dailymed.nlm.nih.gov/dailymed/lookup.cfm?setid=e8f5aad8-8984-4f1e-8ab0-72f7af5e42ea MIRAPEX (pramipexole dihydrochloride) tablet
- la revue prescrire n°356 p434
- [PDF]Avis de la commission de transparence HAS
Liens externes
- Page spécifique dans la base de données sur les produits pharmaceutiques (Canada)
- Compendium suisse des médicaments : spécialités contenant Pramipexole
- Page spécifique sur le Répertoire Commenté des Médicaments, par le Centre belge d'information pharmacothérapeutique
- Page spécifique sur le Vidal.fr
- Portail de la chimie
- Portail de la médecine
- Portail de la pharmacie