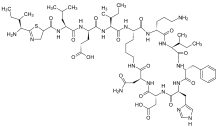
Peptide cyclique
Un peptide cyclique est un polypeptide où l'amine terminale et le carboxyle terminal, l'amine terminale et une chaîne latérale, le carboxyle terminal et une chaîne latérale ou deux chaînes latérales sont liés par une liaison covalente, ce qui rend la molécule cyclique. De nombreux peptides cycliques ont été découverts dans la nature, et une pléthore a été synthétisée en laboratoire. Leur longueur varie de deux résidus d'acide aminé à plusieurs centaines. Ils ont de nombreuses applications en médecine et en biologie.
Classification
Les peptides cycliques peuvent être classifiés selon le type de liaisons présentes dans le cycle.
- Les peptides cycliques homodétiques, tels que la ciclosporine A, sont les peptides cycliques dont le cycle est exclusivement composé de liaisons peptidiques normales (par exemple entre le carboxyle alpha d'un résidu et l'amine alpha d'un autre). Les plus petits éléments de cette famille sont les 2,5-dicétopipérazines, composés dérivés par cyclisation de dipeptides.
- Les isopeptides cycliques sont les composés contenant au moins une liaison amide non-alpha, par exemple entre une chaîne latérale d'un résidu et un groupe carboxyle alpha d'un autre résidu, comme dans le cas des microcystines ou de la bacitracine.
- Les depsipeptides cycliques, tels que l'auréobasidine A et HUN-7293, qui possèdent au moins une liaison de type ester carboxylique à la place d'une liaison amide. Certains depsipeptides cycliques sont cyclisés par une liaison entre le carbone du carboxyle terminal et une chaîne latérale, par exemple un résidu Thr ou Ser comme c'est le cas pour le kahalalide F, le théonellapeptolide ou la didémnine B.
- Les peptides bicycliques, tels que les amatoxines et les phallotoxines, contenant un groupe pontant, généralement entre deux chaînes latérales. Dans les amatoxines, ce pont est formé par une liaison thioéther entre des résidus Trp et Cys. On peut aussi citer parmi eux l'échinomycine, la triostine A et la célogentine C. Il existe aussi de nombreuses hormones peptidiques cycliques, cyclisées par des ponts disulfure entre deux cystéines, comme la somatostatine et l'ocytocine.
Voir aussi
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Cyclic peptide » (voir la liste des auteurs).
- Portail de la chimie
- Portail de la biochimie
Cet article est issu de Wikipedia. Le texte est sous licence Creative Commons - Attribution - Partage dans les Mêmes. Des conditions supplémentaires peuvent s'appliquer aux fichiers multimédias.