Myxobolus cerebralis
Myxobolus cerebralis est un parasite des salmonidés (saumon, truite et affiliés) de la classe des myxosporea. Il provoque la maladie du tournis dans les élevages de saumon, de truite et également dans les populations de poissons sauvages. Il a d'abord été découvert dans la truite arc-en-ciel en Allemagne il y a un siècle, mais son aire de répartition s'est propagée et il est apparu dans la plupart de l'Europe (y compris la Russie), les États-Unis, Afrique du Sud[1], Canada[2] et dans d'autres pays. Dans les années 1980, il a été découvert que M. cerebralis avait également besoin d'un oligochaeta Naididae (une sorte de ver segmenté) pour compléter son cycle de vie[3]. Le parasite infecte ses hôtes avec ses cellules après les avoir percées avec ses filaments polaires, éjectés de cellules proches des nématocystes.
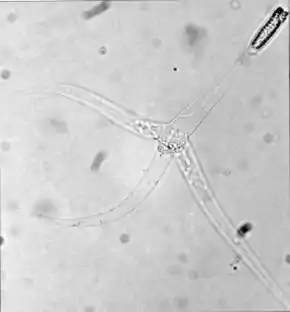
noter les trois « queues »
| Règne | Animalia |
|---|---|
| Embranchement | Cnidaria |
| Classe | Myxosporea |
| Ordre | Bivalvulida |
| Famille | Myxobolidae |
| Genre | Myxobolus |
| Espèce | cerebralis |
Myxosoma cerebralis
Triactinomyxon dubium
Triactinomyxon gyrosalmo
La maladie du tournis, qui affecte les jeunes poissons, cause des déformations du squelette et des dommages neurologiques. Les poissons « tourbillonnent » vers l'avant suivant un mouvement en tire-bouchon au lieu de nager normalement, compliquant la recherche de nourriture et les rendant plus vulnérables aux prédateurs. Le taux de mortalité est élevé pour les alevins, jusqu'à 90 % de la population infectée, et ceux qui survivent sont déformés par les parasites résidant dans leur cartilage et leur os. Ils agissent alors comme un réservoir de parasite. Ceux-ci sont libérés dans l'eau après la mort du poisson. M. cerebralis est l'un des Myxozoa les plus impactant économiquement, dans le secteur de la pisciculture, ainsi que l'un des plus pathogène. Il fut le premier Myxosporea dont la pathologie et les symptômes ont été décrits scientifiquement[4]. Le parasite n'est pas transmissible à l'homme.
Taxonomie
La taxonomie et la désignation de M. cerebralis, et des myxozoae en général, est compliqué. Il a été pensé à l'origine que ce parasite infectait le cerveau des poissons (d'où l' épithète spécifique : cerebralis) et le système nerveux, mais il a été récemment découvert qu'il infectait principalement le cartilage et les tissus squelettiques. Les tentatives de changer son nom en Myxobolus chondrophagus, décrivant plus précisément l'organisme, ont échoué en raison des règles de la nomenclature. Plus tard, les organismes précédemment appelé Triactinomyxon dubium et T. gyrosalmo (classe des Actinosporea) se sont avérés être, en fait, l'étape triactinomyxon du cycle de vie de M. cerebralis, qui a été élargi pour inclure cette étape[5]. De même, d'autres Actinosporea ont été inclus dans les cycles de vie des différents Myxosporea.
Aujourd'hui, les Myxozoa, que l'on croyait être des protozoaires multicellulaires, sont considérés comme des animaux par la plupart des scientifiques, bien que leur statut n'ait pas officiellement changé. De récentes études moléculaires suggéraient qu'ils étaient liés à des Bilatériens ou des Cnidaires, bien que plus proche morphologiquement des Cnidaires parce que les deux groupes ont des filaments extrusifs[6]. Les Bilatériens étaient un peu plus proches dans certaines études génétiques[7], mais celles-ci semblent avoir été faussées par des échantillons qui ont été contaminés par du matériel génétique de l'hôte, et une étude de 2015 confirme qu'ils sont bien des cnidaires[8].
Morphologie
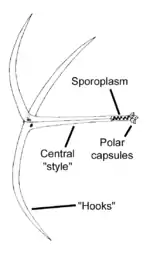
M. cerebralis a de nombreuses étapes de vie différentes qui vont de la cellule simple à une étape de spore relativement grande. Toutes n'ont pas été étudiées en détail.
Stade Triactinomyxon
L'étape qui infecte le poisson, appelé spore triactinomyxon, est constitué d'un style unique, qui fait d'environ 150 micromètres (µm) de long et trois processions ou "queues", chacune d'environ 200 micromètres de long. Le sporoplasme : paquet au bout du style contient 64 cellules germinales entourées par une enveloppe cellulaire. Il y a également trois capsules polaires, chacune contenant un rouleau de filament polaire faisant entre 170 et 180 µm de long. Les filaments polaires, à la fois dans ce stade et dans le stade myxospore, pénètre rapidement dans le corps de l'hôte, et crée une ouverture à travers laquelle le sporoplasme peut entrer.
Stade sporoplasme
Lors du contact avec le poisson hôte et l'accrochage des filaments polaires, le sporoplasme contenu dans le style centrale du triactinomyxon migre dans l'épithélium ou la paroi intestinale. Tout d'abord, ce sporoplasme subit une mitose pour produire plus d'amiboïdes, cellules qui migrent dans les tissus plus profonds, pour atteindre le cartilage cérébral .
Stade Myxospore
Les Myxospores, qui se développent à partir du stade sporogonic dans les tissus cellulaires du poisson hôte, sont de forme lenticulaire. Elles ont un diamètre d'environ 10 micromètres, et sont composées de six cellules. Deux de ces cellules forment des capsules polaires, deux autres s'associent pour former un sporoplasme binucléé, et les dernières forment des valves de protection. Les Myxospores sont infectieux pour les oligochètes, que l'on trouve parmi les restes de digestion des poissons cartilagineux. Ils sont souvent difficiles à distinguer des autres espèces en raison des similitudes morphologiques à travers les genres. Si M. cerebralis est le seul Myxosporea trouvé dans le cartilage des salmonidés, d'autre espèces visuellement similaires peuvent être présentes dans la peau, le système nerveux ou musculaire.
Cycle de vie
.png.webp)
Myxobolus cerebralis a un cycle de vie à deux hôtes impliquant un salmonidés et un Oligochaeta Naididae. Jusqu'à présent, le seul ver connus pour être sensible à M. cerebralis est Tubifex tubifex, bien que ce que les scientifiques appel actuellement T. tubifex peut en fait être plus d'une espèce. Tout d'abord, les myxospores sont ingérés par le ver. Dans la lumière de l'intestin du ver, les spores expulsent leurs capsules polaires et s'attachent à l'épithélium de l'intestin grâce aux filaments polaires. Les valves de protection s'ouvrent le long de la ligne de suture et le sporoplasme binucléé pénètre entre les cellules épithéliales intestinales du ver. Cette cellule se multiplie, produisant de nombreuses cellules amiboïdes par Scissiparité endodyogénie. En conséquence du processus de multiplication, l'espace intercellulaire des cellules épithéliales peut devenir infecté dans plus de 10 segments du ver[9].
Entre 60 et 90 jours après l'infection, le stade de cellule sexuelle du parasite commence la sporogénèse, et deviennent des sporocystes, dont chacun contient huit triactinomyxon de spores. Ces spores sont libérées de l'anus de l'oligochaeta dans l'eau. Alternativement, un poisson peut devenir infectés en mangeant un oligochaeta porteur du parasite. Les vers infectés peuvent libérer des triactinomyxons pendant au moins un an. Les triactinomyxon sont transportés par l'eau, où ils peuvent infecter des salmonidés à travers la peau. La pénétration du poisson par ces spores ne prend que quelques secondes. Dans les cinq minutes, un sac de cellules germinales appelé sporoplasme entre dans l'épiderme du poisson, et quelques heures après, le sporoplasme se divise en cellules individuelles qui vont se répandre dans le poisson.
Dans le poisson, le parasites se reproduit à la fois intracellulairement et extracellulairement dans son cartilage par endodyogénie, c'est-à-dire que de nouvelles cellules se développent à l'intérieur des cellules âgées. L'étape finale dans le poisson est la création de la myxospore, qui est formé par la sporogonie. Elles sont libérées dans l'environnement, lorsque le poisson se décompose ou est mangé. Des recherches récentes indiquent que certains poissons peuvent expulser des myxospores viable alors qu'ils sont toujours en vie[10].
Les Myxospores sont très résistantes : il a été montré que les spores de Myxobolus cerebralis peuvent tolérer une congélation à −20 °C pendant au moins 3 mois, un vieillissement dans la boue à 13 °C pendant au moins 5 mois, et le passage à travers l'appareil digestif de brochet (Esox lucius) ou de canards colverts (Anas platyrhynchos) sans perte d'infectiosité pour les vers[11]. Les Triactinomyxons sont beaucoup plus éphémère : ils survivent 34 jours ou moins, en fonction de la température[12].
Pathologie

Les infections par M.cerebralis ont été signalées sur un large éventail d'espèces de salmonidés : huit espèces de l'Atlantique, (Salmo) ; quatre espèces du Pacifique , (Oncorhynchus) ; quatre espèces de chevalier, Salvelinus ; l'ombre, (Thymallus thymallus) ; et le huchon, (Hucho hucho)[13]. M. cerebralis cause des dommages à ses poissons hôtes par l'attachement des triactinomyxon, la migration des différentes étapes du cycle à travers les tissus et le long des nerfs, ainsi que par la digestion du cartilage. La queue des poissons peut s'assombrir, mais à côté de ces lésions du cartilage, les organes internes apparaissent généralement sains. D'autres symptômes incluent des déformations du squelette et le comportement de "tournis" qui est en fait causé par des dommages à la moelle épinière et du cerveau. Des expériences ont montré que les poissons peuvent tuer M.Myxobolus dans leur peau (éventuellement en utilisant des anticorps), mais que les poissons n'attaquent pas les parasites une fois qu'ils ont migré vers le système nerveux central. Cette réponse varie d'une espèce à l'autre.
Dans T. tubifex, la libération des triactinomyxons depuis la paroi intestinale, cause des dommages à la muqueuse du ver; ceci peut se produire des milliers de fois dans un seul ver, et est supposé à nuire à l'absorption des nutriments. Les spores sont relâchées par le ver presque exclusivement lorsque la température est comprise entre 10 °C et 15 °C, ainsi les poissons dans des eaux plus chaudes ou plus froides sont moins susceptibles d'être infectés, et les taux d'infection varient en fonction des saisons.
Sensibilité
L'espèce, la taille des poissons, l'âge, la concentration en triactinomyxon, et la température de l'eau ont une incidence sur les taux d'infection chez les poissons[14]. La maladie a le plus d'impact sur les poissons de moins de cinq mois en raison de leur squelette qui n'est pas encore ossifié. Cela rend les jeunes poissons plus sensibles aux déformations[15] et fournit à M. cerebralis plus de cartilage sur laquelle se nourrir[4]. Dans une étude sur sept espèces, l'omble de fontaine et la truite arc-en-ciel ont été lourdement touchées par M. cerebralis après deux heures d'exposition tandis que l'omble à tête plate, Quinnat, le saumon, la truite brune, et l' ombre de l'Arctique ont été moins touchés. Alors que la truite brune peut héberger le parasite, en général, elles ne montrent pas tous les symptômes. Cette espèce pourrait être l’hôte originel M. cerebralis[16]. Cette absence de symptômes chez la truite brune signifie que le parasite a été découvert seulement après l'introduction de la truites arc-en-ciel en Europe[4].
Diagnostique

Une infection clinique modérée ou forte des poissons peuvent être diagnostiqué sur la base de changements dans le comportement et l'apparence 35 à 80 jours après l'infection initiale, bien que "une blessure ou une insuffisance de l'apport alimentaire en tryptophane et en acide ascorbique puissent provoquer des signes similaires". Pour diagnostiquer de façon concluante une infection il peut être nécessaire de trouver des myxospores dans les cartilages du poisson[3]. Lors des infections graves, seul l'examen du cartilage au microscope peut être nécessaire pour trouver des spores[3]. Dans les infections moins graves, le test le plus commun consiste à la digestion du cartilage crânien avec les protéases de la pepsine et de la trypsine (pepsine-trypsine digest—PTD) avant de chercher des spores. La tête et d'autres tissus peuvent aussi être examiné à l'aide de l'histopathologie afin confirmer si l'emplacement et la morphologie des spores correspond à ce qui est connu pour M. cerebralis. Une identification sérologique des spores dans des coupes de tissus à l'aide d'un anticorps contre les spores est également possible. L'identité du parasite peut également être confirmée à l'aide de la réaction en chaîne par polymérase pour amplifier les 415 paire de base du gène arnr 18S de M. cerebralis[17]. Les poissons devraient être passé au crible à l'étape de la vie où ils sont les plus vulnérables aux parasites, avec un accent particulier sur les poissons dans les piscicultures[18].
Impact

Bien qu'à l'origine une légère épidémie sur Salmo trutta dans le centre de l'Europe et sur d'autres salmonidés dans le nord-est de l'Asie a été recensé, l'introduction de la truite arc en ciel (Oncorhynchus mykiss) a considérablement augmenté l'impact de ce parasite. N'ayant aucune immunité innée contre M. cerebralis, les truites arc-en-ciel y sont particulièrement sensibles, et peuvent donc libérer tellement de spores que même les espèces de salmonidés les plus résistantes dans la même région, tels que S. trutta, peuvent être surchargés de parasites et d'ainsi engager des taux de mortalité de 80 % - 90 %. Là où M. cerebralis s'est déjà bien établi, il a provoqué le déclin, voire la suppression de l'ensemble des cohortes de poissons[19],[20].
Impact en Europe
L'impact de M. cerebralis en Europe est quelque peu atténué parce que l'espèce est endémique de cette région, donnant aux populations de poissons natives de la région un certain degré d'immunité. La truite arc-en-ciel, l'espèces la plus sensibles à ce parasite, n'est pas originaire d'Europe. D'autre part, elles sont majoritairement élevées pour le repeuplement des eaux de pêche sportive et de l'aquaculture, où le parasite a son plus grand impact. Les méthodes d'incubation et d'élevage visant à prévenir l'infection de la truite arc-en-ciel ont connu des succès en Europe. Ces techniques consiste à couver les œufs dans des eaux sans spores et à élever les alevins jusqu'à l'ossification dans des réservoirs. Ces méthodes impliquent une attention particulière portée à la qualité des ressources d'eau pour se prémunir contre une introduction de spores au cours des échanges d'eau[21]. Les alevins sont déplacés vers des étangs de terre seulement une fois qu'ils sont considérés comme cliniquement résistant aux parasites, après l'ossification du squelette[15].
Impact en Nouvelle-Zélande
M. cerebralis a été découvert pour la première fois en Nouvelle-Zélande en 1971. Le parasite n'a été trouvé que dans les rivières de l'Ile du Sud à l'écart de la plupart des importants sites d'aquaculture. En outre, les espèces de salmonidés commercialement élevées en Nouvelle-Zélande ont une faible sensibilité à la maladie du tournis, et il n'a pas été montré que les salmonidés indigènes avaient été infectés[22]. Un important impact indirecte de la présence du parasite en Nouvelle-Zélande, est la mise en quarantaine des saumons exportés en Australie[22].
Impact aux États-Unis
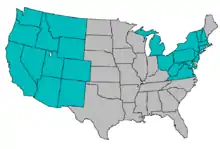
La présence de M. cerebralis a été enregistré pour la première fois en Amérique du Nord, en 1956, en Pennsylvanie, après avoir été introduit par des truites infectées importées d'Europe, et il s'est propagé de façon constante au sud et à l'ouest[23]. Jusque dans les années 1990, la maladie du tournis a été considérée comme un problème tout à fait gérable affectant la truite arc-en ciel en écloseries. Cependant, il a s'est récemment établi dans les eaux naturelles des montagnes Rocheuses (Colorado, Wyoming, Utah, Montana, Idaho, Nouveau-Mexique), où il est à l'origine d'une forte mortalité dans plusieurs rivières de pêche sportive. Certains cours d'eau dans l'ouest des États-Unis ont perdu 90 % de leurs truites[24]. En outre, la maladie du tournis menace la pêche récréative, ce qui est important pour l'industrie du tourisme, un élément clé de l'économie de certains états de l'ouest. Par exemple, The Montana Tournis Task Force estime que la pêche à la truite a engendré 300 000 000 $ de loisirs dans le Montana[4]. qui plus est, certaines des espèces de poissons que M. cerebralis infecte (Truite bull, la truite fardée, et arc-en-ciel) sont déjà menacées ou en voie de disparition, et le parasite pourrait aggraver leur situation[4]. Pour des raisons qui sont mal comprises, mais sans doute à voir avec les conditions environnementales, l'impact sur les poissons infectés a été plus grande dans le Colorado et le Montana, qu'en Californie, dans le Michigan et dans l'état de New York[25].
Impact au Canada
La maladie du tournis a été détecté pour la première fois dans les poissons du Lac Johnson dans le Parc National de Banff en . Les Laboratoires de l'ACIA l'a confirmé en août et le Parcs du Canada, a annoncé l'épidémie le [26]. Bien que le parasite ait été découvert dans le parc national Banff, ce n'est pas nécessairement de là que vient l'épidémie à l'origine. Le Gouvernement de l'Alberta est actuellement en train d'échantillonner et de tester les poissons dans 6 bassins versants différents (Rivière de la Paix, Athabasca, Saskatchewan Nord, Red Deer, Bow et Oldman) pour voir où la maladie s'est propagée. Les premiers échantillons de poissons ont été collectés en 2016, et sont actuellement en cours de traitement par le Gouvernement de l'Alberta et les laboratoires de l'ACIA. Depuis le début des essais, il a été détecté dans la partie Supérieure de la Rivière Bow[27], et en , il a été confirmé que le parasite a également été détecté dans la Rivière Oldman[28]. La déclaration ne signifie pas que chaque population de poissons sensibles au sein de la rivière Bow et Oldman est infectée par la maladie.
Prévention et contrôle
Certains biologistes ont tenté de désarmer triactinomyxon spores, en leur faisant tirer leurs filaments polaires prématurément. En laboratoire, seuls les extrêmes acidité ou basicité, modérées à fortes concentrations de sels, ou de courant électrique ont causé un largage prématuré des filaments ; les neurochimiques, les chimiotactiques de cnidaire, et du mucus de truite ont été inefficaces[29], comme l'ont été les anesthésiants ou les poissons morts[30]. Si les spores peuvent être désarmées, elles seraient incapables d'infecter les poissons, mais des recherches supplémentaires sont nécessaires afin de trouver un traitement efficace[29].
Certaines souches de poissons sont plus résistantes que d'autres, même au sein d'une même espèce[14]; utiliser ces souches résistantes pourrait aider à réduire l'incidence et la gravité de la maladie du tournis dans l'aquaculture. Il existe également des preuves indirectes que les populations de poissons peuvent développer une résistance à la maladie au fil du temps[31]. En outre, les aquaculteurs peuvent éviter les infections de M. cerebralis en n'utilisant pas des étangs mais des réservoirs artificiels pour l'élevage de jeunes poissons; ce qui les tiendrait à l'écart des vers possiblement infectés et rendrait les spores et les oligochètes plus facile à éliminer en utilisant des filtres, du chlore, ou des rayons ultraviolets[3]. Afin de minimiser les populations d’oligochète , des techniques consistent à désinfecter périodiquement les écloseries ou les étangs de pisciculture et d'élever les petites truites à l'intérieur, dans des eaux sans pathogènes. Des caniveaux en béton lisse ou en plastique maintenus propres et sans contamination de l'eau permettraient de garder saines les entreprises d'aquaculture[3].
Enfin, certains médicaments, tels que la furazolidone, furoxone, le bénomyl, la fumagilline, le proguanil et la clamoxyquine, ont montré des effets empêchant le développement des spores, ce qui réduit les taux d'infection[3]. Par exemple, une étude a montré que l'utilisation de fumagilline sur O. mykiss réduirait le nombre de poissons infectés de 73 / 100 % à 10 / 20 %[11]. Malheureusement, ce traitement est considéré comme impropre aux populations de truite sauvage[9] , et aucun traitement médicamenteux ne s'est montré efficace et approuvé par la Food and Drug Administration aux États-Unis[4].
Les loisirs et sports de pêche peuvent aider à éviter la propagation du parasite en ne transportant pas de poisson d'un plan d'eau à un autre, en ne déposant pas des os ou des entrailles de poisson, dans les plans l'eau, et de s'assurer que leurs chaussures ou leurs bottes sont propres avant de se déplacer entre les différents points d'eau. Des régulations fédéral, nationale, provinciale et locale sur l'utilisation des appâts vont être également mis en place[32].
Voir aussi
- L'anémie infectieuse du saumon (ISA) – une infection virale de saumon de l'Atlantique.
- Le pou du saumon, un autre parasite qui s'attaque au population de saumon d’élevage.
Notes
- J.L. Bartholomew et P.W. Reno, « The history and dissemination of whirling disease », American Fisheries Society Symposium, vol. 29, , p. 3–24
- « All the fish in this Banff lake are to be removed and killed to protect other lakes from whirling disease »
- M.E. Markiw, « Salmonid Whirling disease », Fish and Wildlife Leaflet, vol. 17, , p. 1–3 (lire en ligne[archive du ])
- M. A. Gilbert et W. O. Jr. Granath, « Whirling disease and salmonid fish: life cycle, biology, and disease », Journal of Parasitology, vol. 89, no 4, , p. 658–667 (PMID 14533670, DOI 10.1645/ge-82r, JSTOR 3285855)
- M. L. Kent, L. Margolis et J.O. Corliss, « The demise of a class of protists: taxonomic and nomenclatural revisions proposed for the protist phylum Myxozoa Grasse, 1970 », Canadian Journal of Zoology, vol. 72, , p. 932–937 (DOI 10.1139/z94-126)
- R. P. Hedrick et M. El-Matbouli, « Recent advances with taxonomy, life cycle, and development of Myxobolus cerebralis in the fish and oligochaete hosts », American Fisheries Society Symposium, vol. 29, , p. 45–53
- A. S. Monteiro, B. Okamura et P. W. H. Holland, « Orphan worm finds a home: Buddenbrockia is a Myxozoan », Molecular Biology and Evolution, vol. 19, no 6, , p. 968–971 (PMID 12032254, DOI 10.1093/oxfordjournals.molbev.a004155, lire en ligne[archive du ])
- (en) E. Sally Chang, Moran Neuhof, Nimrod D. Rubinstein, Arik Diamant, Hervé Philippe, Dorothée Huchon et Paulyn Cartwright, « Genomic insights into the evolutionary origin of Myxozoa within Cnidaria », Proceedings of the National Academy of Sciences, vol. 112, no 48, , p. 14912–14917 (ISSN 0027-8424, PMID 26627241, PMCID 4672818, DOI 10.1073/pnas.1511468112, lire en ligne)
- M. El-Matbouli et R.W. Hoffmann, « Light and electron microscopic studies on the chronological development of Myxobolus cerebralis to the Actinosporean stage in Tubifex Tubifes », International Journal For Parasitology, vol. 28, , p. 195–217 (DOI 10.1016/s0020-7519(97)00176-8)
- K. A. Nehring, R. B. Thompson, K. G. Taurman et D.L. Shuler, « Laboratory studies indicating that living brown trout Salmo trutta expel viable Myxobolus cerebralis myxospores », American Fisheries Society Symposium, vol. 29, , p. 125–134
- M. El-Matbouli et R.W. Hoffmann, « Effects of freezing, aging, and passage through the alimentary canal of predatory animals on the viability of Myxobolus cerebralis spores », Journal of Aquatic Animal Health, vol. 3, , p. 260–262 (DOI 10.1577/1548-8667(1991)003<0260:eofaap>2.3.co;2)
- M.E. Markiw, « Experimentally induced whirling disease. II. Determination of longevity of the infective triactinomyxon stage of Myxobolus cerebralis by vital staining », Journal of Aquatic Animal Health, vol. 4, no 1, , p. 44–47 (DOI 10.1577/1548-8667(1992)004<0044:eiwdid>2.3.co;2)
- Lom, J. & Dyková, I. (1992). Protozoan Parasites of Fishes, Elsevier, Amsterdam. (ISBN 0-444-89434-9).
- E. R. Vincent, « Relative susceptibility of various salmonids to whirling disease with emphasis on rainbow and cutthroat trout », American Fisheries Society Symposium, vol. 29, , p. 109–115
- M.M. Halliday, « The Biology of Myxosoma cerebralis: The Causative Organism of Whirling Disease of Salmonids », Journal of Fish Biology, vol. 9, , p. 339–357 (DOI 10.1111/j.1095-8649.1976.tb04683.x)
- G Hoffmann, « Whirling Disease Of Trout », U.S. Department of the Interior, Fishery Leaflet, vol. 508, , p. 1–3
- Andree, K.B.; MacConnell, E.; Hedrick, R.P. (1998). "A nested polymerase chain reaction for the detection of genomic DNA of Myxobolus cerebralis in rainbow trout Oncorhynchus mykiss". Diseases of Aquatic Organisms. 34: 145–54. doi:10.3354/dao034145.
- "5.2 Myxobolus cerebralis (Whirling Disease)" (PDF). American Fisheries Society Bluebook. Fish and Wildlife Service. 2004.
- Nehring, R.B. (1996). "Whirling Disease In Feral Trout Populations In Colorado." In E.P. Bergersen And B.A.Knoph (eds.), Proceedings: Whirling Disease Workshop––where Do We Go From Here? Colorado Cooperative Fish And Wildlife Research Unit, Fort Collins.: pp.159.
- Vincent, E.R. (1996). "Whirling Disease—the Montana Experience, Madison River." In, E.P. Bergersen And B.A.Knoph (eds.), Proceedings: Whirling Disease Workshop—where Do We Go From Here? Colorado Cooperative Fish And Wildlife Research Unit, Fort Collins.: pp.159.
- P Ghittino, « Present Status of Whirling Disease In Italian Trout Farms », Riv. It. Piscic. Ittiopat, vol. 5, , p. 89–92
- Stone M A B, MacDiarmid S C, Pharo H J. (1997). Import health risk analysis: salmonids for human consumption. Ministry of Agriculture Regulatory Authority, New Zealand.
- E.P. Bergersen et D.E. Anderson, « The distribution and spread of Myxobolus cerebralis in the United States », Fisheries, vol. 22, no 8, , p. 6–7 (DOI 10.1577/1548-8446(1997)022<0006:tdasom>2.0.co;2)
- Tennyson, J. Anacker, T. & Higgins, S. (January 13, 1997). "Scientific breakthrough helps combat trout disease." U.S. Fish and Wildlife Service Whirling Disease Foundation News Release.
- Wisconsin Department of Agriculture, Trade and Consumer Protection. Division of Animal Health. (October 2001). "Fish Health Advisory: Whirling Disease in Trout." « Archived copy » (version du 26 juin 2004 sur l'Internet Archive) (.pdf).
- Parks Canada. (2016). 'Whirling disease confirmed'
- CBC News. (2016). 'Whirling disease confirmed in Bow River, CFIA says'
- CBC News. (2017). 'Whirling disease now infects entire Oldman River basin, including Waterton Lakes National Park'
- E. J. Wagner, Q. Cannon, M. Smith, R. Hillyard et R. Arndt, « Extrusion of Polar Filaments of the Myxobolus cerebralis Triactinomyxon by salts, electricity, and other agents », American Fisheries Society Symposium, vol. 29, , p. 61–76 (lire en ligne [PDF])
- El-Matbouli, M., Hoffmann, R.W., Shoel, H., McDowell, T. S., & Hedrick, R.P. (1999)." Whirling disease: host specificity and interaction between the actinosporean stage of Myxobolus cerebralis and rainbow trout (Oncorhynchus mykiss) cartilage." Diseases of Aquatic Organisms 35: 1–12.
- Whirling Disease Foundation News. July, 2003. Research on whirling disease resistant rainbow trout « https://web.archive.org/web/20070731130533/http://www.whirling-disease.org/newsletters/wdf_newsletter2003_07.htm »(Archive • Wikiwix • Archive.is • Google • Que faire ?),
- Myxobolus cerebralis. (16 August 2012). USGS Nonindigenous Aquatic Species Database, Gainesville, FL, and NOAA Great Lakes Aquatic Nonindigenous Species Information System, Ann Arbor, MI.
Liens externes
- Report of the World Trade Organization on Australian restrictions on salmon imports
- The Whirling Disease Foundation
- The Whirling Disease Initiative
- Whirling disease maps and data
- Species Profile- Whirling Disease (Myxobolus cerebralis), National Invasive Species Information Center, United States National Agricultural Library, lists general information and resources for whirling disease
- Portail de la parasitologie
- Portail des cnidaires
- Portail de l’ichtyologie