Cyclobutène
| cyclobutène | |
  |
|
| Identification | |
|---|---|
| Nom UICPA | cyclobutène |
| No CAS | |
| No ECHA | 100.011.360 |
| No CE | 212-496-8 |
| PubChem | 69972 |
| SMILES | |
| InChI | |
| Apparence | gaz |
| Propriétés chimiques | |
| Formule | C4H6 [Isomères] |
| Masse molaire[1] | 54,0904 ± 0,0036 g/mol C 88,82 %, H 11,18 %, |
| Moment dipolaire | 0,132 ± 0,001 D [2] |
| Propriétés physiques | |
| T° ébullition | 1,5−2 °C à 972 hPa[3] |
| Masse volumique | 0,733 g·cm-3 [réf. nécessaire] |
| Propriétés électroniques | |
| 1re énergie d'ionisation | 9,43 ± 0,02 eV (gaz)[4] |
| Unités du SI et CNTP, sauf indication contraire. | |
Le cyclobutène de formule brute C4H6 est le cycloalcène le plus petit après le cyclopropène. Il est utilisé dans l'industrie chimique comme monomère dans la synthèse de polymères par polymérisation par ouverture de cycle et comme réactif dans nombre de synthèses organiques.
Synthèse
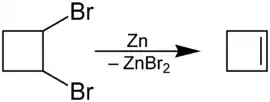
Le cyclobutène peut être obtenu par élimination sur le 1,2-dibromocyclobutane avec de la poudre de zinc (deshalogénation)[3] :
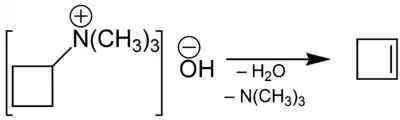
Il peut être également obtenu par une élimination de Hofmann sur l'hydroxyde de cyclobutyl,triméthyl ammonium conduite par distillation à sec[5] :
En outre, le cyclobutène peut aussi être obtenu par cyclisation photochimique du 1,3-butadiène. Cette méthode fonctionne mais elle a un mauvais rendement[6] :
Finalement, le meilleur rendement de 99,2% de pur cyclobutène est obtenu via la synthèse la plus moderne qui débute du cyclopropylcarbinol, cycloprop-CH2-OH qui est transformé par reflux avec de l'acide chlorhydrique concentré, en cyclobutanol. Celui-ci est tosylé avec le chlorure de tosyle dans la pyridine et finalement ce tosylate, traité à 70 °C avec du t-butylate de potassium, K+(CH3)3CO-, dans le DMSO, fournit le cyclobutène en quantité[7] :
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) David R. Lide, Handbook of chemistry and physics, Boca Raton, CRC, , 89e éd., 2736 p. (ISBN 978-1-4200-6679-1 et 1-4200-6679-X), p. 9-50
- R. Willstätter, J. Bruce, Zur Kenntnis der Cyclobutanreihe, Chemische Berichte, 1907, vol. 40, pp. 3979–3999.
- (en) David R. Lide, Handbook of chemistry and physics, Boca Raton, CRC, , 89e éd., 2736 p. (ISBN 978-1-4200-6679-1), p. 10-205
- Hans Beyer, Wolfgang Walter, Organische Chemie, 20e éd., Hirzel Verlag Stuttgart, 1984, p. 364. (ISBN 3-7776-0406-2).
- W. Adam, T. Oppenlaender, G. Zang, The 185-nm photochemistry of cyclobutene and bicyclo[1.1.0]butane, J. Am. Chem. Soc., 1985, vol. 107(13), pp. 3921–3924. DOI:10.1021/ja00299a028
- J. Salaün et A. Fade, Cyclobutene, Org. Synth., 1986, vol. 64, p. 50. DOI:10.15227/orgsyn.064.0050.
Articles connexes
- Portail de la chimie