Capsaïcine
La capsaïcine (8-méthyl-N-vanillyl-6-nonénamide) est un composé chimique de la famille des alcaloïdes, composant actif du piment (Capsicum). C’est un irritant de l’épithélium des cellules des mammifères ; il produit une sensation de brûlure dans la bouche, ce qui peut être considéré comme un élément gustatif intéressant. Du point de vue biologique, ce composé permet aux fruits, et donc aux graines de la plante qui les produit, d'être moins exposés à la prédation ; de plus, contrairement aux mammifères, les oiseaux ne sont pas sensibles à son effet, ce qui favorise la dispersion des graines par des agents plus mobiles[4]. La molécule est classée parmi les métabolites secondaires.
| Capsaïcine | |

| |
 |
|
| Identification | |
|---|---|
| Nom UICPA | (E)-8-méthyl-N-vanillyl-trans-6-nonénamide |
| Synonymes |
(E)-N-(4-hydroxy- |
| No CAS | |
| No ECHA | 100.006.337 |
| No CE | 206-969-8 |
| Code ATC | M02 |
| FEMA | 3404 |
| SMILES | |
| InChI | |
| Apparence | Poudre blanche, sans odeur [réf. nécessaire] |
| Propriétés chimiques | |
| Formule | C18H27NO3 [Isomères] |
| Masse molaire[1] | 305,4119 ± 0,0174 g/mol C 70,79 %, H 8,91 %, N 4,59 %, O 15,72 %, |
| Propriétés physiques | |
| T° fusion | 65 °C [2] |
| T° ébullition | 210 à 220 °C[réf. nécessaire] |
| Solubilité | Faiblement soluble dans l'eau. Soluble dans l'alcool, l'éther, le benzène, l'acétone et le chloroforme[réf. nécessaire]. |
| Point d’éclair | 112,18 °C[réf. nécessaire] |
| Précautions | |
| SIMDUT[3] | |
 D1B, D2B, |
|
| NFPA 704 | |
| Directive 67/548/EEC[réf. nécessaire] | |
 T |
|
| Transport | |
| Écotoxicologie | |
| DL50 | 47,2 mg·kg-1 (souris, oral) [2] 0,4 mg·kg-1 (souris, i.v.) [2] 9 mg·kg-1 (souris, s.c.) [2] 6,5 mg·kg-1 (souris, i.p.) [2] > 512 mg·kg-1 (souris, peau)[2] |
| Unités du SI et CNTP, sauf indication contraire. | |
Histoire
Cet alcaloïde a été découvert et isolé en 1816 par le pharmacochimiste allemand Christian Friedrich Bucholz, et fut appelé capsaïcine par L. T. Thresh[5]. En 1878, E. Hogyes, un médecin hongrois, démontra que celui-ci cause non seulement un effet d'irritation en bouche, mais aussi augmente la sécrétion de liquide gastrique. La capsaïcine fut synthétisée pour la première fois en 1930 par E. Spath et F. S. Darling. En 1958, la dihydrocapsaïcine fut découverte et nommée capsaïcine 2[6]. En 1961, d'autres alcaloïdes similaires furent isolés du piment par les chimistes japonais S. Kosuge et Y. Inagaki, qui créèrent la famille des capsaïcinoïdes[7],[8].
Capsaïcinoïdes
Il y a en fait plusieurs capsaïcinoïdes, qui sont présents en différentes quantités dans le piment rouge. La capsaïcine est le composé majoritaire du piment rouge avec la dihydrocapsaïcine. Ces deux composés sont deux fois plus puissants en goût que les autres capsaïcinoïdes (nordihydrocapsaïcine, homodihydrocapsaïcine et homocapsaïcine). Ces capsaïcinoïdes, qui sont présents en différentes quantités dans différentes espèces de capsicum, ont des profils temporels irritants différents[8],[9]. Cela compte pour l’action retard de C. chinense (habanero) comparé aux autres espèces.
Les capsaïcinoïdes ont la caractéristique d'activer les récepteurs de chaleurs de la peau, d'où la sensation de brûlure, alors qu'il n'y a pas d'augmentation de température.
| Capsaïcinoïde | Concentration typique[9] | Échelle de Scoville | Structure chimique |
|---|---|---|---|
| Capsaïcine (8-méthyl-N-vanillyl-6-nonénamide) |
69 % | 15 000 000 à 16 000 000[10] |
 |
| Dihydrocapsaïcine (8-Méthyl-N-vanillylnonamide) | 22 % | 15 000 000 |  |
| Nordihydrocapsaïcine (7-Méthyl-N-vanillyloctamide) | 7 % | 9 100 000 |  |
| Homodihydrocapsaïcine (9-Méthyl-N-vanillyldécamide) | 1 % | 8 600 000 |  |
| Homocapsaïcine (trans-9-Méthyl-N-vanillyl-7-décénamide) | 1 % | 8 600 000 | 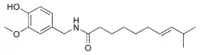 |
Utilisation
Nourriture
À cause de la sensation de brûlure, la capsaïcine est couramment utilisée dans les produits alimentaires pour ajouter de l’épicé ou « pseudo-chaleur » (piquant). Le degré de chaleur (SHU) est mesuré par l’échelle de Scoville. La capsaïcine est le composé le plus irritant (15 000 000 SHU), comparé à la pipérine (piquant du poivre) et au [6]-gingerol le principe piquant du gingembre.
Typiquement, la capsaïcine est obtenue en utilisant du piment, ce qui est préférable pour des raisons de sécurité à la capsaïcine pure. Elle est soluble dans le gras plutôt que dans l’eau, ce qui explique que boire un verre d’eau apporte peu de soulagement tandis que le lait, le beurre ou des crèmes glacées sont efficaces.
La capsaïcine est également utilisée dans les boissons appelées «alcools sans alcool» ou «liqueurs sans alcool». La première personne qui a utilisé cette méthode était Reynald Vito Grattagliano, un inventeur qui a travaillé sur un projet de spiritueux sans alcool de 2007 à 2011 offrant aux consommateurs une alternative[13].
Médical
La capsaïcine est utilisée dans des crèmes locales pour soulager la douleur nerveuse périphérique et même certains prurits (démangeaisons) violents. Le traitement typique implique parfois l’application d’un anesthésiant jusqu’à ce que la zone soit engourdie. Ensuite, la capsaïcine est placée par un thérapeute portant des gants de caoutchouc et une protection sur le visage. Le patch à la capsaïcine reste sur la peau pendant une heure (30 minutes sur les pieds) avant d'être retiré (Patchs Qutenza à 8 % de capsaïcine). On peut utiliser des poches de glace ou des sacs réfrigérants pendant l'application afin de limiter la sensation douloureuse de brûlure. Les nerfs pourraient être dominés par la sensation de brûlure et ne pourraient plus communiquer la douleur pendant une longue période. La capsaïcine stimulant (et désensibilisant ensuite) surtout les récepteurs TRPV1, lesquels réagissent d'ordinaire à une température d'environ 45 °C, la chaleur de l'aliment doit donc faire monter la température des cellules au-delà de 52 °C, pour que les récepteurs TRPV2, insensibles à la capsaïcine, puissent relayer le signal.
Les pommades et bains pour le soulagement des muscles douloureux contiennent souvent de la capsaïcine sous la forme d’un extrait huileux listé parmi les ingrédients sous des noms comme « oléorésine de capsicum ».
Dans le domaine ORL il est montré que la capsaïcine en spray nasal entraîne une diminution significative et à long terme des symptômes de la rhinite perannuelle non allergique et non infectieuse[14].
La capsaïcine inhibe la croissance d'Helicobacter pylori[15].
La capsaïcine contribue à bloquer le cancer de certaines cellules du poumon ou de la prostate par apoptose[16].
La capsaïcine est notamment utilisé dans le médicament Zostrix pour soulager des prurits violents, les douleurs arthritiques et certaines douleurs neuropathiques chroniques[17],[18].
Arme non létale
La capsaïcine est aussi l’ingrédient actif dans le vaporisateur de gaz poivre pour contrôler les émeutes. Les gouttelettes provoquent une douleur vive en contact avec la peau, en particulier celle des yeux ou d’une membrane muqueuse. Se référer à l’échelle de Scoville pour la comparaison avec les autres sources de capsaïcine.
Une société commerciale, Guardian-angel, a mis au point un petit pistolet de défense contenant deux cartouches de capsaïcine.
En grande quantité, la capsaïcine peut être un poison mortel. Les symptômes d’une dose excessive comprennent la difficulté de respirer, la cyanose et les convulsions[19]. Bien que la grande quantité nécessaire pour tuer un adulte humain et la faible concentration dans les piments rendent un empoisonnement accidentel très peu probable, la capsaïcine a été impliquée dans certains cas d’infanticide[20],[21],[22],[23].
Dopage
La capsaïcine peut être utilisée en applications sur les jambes des chevaux, sous forme de pommade ou de lotion. Chez l'homme, elle a des propriétés antidouleur (l'application est douloureuse, l'effet antidouleur survient un ou plusieurs jours après), mais elle provoque une sensation de brûlure chez les chevaux. Leurs jambes sont alors plus sensibles et ils ont tendance à sauter plus haut pour éviter de heurter les obstacles. Cette pratique est formellement interdite en compétition et la capsaïcine est un produit interdit par la Fédération équestre internationale [24].
Mécanisme d’action
Les sensations de brûlures et les douleurs associées à la capsaïcine résultent de l'activation des neurones sensoriels des bourgeons gustatifs. La capsaïcine se lie au récepteur membranaire vanilloïde sous-type 1 (TRPV1). Ceci induit une dépolarisation de la membrane plasmique par entrée calcique et sodique.
La capsaïcine active le TRPV1 car elle est un analogue structurel des métabolites d’acides linoléiques oxydés (en anglais, oxydized linoleic acid metabolites d'où l'acronyme OLAM), substance endogène synthétisée lors de brûlures.
Régimes
La consommation de capsaïcine stimule la production de deux hormones, l'adrénaline et la noradrénaline. En 2014, une méta-analyse retrouvait un possible effet sur la réduction de poids par une réduction de la prise de calories durant le repas suivant la prise de 2 mg de capsaïcine[25], cependant, les études analysées sont hétérogènes et de faible niveau de preuve.
Autres effets
Euphorie
La consommation d’une grande quantité de capsaïcine provoque l’émission d’endorphines et une sensation de plaisir ou une « euphorie »[26].
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Capsaïcine », sur ChemIDplus, consulté le 9 février 2009
- « Capsaïcine » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 24 avril 2009
- (en) J. J. Tewksbury et G. P. Nabhan, « Directed deterrence by capsaicin in chilies », Nature, vol. 412, no 6845, , p. 403–404 (DOI 10.1038/35086653).
- (en) J. King, H. Wickes Felter, J. Uri Lloyd (1905) A King's American Dispensatory. Eclectic Medical Publications (ISBN 1888483024)
- (ja) S. Kosuge, Y. Inagaki et K. Uehara. (1958) Chemical Constitution of the Pungent Principles. Nippon Nogei Kagaku Kaishi (J. Agric. Chem. Soc.), 32, 578-581.
- (ja) S. Kosuge, Y. Inagaki, H. Okumura (1961). Studies on the pungent principles of red pepper. Part VIII. On the chemical constitutions of the pungent principles. Nippon Nogei Kagaku Kaishi (J. Agric. Chem. Soc.), 35, 923-927. (en) Chem. Abstr. 1964, 60, 9827g.
- (ja) S. Kosuge, Y. Inagaki (1962) Studies on the pungent principles of red pepper. Part XI. Determination and contents of the two pungent principles. Nippon Nogei Kagaku Kaishi (J. Agric. Chem. Soc.), 36, p. 251
- (en) DJ Bennett and GW Kirby (1968) Constitution and biosynthesis of capsaicin. Journal of Chemical Society, 442-446.
- (en) MA Cliff and H Heymann (1992) Time–intensity evaluation of oral burn. J. Sens. Stud., 8, 201–211. DOI:10.1111/j.1745-459X.1992.tb00195.x
- (en) S Narasimhan and VS Govindarajan (1978) Evaluation of spices and oleoresin-VI-pungency of ginger components, gingerols and shogoals and quality. International Journal of Food Science & Technology 13 (1), 1–36. DOI:10.1111/j.1365-2621.1978.tb00773.x
- (en) VS Govindarajan, S Narasimhan, B Rajalakshmi and D Rajalakshmi (1980) Evaluation of spices and oleoresins - Correlation of pungency stimuli and pungency in ginger. Zeitschrift für Lebensmitteluntersuchung und -Forschung A, Volume 170(3), p. 200-203 DOI:10.1007/BF01042540
- (en) « An American Self Made Scientist Has Invented a Drink That Eliminates Hangovers », sur Digital Journal
- Se pimenter le nez pour manger mieux ?
- « Capsaicin as an inhibitor of the growth of the gastric pathogen Helicobacter pylori »(en)
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4811481/
- « Les autres crèmes anesthésiantes - www.pharmasante.org », www.pharmasante.org, (lire en ligne, consulté le )
- « ZOSTRIX : la fiche complète », sur Ooreka.fr (consulté le )
- « La capsaïcine à haute concentration », sur neurologies.fr, (2011)
- Tara Brady, « Woman 'killed boyfriend's two-year-old daughter by force feeding her chilli as a punishment' », sur Mail Online, (consulté le )
- (en) Colin Schultz, « Too Much Chili Powder Or Black Pepper Can Kill Kids », sur Smithsonian Magazine (consulté le )
- « Two-Year-Old Girl Dies From Eating A Hot Chili Pepper », sur www.inquisitr.com (consulté le )
- (en) « Why You Should Never, Ever Eat The World's Hottest Pepper », sur HuffPost, (consulté le )
- (en) FEI, « 2021 Equine Prohibited Substances List », sur https://inside.fei.org, (consulté le )
- S Whiting, EJ Derbyshire et B Tiwari, « Could capsaicinoids help to support weight management? A systematic review and meta-analysis of energy intake data. », Appetite, vol. 73, , p. 183–8 (PMID 24246368, DOI 10.1016/j.appet.2013.11.005)
- Uma Sharma, Alyssa Pagano, « What happens to your brain and body when you eat a hot pepper », sur Business Insider (consulté le )
- (en) Xiaochi SuZhuang YangKok Bing Tan, « Preparation and characterization of ethyl cellulose film modified with capsaicin », Carbohydrate Polymers, (DOI 10.1016/j.carbpol.2020.116259, lire en ligne)
- (en) Yann Blake, Daubresse-Chasle Gwendal et Loïc Emmanuel, « Alleviating methods of the irritant effects of Capsaicin on humans and investigation of the efficiency of its other effects : antioxidant and insecticide. », ResearchGate, (lire en ligne)
Voir aussi
Articles connexes
Liens externes
- (en) Compound Display 9083 NCBI database
- (en) COMPOUND: C06866 www.Genome.net
- Portail de la chimie
- Portail des Solanaceae
- Portail des épices et aromates

