Toxoplasma gondii
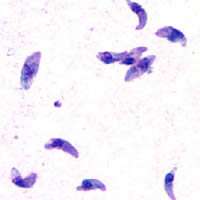
Toxoplasma gondii est un protozoaire intracellulaire appartenant au phylum des Apicomplexa, et il est l'agent de la toxoplasmose. Le phylum des Apicomplexa inclut de nombreux autres pathogènes d'importance médicale ou vétérinaire, parmi lesquels Plasmodium falciparum, responsable de la malaria chez l'humain.
| Domaine | Eukaryota |
|---|---|
| Règne | Chromalveolata |
| Division | Alveolata |
| Embranchement | Apicomplexa |
| Classe | Conoidasida |
| Ordre | Eucoccidiorida |
| Sous-ordre | Eimeriorina |
| Famille | Sarcocystidae |
| Genre | Toxoplasma |
Nom binominal
Les Apicomplexa sont des parasites intracellulaires obligatoires : ils doivent vivre à l'intérieur d'une cellule pour survivre. Une fois le parasite installé dans la cellule-hôte, celle-ci lui assure de larges ressources en nutriments ainsi qu'une protection contre le système immunitaire de l'hôte.
Historique
Les données sur le toxoplasme et son épidémiologie ont été acquises très progressivement : le parasite a d'abord été découvert uniquement sous sa forme infectieuse dans les tissus d'un rongeur sauvage, le gundi ( Ctenodactylus gundii), en Tunisie par Nicolle et Manceaux en 1908[1] et presque simultanément au Brésil chez un lapin par Splendore en 1909[3]. Au début Nicolle et Manceaux pensaient avoir affaire à un parasite du genre Leishmania, qu'ils nommèrent "Leishmania gondii", mais un an plus tard, en 1909[2], ils le nommèrent Toxoplasma gondii à cause de sa forme arquée (du grec τοx(ο) = arc) et à partir du nom du rongeur chez qui il avait été observé. Toutes notions concernant son cycle biologique ou son importance en parasitologie humaine sont alors inconnues. Il faut attendre les années 1920-1930 pour voir apparaître les premières descriptions de toxoplasmose humaine. C'est la mise au point des premiers tests sérologiques dans les années 1940 qui a permis de révéler l'importance de la prévalence de la toxoplasmose humaine. La compréhension du cycle de ce parasite et des modes de transmission n'a eu lieu qu'au cours des années 1970[4].
Un parasite intracellulaire obligatoire
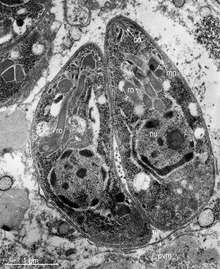
T. gondii est constitué d'une cellule polarisée de forme arquée, d'environ 8 micromètres de long par 3 micromètres de large. T. gondii est un eucaryote unicellulaire haploïde, qui présente certaines caractéristiques conservées chez tous les eucaryotes, mais également des organites spécifiques de son groupe, les Alveolata, ou de son phylum, les Apicomplexa.
T. gondii est autonome pour la plupart de ses besoins de synthèse et de transport de protéines, de lipides ou d'énergie (sous forme d'ATP). Cependant sa prolifération est obligatoirement intracellulaire car il dépend de la cellule-hôte pour un certain nombre de nutriments essentiels pour lesquels il ne dispose pas de voie métabolique propre. Comme toute cellule eucaryote, T. gondii possède toute la machinerie nécessaire à la synthèse et au transport de protéines. Ceci comprend un noyau, un réticulum endoplasmique (ER) périnucléaire, un appareil de Golgi réticulé ainsi qu’un appareil mitochondrial. Cependant, certains acides aminés, briques élémentaires des protéines, doivent être importés à partir de la cellule-hôte. T. gondii synthétise également la plupart de ses lipides ainsi que des ribonucléotides tels que l’ATP, à partir de petites molécules (précurseurs lipidiques, bases azotées) importées du cytoplasme de la cellule-hôte[6]. Cependant T. gondii n’a pas les enzymes nécessaires à la synthèse des stérols (en particulier le cholestérol) et de la choline, il doit donc importer ces lipides intacts de la cellule-hôte [7]. Les mécanismes d’import de ces différentes molécules ne sont pas tous encore bien identifiés.
Le cycle vital de T. gondii
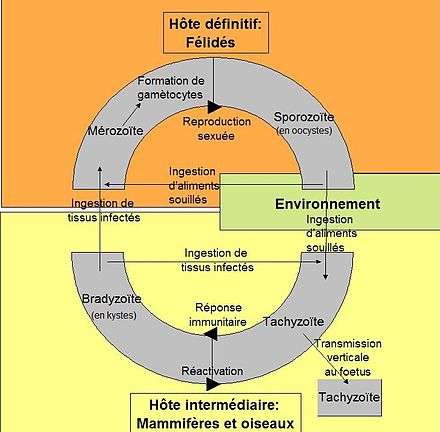
T. gondii ne peut se multiplier de manière sexuée que chez les Félidés, qui constituent ainsi ses hôtes définitifs, bien qu’il puisse infecter tous les animaux homéothermes, dénommés hôtes intermédiaires. Le toxoplasme a un cycle complexe qui implique la transmission entre hôtes par des stades spécialisés pour l’invasion (voir Figure) :
- le stade tachyzoïte, forme proliférative infectieuse chez l’hôte intermédiaire, se développe dans des vacuoles transitoires qui peuvent contenir jusqu’à 128 parasites ; cette forme peut se retrouver aussi chez le fœtus ;
- le stade bradyzoïte, chez l’hôte intermédiaire, est contenu dans des kystes intracellulaires qui mesurent environ 100µm de diamètre et contiennent plusieurs milliers de parasites ;
- le stade mérozoïte, chez l’hôte définitif, est le seul stade capable de reproduction sexuée ;
- le stade sporozoïte, résultat de la reproduction sexuée chez l’hôte définitif, est libéré dans l’environnement avec les déjections du chat dans des oocystes de 10 à 15 μm de diamètre qui contiennent huit sporozoïtes.
Les stades sporozoïte et bradyzoïte correspondent à des formes de résistance et de dissémination du parasite car les kystes et les oocystes protègent, dans une certaine mesure, les parasites qu’ils contiennent des variations de température, de pH, etc. T. gondii peut alterner entre ces stades en fonction de son hôte et de son contexte, par un processus de différenciation.
Une infection par Toxoplasma gondii peut modifier le comportement des hôtes intermédiaires. En effet, en 2011, il a été démontré que des rats infectés montraient des signes d'excitation sexuelle après avoir reniflé de l'urine de chat au lieu des signes de peur détectés chez les individus sains. Ainsi, les rats infectés ont tendance à rechercher la présence de chats au lieu de la fuir (ces derniers étant des prédateurs), ce qui favorise la transmission du parasite à l'hôte définitif[8]. De même, une étude publiée en février 2016 montre que cette manipulation parasitaire affecte également les chimpanzés, qui acquièrent suite à l'infection une attirance à l'égard de l'urine du léopard, prédateur naturel et hôte définitif de T. gondii. Cette étude amène à repenser les différences de comportement observées chez les humains porteurs du parasite.
Toxoplasmose
Contamination
Les oocystes sont présents sur des plantes ou de la terre souillée par des déjections de Félidés. De là, ils peuvent passer sur les aliments, sur les mains ou dans l'eau consommée, puis être ingérés. Les kystes sont également une source de contamination, car ils sont présents dans la viande de nombreux animaux (ovins et caprins en particulier). Cependant une cuisson adaptée de la viande évite cette contamination, en tuant les parasites enkystés. Enfin la transmission de T. gondii peut se produire de la mère au fœtus, si la mère subit la première infection au cours de sa grossesse.
Chez l'hôte intermédiaire (y compris l'homme), les kystes ou oocystes ingérés se rompent en passant dans le tube digestif et libèrent des parasites qui se redifférencient en tachyzoïtes. Ceux-ci envahissent les cellules et s'y multiplient rapidement, en particulier dans les macrophages, déclenchant une phase sanguine de dissémination; l'hôte développe la toxoplasmose. Les cellules envahies sont lysées après un certain nombre de cycles de réplication, relâchant des parasites qui réenvahissent de nouvelles cellules. La réponse immunitaire de l'hôte restreint ensuite la dissémination des tachyzoïtes mais le parasite persiste à vie, sous forme latente, enkysté dans les cellules où la réponse immunitaire est la plus faible (cellules nerveuses, rétiniennes et musculaires).
Le 28 juin 2018, l'Institute for Advanced Biosciences publie dans la revue Cell Host & Microbe sa découverte sur le mécanisme déployé par le parasite toxoplasma gondii afin de rentrer dans une cellule. L'étude révèle que le parasite injecte dans la membrane plasmique d'une cellule, un complexe de protéines capable de former une porte par laquelle il s'engouffre. Toxoplasma gondii va alors pouvoir s'isoler dans la vacuole ainsi créée en faisant une rotation sur lui même qui provoque l'obturation du sas d'entrée. Le parasite peut alors se développer à l'abri[9].
Prévalence et pathogénicité
La toxoplasmose est une des parasitoses les plus répandues : un tiers de la population mondiale est infecté par Toxoplasma gondii[10]. Sa prévalence chez l’être humain est variable. Pour les adultes présentant une séropositivité au toxoplasme (et donc une immunité à une réinfection), la prévalence est faible en Asie ou en Amérique[11],[12], elle est inférieure à 30 % dans les pays scandinaves et au Royaume-Uni, elle va de 20 à 50 % en Europe du Sud ainsi que dans les régions humides de l’Afrique et elle va de 50 à 70 % en Europe de l’Ouest[13].
La toxoplasmose est habituellement bénigne et passe inaperçue, mais c’est une affection redoutable chez les sujets fragiles, dont la réponse immunitaire ne peut pas endiguer la dissémination des parasites[14]. La gravité de cette infection est liée, d’une part, au risque de transmission fœtale du parasite en cas de contamination en cours de grossesse, et d’autre part, au risque différé de réactivation d’une infection antérieurement acquise, sous l’effet d’une immunodépression. Le manque de vaccins ou de traitement éradiquant l’infection en fait l’une des priorités des programmes de veille sanitaire[15].
Une seule espèce mais des souches de virulence variable
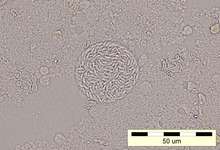
Bien qu’une seule espèce, T. gondii, soit décrite au sein du genre Toxoplasma, plus de 200 isolats ou souches ont bénéficié à ce jour d’analyses génotypiques. La pathogénicité des souches est définie par l’étude de la virulence chez la souris : détermination des DL50 et DL100, doses de parasites minimales entraînant la mort de 50 % ou de 100 % des souris infectées. La plupart des isolats analysés (95 %) sont généralement regroupés en trois génotypes principaux (types I, II et III) en fonction de leur virulence[17]. Ces souches diffèrent très peu génétiquement (moins de 1 %). Le génotype I est très virulent (ex. : la souche RH) : la DL100 est de un ou deux parasites. Les génotypes II (ex. : la souche Prugniaud) et III (ex. : la souche C) sont avirulents ou de virulence intermédiaire (DL50 = 10 000 parasites). La souche RH, une des plus utilisées dans les programmes de recherche sur ce parasite, a été isolée par Sabin en 1941, à partir d’un cas d’encéphalite humaine aiguë[18]. C’est l’une des souches les plus virulentes mais aussi des mieux caractérisées : une souris infectée par un parasite meurt en moins de 15 jours[19].
Notes et références
- C. Nicolle, L. Manceaux, « Sur une infection à corps de Leishman (ou organismes voisins) du gundi », Comptes Rendus de l'Académie des Sciences, vol. 147, , p. 763–766
- C. Nicolle, L. Manceaux, « Sur un Protozoaire nouveau du Gondi », Comptes Rendus de l'Académie des Sciences, vol. 148, , p. 369-372
- A. Splendore, « Sur un nouveau protozoaire du lapin, 2e note préliminaire », Bull Soc Path Exot, vol. 2, , p. 462
- (en) J. P. Dubey, J. K. Frenkel, « Experimental toxoplasma infection in mice with strains producing oocysts », J Parasitol, vol. 59, , p. 505–512
- (en) Jacques Rigoulet, Alain Hennache, Pierre Lagourette, Catherine George, Loïc Longeart, Jean-Loïc Le Net et Jitender P. Dubey, « Toxoplasmosis in a bar-shouldered dove (Geopelia humeralis) from the Zoo of Clères, France », Parasite, vol. 21, , p. 62 (ISSN 1776-1042, PMID 25407506, DOI 10.1051/parasite/2014062)
- (en) Audra J Charron, L. David Sibley, « Host cells: mobilizable lipid resources for the intracellular parasite T. gondii », J Cell Sci, vol. 115, , p. 3049–3059
- (en) I. Coppens, A. P. Sinai, K. A. Joiner, « T. gondii exploits host low-density lipoprotein receptor-mediated endocytosis for cholesterol acquisition », J Cell Biol, vol. 149, , p. 167–180
- (en) House PK, Vyas A, Sapolsky R. (2011) « Predator Cat Odors Activate Sexual Arousal Pathways in Brains of Toxoplasma gondii Infected Rats » PLoS ONE 6(8): e23277.
- « Toxoplasmose : des chercheurs grenoblois ont découvert comment le parasite pénètre dans les cellules », sur placegrenet.fr, (consulté le 24 juillet 2018)
- (en) J. Montoya, O. Liesenfeld, « Toxoplasmosis », Lancet, vol. 363, no 9425, , p. 1965-1976 (PMID 15194258)
- (en) G. McQuillan, D. Kruszon-Moran, B. Kottiri, L. Curtin, J. Lucas, R. Kington, « Racial and ethnic differences in the seroprevalence of 6 infectious diseases in the United States: data from NHANES III, 1988-1994 », Am. J. Public Health, vol. 94, no 11, , p. 1952-1958 (PMID 15514236)
- (en) Jones J, Kruszon-Moran D, Wilson M, « Toxoplasma gondii infection in the United States, 1999-2000 », Emerg Infect Dis, vol. 9, no 11, , p. 1371-1374 (PMID 14718078, lire en ligne)
- [PDF] Diagnosis of Strongyloides infections. A.M. Polderman, J. Blotkamp et J.J. Verweij, Ned. Tijdschr. Klin. Chem., 1999, 24, p. 60-65.
- (en) Pignanelli S., « Laboratory diagnosis of Toxoplasma gondii infection with direct and indirect diagnostic techniques », Indian J Pathol Microbiol, vol. 54, no 4, , p. 786-9.
- Rapport du groupe de travail « T. gondii » de l'Afssa, « https://www.anses.fr/fr/system/files/MIC-Ra-Toxoplasmose.pdf »(Archive • Wikiwix • Archive.is • Google • Que faire ?), (consulté le 13 septembre 2017)
- (en) Costache CA, Colosi HA, Blaga L, Györke A, Pastiu AI, Colosi IA & Ajzenberg D. « Premier isolement avec caractérisation génétique d’une souche de Toxoplasma gondii en Roumanie, à partir d’un cas humain symptomatique de toxoplasmose congénitale (First isolation and genetic characterization of a Toxoplasma gondii strain from a symptomatic human case of congenital toxoplasmosis in Romania) » Parasite 2013;20(11). DOI:10.1051/parasite/2013011
- (en) D. K. Howe, L. D. Sibley, « T. gondii comprises three clonal lineages: correlation of parasite genotype with human disease », J Infect Dis, vol. 172, , p. 1561–6
- (en) A.B. Sabin, « Toxoplasmic encephalitis in children », J Am Med Assoc, vol. 116, , p. 801–7
- (en) D. K. Howe, B. C. Summers, L. D. Sibley, « Acute virulence in mice is associated with markers on chromosome VIII in T. gondii », Infect Immun, vol. 64, , p. 5193–8
Voir aussi
Bibliographie
- Joanna Kubar, Un parasite à la conquête du cerveau. Le toxoplasme, EDP Sciences, 2017 (ISBN 978-2759819324)
Liens externes
- (en) Référence NCBI : Toxoplasma gondii
- ToxoDataBase : http://www.toxodb.org
- (en) Toxoplasmosis - Recent advances, Open access book published in September 2012
- Portail de la médecine
- Portail de la biologie cellulaire et moléculaire
- Portail de la parasitologie