Propylène glycol
Le propylène glycol (PG) ou propane-1,2-diol appelé aussi 1,2-dihydroxypropane, méthyl glycol est un diol utilisé dans de nombreux usages industriels et pharmaceutiques ou agropharmaceutiques (solvant de pesticides), à faible dose comme additif alimentaire et depuis peu dans les cigarettes électroniques (liquide à vapoter). Il est issu à faible coût de la carbochimie, et généralement de la pétrochimie.
| Propylène glycol | |
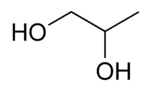 | |
  |
|
| Identification | |
|---|---|
| Nom UICPA | Propane-1,2-diol |
| Synonymes |
propane-1,2-diol |
| No CAS | (racémique) (S+) (R-) |
| No ECHA | 100.000.307 |
| No EC | 200-338-0 |
| PubChem | 1030 |
| No E | E1520 |
| FEMA | 2940 |
| SMILES | |
| InChI | |
| Apparence | liquide incolore, inodore, hygroscopique, visqueux[1]. |
| Propriétés chimiques | |
| Formule brute | C3H8O2 [Isomères] |
| Masse molaire[2] | 76,0944 ± 0,0036 g/mol C 47,35 %, H 10,6 %, O 42,05 %, |
| pKa | 14,8 (25 °C)[3] |
| Moment dipolaire | 2,25 D [4] |
| Diamètre moléculaire | 0,533 nm [4] |
| Propriétés physiques | |
| T° fusion | −59 °C[1] |
| T° ébullition | 188,2 °C[1] |
| Solubilité | Soluble dans l'éther[3]. Insoluble dans les huiles |
| Paramètre de solubilité δ | 25,8 J1/2·cm-3/2 (≤20 °C)[4] |
| Miscibilité | Miscible à l'eau[3], l'acétone[3], le chloroforme[3], l'alcool. |
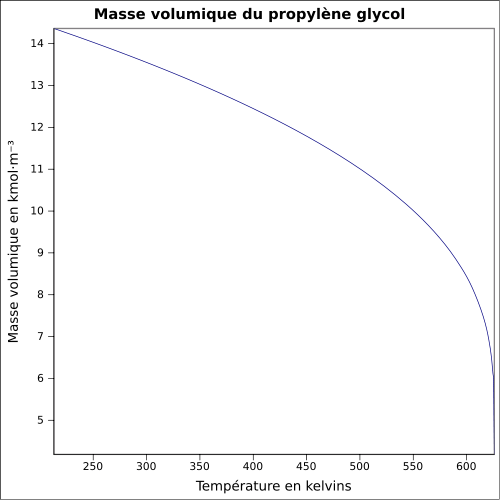
| Masse volumique | 1,036 g·cm-3 (25 °C)[3]
|
| T° d'auto-inflammation | 371 °C[1] |
| Point d’éclair | 99 °C (coupelle fermée); 107 °C (coupelle ouverte)[1] |
| Limites d’explosivité dans l’air | 2,6–12,6 %vol[1] |
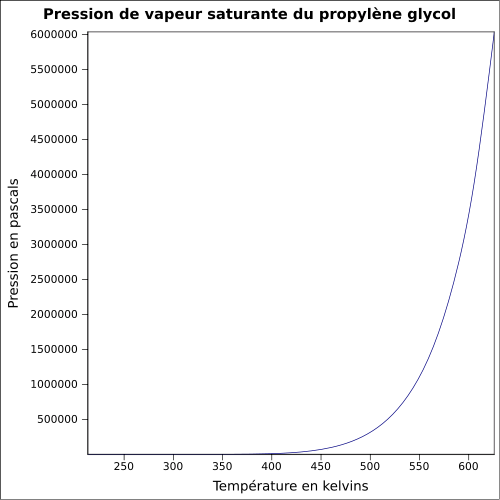
| Pression de vapeur saturante | à 20 °C : 10,6 Pa[1]
|
| Viscosité dynamique | 0,581 poise (20 °C)[3] |
| Thermochimie | |
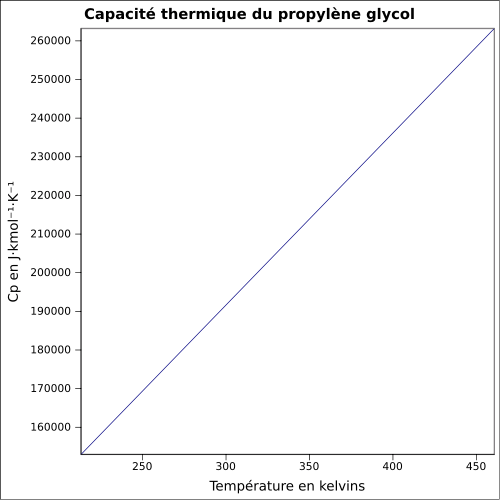
| Cp | |
| Propriétés optiques | |
| Indice de réfraction | 1,4314 [4] |
| Précautions | |
| SIMDUT[7] | |
Produit non contrôlé |
|
| NFPA 704 | |
| Directive 67/548/EEC | |
 Xi Phrases S : 24/25, |
|
| Écotoxicologie | |
| DL50 | 10 à 30 g·kg-1[8] |
| Autre | S'enflamme au contact de KMnO4 après 40 secondes. |
| LogP | -0,92[1] |
| Données pharmacocinétiques | |
| Métabolisme | Oxydé dans le foie en acide lactique puis acide pyruvique[8] |
| Demi-vie d’élim. | 4 heures[8] |
| Composés apparentés | |
| Isomère(s) | Propane-1,3-diol |
| Unités du SI et CNTP, sauf indication contraire. | |
Le propylène-glycol est obtenu à partir de la réaction de l'oxyde de propylène avec l'eau pour former du monopropylène glycol (MPG), les réactions ultérieures produisant des di-(DPG), tri-(TPG) et autres propylène-glycols.
Stéréochimie
L'atome de carbone 2 est chiral. Le propane-1,2-diol se présente donc sous la forme d'une paire d'énantiomère, l'énantiomère R étant lévogyre tandis que le S est dextrogyre. Le propylène glycol est le plus souvent un racémique.
Utilisations
Le propylène glycol a beaucoup d'applications industrielles, médicales, cosmétiques et domestiques, presque toujours en tant que solvant organique permettant de rendre miscibles dans l'eau des molécules organiques.
C'est un produit abondamment utilisé, notamment dans les domaines suivants :
- L'industrie alimentaire l'utilise à faibles doses comme émulsifiant (E1520), dans les plats préparés (sauces et assaisonnements) et/ou comme solvant de certains arômes dans certains arômes liquides.
- Dans les cigarettes électroniques, en tant que liquide de remplissage dans lequel sont éventuellement ajoutés glycérol, arômes et nicotine, afin de produire un aérosol simulant la fumée du tabac.
- L'industrie pharmaceutique et les médecins l'utilisent également : il compte par exemple pour 40 % de la composition d'un médicament à base de phénytoïne (Dilantin).
- L'Industrie cosmétique en fait un humectant anti-moisissure dans certains cosmétiques, tout comme l'industrie du tabac. Il remplace souvent la glycérine comme excipient, et parfois abusivement présenté comme hydratant (tout comme la glycérine, qui ne peut que freiner une éventuelle déshydratation par la peau).
- L'industrie textile le mobilise pour la fabrication de certaines fibres (polyester).
- En élevage, il est donné oralement aux vaches laitières en tant que précurseur du glucose pour éviter l'acétonémie en début de lactation.
- L'Industrie du spectacle (discothèque, théâtre, cinéma, plateaux de TV) l'utilisent pour alimenter les machines à fumées : son évaporation permet de produire un aérosol réputé non toxique[9] et permettant des effets spéciaux (fausses vapeurs, brumes artificielles, matérialisation des rayons laser ou lumineux...), a priori sans danger pour les acteurs ou les spectateurs.
- L'Industrie aéronautique, l'aviation civile ou militaire l'utilisent (en aspersion sur les ailes des avions afin d'y réduire la formation de glace : le givre est à l'origine d'environ 10 % des accidents d'avions [10]). Et l'industrie des systèmes de climatisation/chauffage l'utilise parfois comme antigel non-corrosif et améliorant les transferts de chaleur[11] dans les circuits et applications sensibles (ex. : compresseurs de gaz de pompes à chaleur, capteurs solaires, chambres froides alimentaires…) où il remplace l'éthylène glycol, moins coûteux mais toxique pour l'Homme et l'environnement.
- Il permet de produire des solutions de nanoparticules sans qu'elles ne s'agglomèrent[12] (avec un risque toxicologique et écotoxicologique alors renforcé par une bioassimilabilité plus importante de ces nanoparticules).
Production biologique
En plus des modes de production issus de l'industrie chimique, on note l'existence d'une filière biologique portée en France par l'entreprise Metabolic Explorer basée à Clermont-Ferrand et offrant un avantage économique significatif par rapport aux procédés pétrochimiques classiques[13].
Elle s'est alliée en Europe avec le géant Finlandais UPM (CA de 10 Milliards € et 20 000 salariés) pour construire une unité de production de MPG biosourcée et écologique présentant une alternative sérieuse aux procédés chimiques[14].
Il s'agit d'un marché très important valorisé à plus de 3 Milliards € et en forte progression[15].
Toxicologie
Voie orale
Le propylène-glycol est principalement absorbé par voie digestive. Il est oxydé dans le foie en acide lactique, puis en acide pyruvique, qui est utilisé par le corps humain comme source d'énergie. Chez l'être humain il est éliminé du sang avec une demi-vie de deux heures et de l'organisme avec une demi-vie de quatre heures [8].
L'ingestion par des volontaires d'une forte dose de propylène-glycol n'a pas mis en évidence d'effet métabolique ou biologique patent, en dehors d'un effet sédatif isolé [8],[3].
Des effets toxiques et/ou neurotoxiques (reins, système nerveux central) existent à très hautes doses. Cependant, au vu des faibles concentrations dans les produits alimentaires, il paraît impossible d'atteindre ces doses [16]. Les cas d'intoxication au propylène glycol sont plus généralement liés à une administration intraveineuse ou à l'ingestion accidentelle de grandes quantités par des enfants [17],[18].
Le potentiel de toxicité à long terme apparaît également faible. Lors d'une étude faite en 1972, aucun effet nocif apparent n'a été constaté sur des rats ayant ingéré durant 104 semaines des aliments contenant jusqu'à 5 % de PG[19].
Voie cutanée
Le contact prolongé avec la peau n'est pas ou peu irritant[20]. On constate une irritation modérée en cas de contact cutané occlusif ou de projection de produit non-dilué [8]. Il existe toutefois des cas d'allergie [21] ou d’eczéma de contact (par exemple lors de l'utilisation de crèmes dermiques utilisées pour traiter l'herpès labial[22]). Il est fortement irritant pour les yeux. De manière générale, il est recommandé d'éviter le contact du produit avec la peau ou les yeux.
Voie respiratoire
L'inhalation de vapeur de propylène glycol ne semble pas présenter de risques importants lors des usages courants. Dans des conditions expérimentales, une inhalation pendant une heure d'un aérosol contenant 10 % de propylène-glycol ne provoque aucun effet sur les sujets exposés. Une exposition d'une minute dans une atmosphère contenant une concentration importante de propylène-glycol dans l'air (309 mg/m3) provoque une irritation oculaire et respiratoire. Aucune valeur limite d'exposition professionnelle dans l'air n'est fixée dans l'Union Européenne ou aux États-Unis [8].
Effets génotoxiques
Effets cancérigènes
Effets sur le système reproducteur
Le propylène-glycol n’agit ni sur la fertilité ni sur le développement des animaux.[8].
Toxicité indirecte
Comme tout solvant, le propylène glycol peut présenter une toxicité indirecte, étant capable de solubiliser un grand nombre de produits potentiellement toxiques issus de la chimie organique[24]. En tant que surfactant ou solvant, sa capacité à augmenter la toxicité de certains pesticides tels que le diuron, l'atrazine et l'aminotriazole est discutée[25].
Intoxication
Elle peut être due à une ingestion accidentelle, mais aussi par l'injection, à fortes doses, de certains médicaments, dont le propylène glycol constitue le diluant[26].
A fortes doses, la molécule peut provoquer une insuffisance rénale, une insuffisance hépatique. Au niveau biologique, il existe une acidose lactique, une hyperosmolarité. Le traitement repose sur l'hémodialyse[27].
Notes et références
- PROPYLENEGLYCOL, fiche(s) de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée(s) le 9 mai 2009.
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « PROPYLENE GLYCOL », sur Hazardous Substances Data Bank (consulté le 3 février 2010).
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, England, John Wiley & Sons Ltd, , 239 p. (ISBN 978-0-471-98369-9, LCCN 98018212).
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, USA, McGraw-Hill, , 7e éd., 2400 p. (ISBN 978-0-07-049841-9, LCCN 96051648), p. 2-50.
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 1, Huston, Texas, Gulf Pub. Co., (ISBN 978-0-88415-857-8, LCCN 96036328).
- « Propylène glycol » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009.
- Fiche toxicologique FT 226 de l'Institut national de recherche et de sécurité (INRS), 1994.
- Werley MS, McDonald P, Lilly P, Kirkpatrick D, Wallery J, Byron P, Venitz (2011) Non-clinical safety and pharmacokinetic evaluations of propylene glycol aerosol in Sprague-Dawley rats and Beagle dogs. J. Toxicology. 2011 Sep 5; 287(1-3):76-90. Epub 2011 Jun 12 ().
- http://www.sciam.com/article.cfm?id=ice-flight-3407.
- Holfield, R. (1995). Glycol coolants improve heat transfer and corrosion control. Pipeline & gas journal, 222(3), 28-30 (résumé).
- Bonet, F., Delmas, V., Grugeon, S., Herrera Urbina, R., Silvert, P. Y., & Tekaia-Elhsissen, K. (1999) Synthesis of monodisperse Au, Pt, Pd, Ru and Ir nanoparticles in ethylene glycol. NanoStructured Materials, 11(8), 1277-1284.
- « L-methionine acide amine amidon », sur www.metabolic-explorer.com (consulté le 22 juin 2015).
- « UPM’s ValChem project receives significant EU funding to demonstrate wood to chemicals value chain », sur www.upm.com (consulté le 22 juin 2015).
- « ICIS Pricing,prix moyen 2012-2014, spot, MPG Industriel FD NWE ».
- Flanagan RJ;Braithwaite RA;Brown SS;Widdop B;de Wolff FA;. The International Programme on Chemical Safety: Basic Analytical Toxicology. WHO, 1995.
- Guillot M.; Bocquet G.; Eckart P.; Amiour M.; El-Hachem C.; Garnier R.; Galliot-Guilley M.; Haguenoer J. M., « Environnement domestique et intoxication aiguë au propylène glycol chez un nourrisson de deux ans. À propos d'une observation inhabituelle. », sur http://cat.inist.fr, Archives de pédiatrie, 2002, vol. 9, no4, pp. 382-384, e.
- National Library of Medicine;.Propylene glycol is used in antifreezes Human Toxicity Excerpts: CAS Registry Number: 57-55-6 (1,2-Propylene Glycol). Selected toxicity information from HSDB. 2005.
- Gaunt, I. F.; Carpanini, F. M. B.; Grasso, P.; Lansdown, A. B. G. (1972). "Long-term toxicity of propylene glycol in rats". Food and Cosmetics Toxicology 10 (2): 151–162. ().
- Agency for Toxic Substances and Disease Registry (2008). Addendum to the Toxicological Profile for Propylene Glycol. p. 7.
- Fisher, A. A. (1990). Use of glycerin in topical minoxidil solutions for patients allergic to propylene glycol. Cutis, 45(2), 81-82.
- Claverie, F., Giordano-Labadie, F., & Bazex, J. (1997). Eczéma de contact au propylène glycol: Concentration et véhicule adaptés pour les tests épicutanés. In Annales de dermatologie et de vénéréologie (Vol. 124, No. 4, p. 315-317). Masson.
- (en) U.S. DEPARTMENT OF HEALTH AND HUMAN SERVICES Public Health Service Agency for Toxic Substances and Disease Registry, « ATSDR - Toxicological Profile: Propylene Glycol » [PDF], sur www.atsdr.cdc.gov, (consulté le 24 janvier 2017).
- Neipp, L. (1957). Action du propylène-glycol et d’autres substances à fonction alcool sur l’activité antibactérienne. Pathobiology, 20(2), 150-160. (extrait ).
- Brinquin, L., Rousseau, J. M., Corbe, H., DIRAISON, Y., & BONSIGNOUR, J. (1993). Intoxication aiguë volontaire par herbicide à base de diuron, d'atrazine et d'aminotriazole: toxicité du solvant, le propylène-glycol?. Journal européen des urgences, 6(1), 20-22 (résumé).
- Kraut JA, Mullins ME, Toxic alcohols, N Engl J Med, 2018;378:270-280.
- Zar T, Graeber C, Perazella MA, Recognition, treatment, and prevention of propylene glycol toxicity, Semin Dial, 2007;20:217-219.
Voir aussi
Articles connexes
- Éthylène glycol
- Diéthylène glycol
- Éther de glycol
Liens externes
Bibliographie
- (en) Vasilevskaya, V. V., Khokhlov, A. R., Matsuzawa, Y., & Yoshikawa, K. (1995). Collapse of single DNA molecule in poly (ethylene glycol) solutions. The Journal of chemical physics, 102(16), 6595.
- (en) Sawhney, A. S., Pathak, C. P., & Hubbell, J. A. (1993). Bioerodible hydrogels based on photopolymerized poly (ethylene glycol)-co-poly (. alpha.-hydroxy acid) diacrylate macromers. Macromolecules, 26(4), 581-587.
- Portail de la chimie
- Portail de la pharmacie
- Portail de l’énergie