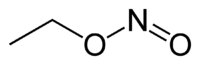
Nitrite d'éthyle
Le nitrite d'éthyle est un composé de la famille des nitrites d'alkyle. Il se présente sous la forme d'un liquide incolore à jaunâtre, à l'odeur éthérée, ou d'un gaz incolore (ébullition à 17 °C). C'est un produit particulièrement instable (il se décompose quand il est stocké[2]), et explosif. Il libère notamment des oxydes d'azote par décomposition.
| Nitrite d'éthyle | |||
 | |||
 | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | Nitrite d'éthyle | ||
| No CAS | |||
| No ECHA | 100.003.385 | ||
| No EC | 203-722-6 | ||
| SMILES | |||
| InChI | |||
| Propriétés chimiques | |||
| Formule brute | C2H5NO2 [Isomères] |
||
| Masse molaire[1] | 75,0666 ± 0,0028 g/mol C 32 %, H 6,71 %, N 18,66 %, O 42,63 %, |
||
| Propriétés physiques | |||
| T° ébullition | 17 °C[2] | ||
| Masse volumique | 0,8695 g·cm-3[2] | ||
| T° d'auto-inflammation | 90 °C[2] | ||
| Point d’éclair | −35 °C[2] | ||
| Limites d’explosivité dans l’air | limite basse : 3,0 Vol.-%, 95 g·m-3 limite haute :50 Vol.-%, 1 555 g·m-3 Pression d'explosion max: 11,6 bar |
||
| Précautions | |||
| Directive 67/548/EEC[2] | |||
 Xn  E Phrases R : 2, 20/21/22, Phrases S : (2), |
|||
| Transport[2] | |||
| Unités du SI et CNTP, sauf indication contraire. | |||
Synthèse
Le nitrite d'éthyle peut être préparé à partir d'éthanol et de nitrite de sodium, en présence d'acide sulfurique[3] :
Utilisation
Le nitrite d'éthyle est le principal ingrédient d'un remède sud-africain à base d'éthanol contre le rhume ou la grippe, connu sous le nom de « witdulsies » et vendu en pharmacie. Il est connu comme remède traditionnel afrikaans et pourrait avoir des origines néerlandaise, puisque ce remède semble exister aussi dans la communauté Amish d'origine germano-néerlandaise aux États-Unis, et est appelé « sweet nitrite » (« nitrite doux ») ou « sweet spirit of nitre » (« esprit doux de nitre »). Cependant, la FDA a interdit sa vente à travers le pays depuis 1980[4].
Risques
Il peut exploser au contact d'agents réducteurs, d'acides, lors d'impact, de friction, s'il est chauffé ou en contact avec un corps incandescent. Il réagit violemment avec l'eau, et forme un mélange explosif avec l'air[2].
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée du numéro CAS « 109-95-5 » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 20 juillet 2010 (JavaScript nécessaire)
- Semon, W. L.; Damerell, V. R. (1943). "Dimethylglyoxime". Org. Synth.; Coll. Vol. 2: 204.
- http://www.fda.gov/Drugs/DevelopmentApprovalProcess/DevelopmentResources/Over-the-CounterOTCDrugs/StatusofOTCRulemakings/ucm072140.htm
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Ethyl nitrite » (voir la liste des auteurs).
- Portail de la chimie
