Neurone
Un neurone, ou une cellule nerveuse, est une cellule excitable constituant l'unité fonctionnelle de base du système nerveux.
Les neurones assurent la transmission d'un signal bioélectrique appelé influx nerveux. Ils ont deux propriétés physiologiques : l'excitabilité, c'est-à-dire la capacité de répondre aux stimulations et de convertir celles-ci en impulsions nerveuses, et la conductivité, c'est-à-dire la capacité de transmettre les impulsions.
Statistiques
Le nombre total de neurones du cerveau humain est estimé de 86[1] à 100 milliards (1011)[2],[3].
Les neurones sont moins nombreux que les cellules gliales (il y a généralement 3 cellules gliale sur un neurone)[4]. Elles sont les seconds composants du tissu nerveux assurant plusieurs fonctions dont le soutien et la nutrition des neurones.
Le cerveau n'est pas le seul organe à avoir une forte concentration de neurones : l'intestin en compte selon les estimations, environ 500 millions[5] et le cœur environ 40 000[6],[7].
Structure
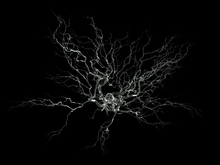
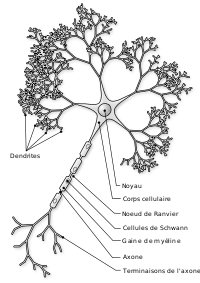
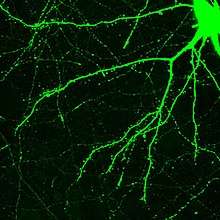
Le neurone est composé d'un corps appelé péricaryon ou corps cellulaire ou encore soma, et de deux types de prolongements : l'axone, unique, qui conduit le potentiel d'action de manière centrifuge[citation nécessaire], et les dendrites, qui sont en moyenne 7 000 par neurone et qui conduisent les potentiels d'action de manière centripète[citation nécessaire]. La morphologie, la localisation et le nombre de ces prolongements, ainsi que la forme du soma, varient et contribuent à définir différentes familles morphologiques de neurones. Par exemple, il existe des neurones unipolaires ou multipolaires[citation nécessaire].
Le diamètre du corps des neurones varie selon leur type, de 5 à 120 μm. Il contient le noyau, bloqué en interphase et donc incapable de se diviser, et le cytoplasme. On trouve dans le cytoplasme le réticulum endoplasmique rugueux (formant les corps de Nissl des histologistes), les appareils de Golgi, des mitochondries et des neurofilaments qui se regroupent en faisceau pour former des neurofibrilles.
L'axone (ou fibre nerveuse) a un diamètre compris entre 1 et 15 μm, sa longueur varie d'un millimètre à plus d'un mètre. Le cône d'émergence, région extrêmement riche en microtubules, constitue l'origine de l'axone. Il est également appelé zone gâchette car il participe à la genèse du potentiel d'action. Il décrit un trajet plus ou moins long (quelquefois plusieurs mètres)[Quand ?] avant de se terminer en se ramifiant (c'est l'arborisation terminale). Chaque ramification se termine par un renflement, le bouton terminal ou bouton synaptique où s'accumulent des vésicules synaptiques contenant un neurotransmetteur. Cependant, s'observent aussi des « enfilades » de renflements synaptiques sur un même segment axonal constituant des synapses en passant. La membrane plasmique de l'axone, ou axolemme (en), borde l'axoplasme en continuité avec le cytoplasme du péricaryon. Il est constitué de neurofilaments et de microtubules qui sont parcourus par des vésicules (celles-ci sont produites par le réticulum endoplasmique rugueux et les appareils de Golgi). Certains axones sont recouverts d'une gaine de myéline, formée par des cellules gliales, les cellules de Schwann dans le système nerveux périphérique, et les oligodendrocytes dans le système nerveux central. On estime qu'environ un axone sur trois est recouvert de myéline. Le recouvrement des axones par la myéline est en fait discontinu, séparé par les nœuds de Ranvier, lesquels sont isolés par des astrocytes. Ce recouvrement permet une plus grande vitesse de passage de l'information nerveuse.
Les dendrites sont nombreuses, courtes et très ramifiées dès leur origine. Elles sont parfois recouvertes d'épines dendritiques (élément post-synaptique). Le dendrite conduit l'influx nerveux, induit à son extrémité, jusqu'au corps cellulaire : c'est un prolongement afférent. Des vésicules peuvent également y circuler le long des faisceaux de microtubules.
Les axones sont rassemblés en faisceaux, eux-mêmes reliés par du tissu conjonctif (endonèvre et périnèvre) formant les tractus et les nerfs.
Génétique neuronale
L'ADN des neurones est, comme dans tout autre type cellulaire, susceptible de subir des modifications (délétions de chromosomes, duplications de séquences, événements de transposition, mutations ponctuelles...). Cependant, des expériences de séquençage de neurones au sein d'un même cerveau[8],[9] ont montré que les neurones étaient plus susceptibles à ces événements que les autres cellules d'un même organisme. Ce phénomène s'appelle le mosaïcisme du cerveau (Brain mosaicism)[10] et est observé chez différentes espèces.
Les mécanismes sous-jacents à ce plus grand mosaïcisme somatique des cellules du cerveau par rapport aux cellules d'autres organes sont encore peu connus, les conséquences de ce mosaïcisme comme l'éventuel effet physiologique qu'il pourrait avoir dans la plasticité neurale ou encore dans diverses pathologies font l'objet d'intenses études et financements[11].
Concentrations ioniques
Les neurones disposent d'ions, permettant aux neurones de varier leur potentiel, avoir des courants ioniques et aussi de créer des potentiels d'actions (ou influx nerveux, voir prochaine section).
Ces concentrations ne sont pas universelles car elles varient en fonction de l'espèce. Par exemple, un mammifère n'aura pas les mêmes concentrations ioniques qu'un calmar.
À chaque instant, nos neurones possèdent des potentiels de membrane qui existent grâce aux gradients électrochimiques exercés par les ions. L'exemple le plus commun en neurosciences est celui du potentiel de repos et du potentiel d'action. En effet, le potentiel de repos est dû à la perte continuelle d'ions potassiums (K+) de la face intracellulaire vers la face extracellulaire car certains canaux potassiques sont ouverts à ce potentiel (~ -60mv ou plus rarement ~ -90mv). De ce fait, le potentiel de la membrane (Vm) tend vers le potentiel d'équilibre des ions K+, qui est à peu près -90mV. Mais comme un tout petit peu de canaux sodiques (Na+) sont aussi ouverts (dit perméables) à ce potentiel, le potentiel de repos de la membrane se situe entre le potentiel d'équilibre des ions K+ (EK+) et celui de Na+ (ENa+). Celui-ci sera logiquement beaucoup plus proche de EK+ que de ENa+ car il y a bien plus de canaux potassiques ouverts que de canaux sodiques, donc au bout du compte le potentiel de repos sera très souvent aux alentours de -60mV. Pour le potentiel d'action, il est expliqué dans d'autres sections ci-dessous.
Remarque :
Dû au fait que les ions K+ sont en minorité en intracellulaire par rapport en extracellulaire (voir tableau ci-dessous), les canaux potassiques ouverts vont créer un efflux pour pouvoir atteindre le potentiel d'équilibre EK+ qui est de -90mV environ.
À l'inverse, les canaux sodiques vont créer un influx (l'inverse d'efflux) d'ions Na+ pour pouvoir là aussi atteindre le potentiel d'équilibre ENa+ (83 mV).
| Ions | Intracellulaire | Extracellulaire |
|---|---|---|
| Potassium (K+) | 140 mM | 5 mM |
| Sodium (Na+) | 5-15 mM | 145 mM |
| Chlorure (Cl-) | 4-30 mM | 110 mM |
| Calcium (Ca²+) | 0,0001 mM | 1-2 mM |
Informations : Ce tableau est directement repris du livre Neurosciences 5e édition aux éditions de boeck car il illustre de manière simple et les valeurs sont semblables à tout autre véritable tableau de ce genre.
Dans ce tableau, mM est ici une ancienne unité, signifiant miliMolaires (mol.L-1 ou mol/L).
Remarque :
Les valeurs intracellulaires pour les ions sodium, 5-15 mM, dépendent du mammifère en question. Il en va même pour les ions chlorures et calciums.
L'influx nerveux
Au repos, il existe une différence de potentiel négative (de l'ordre de -60 mV à -90 mV, c'est le potentiel de repos) entre la face intracellulaire de la membrane du neurone et sa face extracellulaire. Cette différence de potentiel résulte d'une différence de concentration en ions entre l'intérieur et l'extérieur du neurone secondaire à une perméabilité sélective de la membrane plasmique et d'autre part à des courants ioniques actifs transmembranaires (par exemple, la pompe sodium-potassium ATP-asique). Il existe également des courants de fuite concernant les ions potassium vers le milieu extracellulaire[pas clair] par des canaux ioniques spécifiques transitoirement ouverts (à cause des fluctuations électro-chimiques locales).
L'influx nerveux se caractérise par une modification instantanée et localisée de la perméabilité de la membrane du neurone : des ions sodium (Na+) pénètrent dans la cellule en passant à travers des canaux ioniques sélectivement perméables au sodium. Le potentiel de membrane prend alors une valeur positive (environ +35 mV) proche du potentiel électro-chimique d'équilibre du sodium (ENA). Ce phénomène porte le nom de dépolarisation. Puis, très rapidement des ions potassium (K+) sortent de la cellule en passant à travers d'autres canaux ioniques, perméables au potassium. Le potentiel de membrane décroît pour aboutir à une valeur plus basse que la valeur du potentiel de repos : on parle de repolarisation puis d'hyperpolarisation. Puis il y a une phase de retour à la normale grâce à l'action d'une pompe ionique ATP-asique sodium-potassium dépendante. La variation locale, transitoire et stéréotypée du potentiel transmembranaire de l'axone comprenant la dépolarisation et la repolarisation, s'appelle le potentiel d'action. Il ne dure que quelques millisecondes. Le potentiel d'action, ou influx nerveux, se propage de proche en proche le long de l'axone du neurone, ou d'un nœud de Ranvier à l'autre (conduction saltatoire) .
Remarques :
- Lorsque les canaux sodiques sont ouverts, la membrane est totalement insensible aux stimuli additionnels. La cellule est en période réfractaire absolue. Durant la repolarisation, la membrane peut être stimulée par un stimulus très important. Cette période est appelée période réfractaire relative.
- À la suite de l'existence d'un potentiel seuil, le potentiel d'action suit la loi du « tout ou rien ».
Les synapses
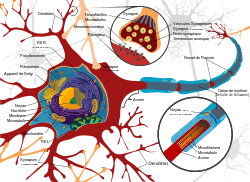
Le relais qui assure la transmission de l'influx nerveux est la synapse. Il y en a de 1 à plus de 100 000 par neurone (moyenne 10 000).
Il existe deux sortes de synapse :
- Les synapses électriques (jonction GAP, également appelées jonction communicante), qui sont surtout retrouvées chez les invertébrés et les vertébrés inférieurs, rarement chez les mammifères.
- Les synapses chimiques, très majoritaires chez les mammifères et l'homme. Certains circuits cérébraux, nécessitant une grande rapidité pour assurer la survie, ont conservé des synapses électriques.
La synapse est constituée d'un élément présynaptique, d'une fente synaptique et d'un élément postsynaptique.
- L'élément présynaptique est soit la membrane du bouton terminal de l'axone, soit la membrane d'une dendrite. C'est le lieu de synthèse et souvent d'accumulation du neuromédiateur. Il assure la libération du neuromédiateur sous l'influence d'un potentiel d'action. Il contient les vésicules présynaptiques, contenant le neuromédiateur. Il existe 4 types de vésicules :
- Les vésicules arrondies à centre clair, sphériques, de diamètre de 40 à 60 nm. Elles contiennent l'acétylcholine, l'acide glutamique, et la substance P ;
- Les vésicules aplaties à centre clair, de forme plutôt ovale, avec un diamètre de 50 nm. Elles contiennent le GABA et la glycine, donc des neurotransmetteurs inhibiteurs ;
- Les petites vésicules à centre dense, de forme sphérique, et de diamètre de 40 à 60 nm. Elles contiennent la noradrénaline, la dopamine, et la sérotonine ;
- Les grandes vésicules à centre dense, sphériques, de 80 à 100 nm de diamètre.
- L'élément postsynaptique peut être la membrane d'un axone, d'un péricaryon, d'une dendrite, d'une cellule somatique (exemple : cellule musculaire). Suivant leur effet, on différencie les synapses excitatrices et les synapses inhibitrices. Il y a un épaississement de la membrane postsynaptique, qui devient très large et très dense (ceci permet, au microscope électronique, de repérer aisément le sens de propagation de l'information).
- La fente synaptique, qui mesure environ 20 nm de large. Elle est remplie de matériel dense parallèle aux membranes.
D'habitude, le lieu initial de la dépolarisation est la membrane postsynaptique. L'influx nerveux se propage ensuite le long de la membrane de la dendrite puis du péricaryon en s'atténuant peu à peu. Si au niveau du cône d'émergence, le potentiel est suffisant (loi du tout ou rien), des potentiels d'action sont générés qui se propageront le long de l'axone sans déperdition. En arrivant à la membrane du bouton terminal, ils déclencheront la libération des microvésicules contenant les neurotransmetteurs, qui diffuseront dans la fente synaptique avant d'être captés par les récepteurs de la membrane postsynaptique.
La propagation de l'influx nerveux est un phénomène qui consomme de l'énergie, en particulier pour activer les pompes qui rétablissent l'équilibre ionique, après la re-perméabilisation de la membrane aux ions (fermeture des canaux ioniques). Cette énergie est fournie par la dégradation de l'adénosine triphosphate (ATP) en adénosine-diphosphate (ADP). L'ATP sera ensuite régénéré par les mitochondries.
On peut classer topographiquement les différents types de synapses en fonction de la partie de la cellule qui sert d'origine et d'arrivée. On aura ainsi des synapses :
- Axodendritique, les plus fréquentes, où l'influx passe d'un axone à une dendrite,
- Axosomatique où l'influx passe d'un axone à un corps cellulaire
- Axoaxonique, où l'influx remonte d'un axone à un autre axone situé en amont pour la régulation du neurone pré-synaptique (généralement c'est une inhibition, une sorte de régulation en boucle)
- Dendrodendritique où l'influx passe d'une dendrite à une autre dendrite
- Dendrosomatique, où l'influx passe d'une dendrite à un corps cellulaire
- Somatosomatique où la synapse se fait entre deux corps cellulaires.
Neurogenèse et neurolyse
Chez l'humain, avant les quatre premiers mois, l'organisme produit 8,6 neurones par seconde pour atteindre un nombre total de 100 milliards. Cependant, c'est durant les quatre premiers mois de la vie embryonnaire que l'augmentation la plus marquée du nombre de neurones est observable ; il se formerait environ 500 000 neurones par minute[12].
Durant la vie adulte les pertes neuronales spontanées ou causées par une dégénérescence pathologique (comme dans la maladie de Parkinson ou la maladie d'Alzheimer) ou encore par des traumatismes du système nerveux central sont définitives : le neurone est en effet une cellule non divisible, ce qui empêche le remplacement des neurones perdus. Mais des études tendent à montrer que certaines cellules souches équivalentes aux cellules gliales, peuvent générer de nouvelles cellules gliales et de nouveaux neurones, que ce soit des cellules souches d'un cerveau mature ou d'un cerveau en maturation[4] [voir page 7 et 8]. Néanmoins, le dogme de l'absence de neurogenèse après la naissance est réfuté depuis les années 1970[13]. De nouveaux neurones continuent à être produits tout au long de la vie adulte dans deux zones très restreintes du cerveau des mammifères, l'hippocampe et le bulbe olfactif.
La neurolyse est la destruction d'une cellule nerveuse, notamment par apoptose ou par des leucocytes ou des cellules gliales qui l'ont envahie et l'ont phagocytée. Elle désigne également l'opération chirurgicale consistant à libérer un nerf lorsque celui-ci est comprimé par une adhérence pathologique
Historique
Le terme « neurone » fut introduit dans le vocabulaire médical en 1881 par l'anatomiste allemand Heinrich Wilhelm Waldeyer.
De nouveaux types de neurones sont régulièrement découvert au sein des organismes de diverses espèces. Plus rarement on en découvre encore chez l'Homme, avec par exemple en 2018 la description d'un nouveau type de cellule neuronale trouvé dans la couche externe du cortex, une zone du cerveau qui abrite de nombreux types de neurone capables d'inhiber l'activité d'autres neurones[14]. Il a été trouvé lors d'une étude cherchant à répertorier tous les types de cellules humaines cérébrales en combinant l'anatomie et la génétique. Baptisé « rosehip », cette cellule est plus petite et compacte que les autres neurones, organisée en faisceau dense et buissonnant autour d’un gros bouton central en forme de bulbe[15]. Selon l'étude parue dans Nature Neurosciences[14], ce type de neurone et son expression génétique semblent manquer chez la souris[15].
Utilisation
Marquage neuronal
Des colorants ou marqueurs spécifiques sont utilisés depuis plus de 100 ans pour détecter les neurones et les colorer dans des préparations. Depuis peu, on peut même les observer en fluorescence sans les tuer. On peut aussi utiliser des anticorps dirigés contre les neurofilaments ou contre la protéine tau, qui ne sont retrouvés que dans les neurones.
Transformation de cellules souches en neurones
En 2008, la transformation de cellules souches en neurones du cortex et leur greffe réussie dans le cerveau de souris (la majorité des nouveaux neurones s’étant connectés avec de nombreuses parties du cerveau des souris), effectuées à l’Université libre de Bruxelles, constitue une piste sérieuse pour la guérison de diverses maladies neurologiques et psychiatriques comme les épilepsies, les accidents vasculaires cérébraux, la maladie d'Alzheimer ou la schizophrénie[16].
Neurone formel
Un neurone formel est une représentation mathématique et informatique du neurone biologique. Il reproduit certaines caractéristiques biologiques, en particulier les dendrites, axone et synapses, au moyen de fonctions et de valeurs numériques. Les neurones formels sont regroupés en réseaux de neurones. Grâce à des algorithmes d'apprentissage automatique, on peut régler un réseau de neurones pour lui faire accomplir des tâches qui relèvent de l'intelligence artificielle.
Chez les animaux
.jpg)
Pour plus de détails, voir l'article : Liste d'animaux par le nombre de neurones.
Les neurones sont présents chez tous les animaux à l'exception des éponges et des placozoaires. Il existe deux hypothèses majeurs concernant leur apparition :
- Ils seraient apparus chez les eumétazoaires et donc constitueraient donc une synapomorphie de ce groupe. Dans cette hypothèse les cténaires font partie des eumétazoaires. Il s'agit de l'hypothèse dominante actuellement.
- Ils seraient apparus indépendamment chez les eumétazoaires et les cténaires (qui ne font alors pas partie des eumétazoaires).
Chez les cnidaires et les cténaires, les neurones ne sont pas polarisés, le signal nerveux passe dans les deux sens. On ne parle donc pas de dendrites ou d'axones mais de neurites.
Chez les bilatériens, il y a apparition d'une spécialisation des neurites en prolongement émetteur (axone) ou récepteur (dendrite).
Notes et références
- Janlou Chaput, « En bref : le cerveau aurait-il perdu 14 milliards de neurones ? », sur Futura-Sciences,
- Williams, R and Herrup, K (2001). The Control of Neuron Number, The Annual Review of Neuroscience no 11, p. 423–453 (1988)
- Hervé Chneiweiss, neurobiologiste, neurologue et chercheur, entendu dans l'émission Révolutions médicales du 15 janvier 2013 sur France Culture estime que le cerveau possède ± 200 milliards de cellules réparties en ± 60 milliards de neurones et 110 à 130 milliards de cellules gliales. S'y ajoutent 100 km de vaisseaux.
- « Neurosciences 2015 (Neurosciences) », sur contenu.deboecksuperieur.com (consulté le 24 février 2018)
- Emma Young, « Gut Instincts: The Secrets of your Second Brain », sur New Scientist, New Scientist, (consulté le 8 avril 2015) (ainsi que NeuroScienceStuff, archived 2013-05-04)
- « Le coeur a aussi des neurones – Nos Pensées », Nos Pensées, (lire en ligne)
- (en-US) « Chapter 01: Heart-Brain Communication - HeartMath Institute », sur heartmath.org (consulté le 24 février 2018)
- (en) « Ubiquitous L1 Mosaicism in Hippocampal Neurons », Cell, vol. 161, no 2, , p. 228–239 (ISSN 0092-8674, DOI 10.1016/j.cell.2015.03.026, lire en ligne)
- M. J. McConnell, M. R. Lindberg, K. J. Brennand, J. C. Piper, T. Voet, C. Cowing-Zitron, S. Shumilina, R. S. Lasken, J. R. Vermeesch, I. M. Hall, F. H. Gage (2013), Mosaic Copy Number Variation in Human Neurons. Science, 2013; 342 (6158): 632 DOI: 10.1126/science.1243472
- « Insights into the role of somatic mosaicism in the brain », Current Opinion in Systems Biology, vol. 1, , p. 90–94 (ISSN 2452-3100, DOI 10.1016/j.coisb.2016.12.004, lire en ligne)
- (en) Michael J. McConnell, John V. Moran, Alexej Abyzov et Schahram Akbarian, « Intersection of diverse neuronal genomes and neuropsychiatric disease: The Brain Somatic Mosaicism Network », Science, vol. 356, no 6336, , eaal1641 (ISSN 0036-8075 et 1095-9203, PMID 28450582, DOI 10.1126/science.aal1641, lire en ligne)
- Marieb, Helen, Hoen, Katja. Anatomie et physiologie humaines, ERPI éditions, 2010, p. 442
- voir notamment les travaux des Docteurs André Gernez, Delahousse, Jacques Lacaze, Dumont et Deston
- Eszter Boldog, Trygve E. Bakken, [...] Gábor Tamás (2018), Transcriptomic and morphophysiological evidence for a specialized human cortical GABAergic cell type| 27 aout 2018 Nature Neurosciencevolume 21, pages1185–1195 (2018)| résumé
- (en) Kelly Servick, « Mysterious new brain cell found in people », Biology, Brain & Behavior, (DOI 10.1126/science.aav2307, lire en ligne)
- Voir les articles du quotidien Le Soir du (résumé des pages 2 et 3 de la version papier dans : ) :
- Page 2 : « Comment des cellules souches peuvent soutenir le cortex - Leur recherche est publiée aujourd’hui dans la revue Nature » : extrait : « Menée par Pierre Vanderhaeghen, chercheur FNRS à l’Institut de recherche interdisciplinaire en biologie humaine et moléculaire de l’Université libre de Bruxelles, une équipe de chercheurs européens vient d’observer pour la première fois le mécanisme interne d’une cellule souche qui évolue en neurone du cortex. Et comment en injecter de nouvelles dans un cerveau afin de tenter de l’aider à mieux fonctionner ! »
- Page 3 : « « Bloquer Alzheimer » : extrait : Il va sans dire que la découverte de la possibilité de transformer des cellules souches en nouveaux neurones capables de remplacer ou épauler les neurones existants pourrait représenter une piste sérieuse pour soigner les malades (ndlr : d’Alzheimer) actuels [...] « L’épilepsie traquée » : extrait : La synchronisation des neurones est une propriété intrinsèque des réseaux neuronaux. L’observation d’EEG de sujets sains révèle l’existence de différentes fréquences propres à l’activité cérébrale qui correspondent à des synchronisations de groupes de neurones. Il semblerait que dans le cas de l’épilepsie, cette synchronisation s’emballerait. Caractériser les neurones qui auraient une activité normale face à ceux qui s’emballent permettrait de tenter de réduire l’ampleur des crises d’épilepsie [...] Page 3 : « L’accident vasculaire » : extrait : Ce déficit concerne généralement un territoire bien défini du cerveau. C’est pourquoi comprendre comment on pourrait, à terme, « fabriquer » des pièces de rechange qui pourraient remplacer les neurones détruits donne l’espoir de diminuer la lourdeur des séquelles de cette maladie ».
Voir aussi
Bibliographie
- Qu'est-ce qu'un neurone ?, B. Calvino, Le Pommier, 2006, (ISBN 978-2-7465-0280-2)
Articles connexes
- Adrénergique
- Cellule amacrine
- Cellule gliale
- Cerveau
- Classement thématique des neurosciences
- Développement du neurone
- Interneurone
- Moelle épinière
- Neurogenèse
- Neurotransmetteur
- Plasticité synaptique
- Réflexe d'extension
- Réflexe de flexion
- Synapse
- Théorie du neurone
- Théorie des neurones miroirs
Liens externes
- (en) Article « Neuron » sur Scholarpedia.
- Portail des neurosciences
- Portail de la biologie