Dientamoebose
La dientamoebose est une affection causée par le protozoaire Dientamoeba fragilis qui infecte le tractus gastro-intestinal bas de l'humain. Il s'agit d'une cause importante de diarrhée du voyageur, de douleurs abdominales chroniques, d'asthénie chronique ainsi que, chez l'enfant, de troubles du développement.
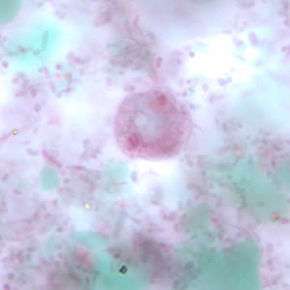
| Spécialité | Infectiologie (en) |
|---|
| CIM-9 | 007 |
|---|---|
| DiseasesDB | 32407 |
| eMedicine | 997239 |
| eMedicine | ped/563 |
| MeSH | D004030 |
![]()
Histoire
Les premières descriptions faisaient état d'un micro-organisme non pathogène, bien que cinq des sept premiers individus dont le parasite était isolé se plaignaient de symptômes de dysenterie. Ce rapport, datant de 1918[1], concluait à un organisme non pathogène en raison de sa consommation de bactéries en culture et non de globules rouges comme ceci était retrouvé chez l'amibe pathogène la mieux connue à l'époque, Entamoeba histolytica. Cette première publication peut avoir contribué à un sous-diagnostic dès cette époque.
Diversité génétique
Étant donné l'existence de nombreux individus porteurs sains de D. fragilis, il est supposé exister des variants pathogène et non pathogène du protozoaire. Une étude d'isolats de D. fragilis issus de 60 individus avec des infections symptomatiques à Sydney retrouvait que tous les individus étaient infectés par le même génotype[2], lequel était le plus commun à travers le monde, mais différait du premier génotype décrit d'un isolat nord-américain également retrouvé en Europe[3].
Épidémiologie
La prévalence de l'infection augmente dans des conditions sanitaires défavorables. Les taux d'infection chez les militaires ainsi que les pensionnaires d'institutions psychiatriques sont supérieurs au reste de la population. Cependant, la véritable incidence de l'infection est toujours mal connue, les techniques de diagnostic de nombreux laboratoires étant souvent inadaptées. Une étude australienne a identifié un grand nombre de patients considérés comme atteints de syndrome du colon irritable qui étaient en fait infectés par D. fragilis[4].
Bien que D. fragilis ait été décrit comme une infection émergente[5], elle est devenue l'une des plus prévalentes parmi les infections gastro-intestinales dans les pays industrialisés, particulièrement parmi les enfants et les adultes jeunes. Une étude canadienne rapporte une prévalence autour de 10 % chez les garçons et les filles âgés de 11 à 15 ans, une prévalence de 11,5 % chez les individus âgés de 16 à 20 ans et une incidence inférieure, de 0,3 à 1,9 % chez les individus de plus de 20 ans[6].
Symptômes
Les symptômes les plus fréquemment retrouvés lors de l'infection à D. fragilis incluent les douleurs abdominales (69 %) et la diarrhée (61 %)[7]. Cette dernière peut être intermittente et n'est pas constamment présente. Elle est souvent chronique, durant plus de deux semaines. La sévérité des symptômes varie d'asymptomatique à sévère[8] et peut inclure une perte de poids, des nausées et vomissements, de la fièvre voire l'implication d'autres organes digestifs.
Les symptômes peuvent être plus sévères chez l'enfant. On peut retrouver en plus des éléments sus-cités une asthénie, de l'urticaire, des démangeaisons ou encore des infections biliaires[5].
Transmission
Des organismes similaires à D. fragilis sont connus pour connaître un stade kystique dans leur cycle de vie leur permettant de survivre en milieu extérieur et facilitant l'infection de nouveaux hôtes. Cependant, la manière exacte par laquelle ce parasite est transmis ne commence qu'à être comprise, la forme trophique du parasite étant extrêmement fragile et une forme kystique n'ayant pu être décrite[6] qu'au cours des années 2013 et 2014. Ainsi, il semble que D. fragilis soit transmis par voie oro-fécale ce qui semble concordant avec le fort taux (40 %) d'infection concomitante avec d'autres protozoaires rapporté au St. Vincent's Hospital à Sydney.
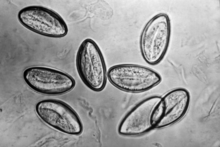
Avant la mise en évidence de ce stade kystique, une théorie suggérait une transmission du parasite concomitante avec les helminthes apportant une protection au parasite durant son séjour en milieu extérieur. Ainsi, de l'ADN de D. fragilis a pu être détecté à la surface d'œufs d'Enterobius vermicularis (oxyurose) suggérant que ces derniers puissent servir de vecteurs au protozoaire[9]. Une ingestion expérimentale d'œufs d'helminthes a permis d'établir l'infection à D. fragilis chez deux expérimentateurs. Cependant, des études récentes ont échoué à montrer une association entre l'infection à helminthes et l'infection par D. fragilis.
Diagnostic
Le diagnostic est le plus souvent obtenu à la suite d'un examen parasitologique des selles. Cependant, environ 30 % des enfants infectés par D. fragilis montrent une éosinophilie dans le sang périphérique.
Des selles ayant été immédiatement fixées dans de l'alcool polyvinylique, de l'acétate de sodium - acide acétique - formaline ou du fixateur de Schaudinn sont soumises à l'examen, le parasite ne restant morphologiquement identifiable que quelques minutes. Tous les échantillons sont colorés avant l'examen au microscope. Si ces conditions ne sont pas réunies, le diagnostic peut revenir faussement positif[10].
Des formes trophozoïtes ont été retrouvées dans des selles non diarrhéiques mettant en lumière la nécessité de pratiquer l'examen parasitologique des selles non uniquement sur des selles diarrhéiques. L'analyse de fragments d'ADN permet de très bonnes sensibilités et spécificités en comparaison de l'examen microscopique pour la détection de D. fragilis et les deux méthodes devraient être employées en parallèle lorsque la PCR est disponible. La méthode de détection la plus sensible semble tous de même la culture du parasite. Le milieu de culture nécessite l'adjonction d'amidon de riz.
Un anticorps fluorescent indirect a été développé pour la détection sur échantillons de selles fixées[11],[12],[13].
Traitement
L'helminthiase concomitante doit être exclue bien que l'association des deux infections n'ait pas été prouvée. Des traitements efficaces ont été rapportés lors de l'utilisation d'iodoquinol, de doxycycline, de métronidazole, de paromomycine ou encore de secnidazole[5],[8]. L'émergence de résistance nécessite l'utilisation de thérapies combinées afin d'éradiquer le parasite. Toutes les personnes vivant sur le même lieu devraient être diagnostiquées, un porteur pouvant être une source d'infections itératives. La paromomycine est un prophylactique efficace pour les voyageurs en zones de faibles conditions sanitaires.
Notes et références
- (en) M. W. Jepps, C. Dobell, « Dientamoeba fragilis ng, n. sp., a new intestinal amoeba from man », Parasitology, vol. 10, , p. 352-367. (DOI 10.1017/S0031182000003929, lire en ligne)
- (en) Stark D, Beebe N, Marriott D, Ellis J, Harkness J, « Prospective study of the prevalence, genotyping, and clinical relevance of Dientamoeba fragilis infections in an Australian population », J. Clin. Microbiol., vol. 43, no 6, , p. 2718–23 (PMID 15956388, PMCID 1151954, DOI 10.1128/JCM.43.6.2718-2723.2005)
- (en) Johnson JA, Clark CG, « Cryptic genetic diversity in Dientamoeba fragilis », J. Clin. Microbiol, vol. 38, no 12, , p. 4653–4654. (PMID 11101615, PMCID 87656)
- Borody T, Warren E, Wettstein A et <Please add first missing authors to populate metadata.>, « Eradication of Dientamoeba fragilis can resolve IBS-like symptoms », J Gastroenterol Hepatol, vol. 17 (Suppl), , A103. (DOI 10.1046/j.1440-1746.2002.02681.x)
- Johnson EH, Windsor JJ, Clark CG, « Emerging from obscurity: biological, clinical, and diagnostic aspects of Dientamoeba fragilis », Clin. Microbiol. Rev., vol. 17, no 3, , p. 553–70, table of contents (PMID 15258093, PMCID 452553, DOI 10.1128/CMR.17.3.553-570.2004)
- Lagacé-Wiens PR, VanCaeseele PG, Koschik C, « Dientamoeba fragilis: an emerging role in intestinal disease », Canadian Medical Association Journal, vol. 175, no 5, , p. 468–9 (PMID 16940260, PMCID 1550747, DOI 10.1503/cmaj.060265)
- (en) Vandenberg O, Peek R, Souayah H, Anne Dediste, Michel Buset, Robert Scheen, Patricia Retore, Georges Zissis et Tom van Gool, « Clinical and microbiological features of dientamoebiasis in patients suspected of suffering from a parasitic gastrointestinal illness: a comparison of Dientamoeba fragilis and Giardia lamblia infections », Int. J. Infect. Dis, vol. 10, no 3, , p. 255–61. (PMID 16469517, DOI 10.1016/j.ijid.2005.05.011)
- (en) Norberg A, Nord CE, Evengård B, « Dientamoeba fragilis -- a protozoal infection that may cause severe bowel distress », Clin. Microbiol. Infect, vol. 9, no 1, , p. 65–8. (PMID 12691546, DOI 10.1046/j.1469-0691.2003.00459.x)
- (en) Ogren J, Dienus O, Löfgren S, Iveroth P, Matussek A, « Dientamoeba fragilis DNA detection in Enterobius vermicularis eggs », Pathogens and disease, vol. 69, no 2, , p. 157–8. (PMID 23893951, DOI 10.1111/2049-632X.12071)
- Grendon JH, Digiacomo RF, Frost FJ, « Dientamoeba fragilis detection methods and prevalence: a survey of state public health laboratories », Public Health Rep, vol. 106, no 3, , p. 322–5 (PMID 1905055, PMCID 1580247)
- Steinitz H, Talis B, Stein B, « Entamoeba histolytica and Dientamoeba fragilis and the syndrome of chronic recurrent intestinal amoebiasis in Israel », Digestion, vol. 3, no 3, , p. 146–53 (PMID 4317789, DOI 10.1159/000197025)
- Windsor JJ, Macfarlane L, Hughes-Thapa G, Jones SK, Whiteside TM, « Detection of Dientamoeba fragilis by culture », Br. J. Biomed. Sci., vol. 60, no 2, , p. 79–83 (PMID 12866914)
- Sawangjaroen N, Luke R, Prociv P, « Diagnosis by faecal culture of Dientamoeba fragilis infections in Australian patients with diarrhoea », Trans. R. Soc. Trop. Med. Hyg., vol. 87, no 2, , p. 163–5 (PMID 8337717, DOI 10.1016/0035-9203(93)90472-3)
Source de la traduction
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Dientamoebiasis » (voir la liste des auteurs).
- Portail de la médecine
- Portail de la parasitologie