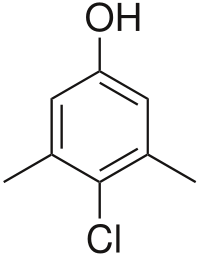
Chloroxylénol
Le chloroxylénol ou 4-chloro-3,5-diméthylphénol est un composé chimique antimicrobien utilisé pour lutter contre les bactéries, algues et moisissures dans les colles, émulsions et peintures et pour nettoyer des réservoirs[5]. Il est aussi régulièrement utilisé dans des solutions antibactériennes comme le Dettol ou des pommades comme la vaseline[6]. Des études ont montré une légère activité antimicrobienne qui peut être améliorée par l'ajout d'additifs. Son action antibactérienne est due à sa capacité à rompre les membranes plasmiques[7].
| Chloroxylénol | |||
 | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | 4-chloro-3,5-diméthylphénol | ||
| Synonymes |
4-chloro-3,5-xylénol, 4-chloro-sym-m-xylénol |
||
| No CAS | |||
| No ECHA | 100.001.631 | ||
| No EC | 201-793-8 | ||
| No RTECS | ZE6850000 | ||
| Code ATC | D08 | ||
| SMILES | |||
| InChI | |||
| Apparence | cristaux beige, odeur proche du phénol[1] | ||
| Propriétés chimiques | |||
| Formule brute | C8H9ClO [Isomères] |
||
| Masse molaire[2] | 156,609 ± 0,009 g/mol C 61,35 %, H 5,79 %, Cl 22,64 %, O 10,22 %, |
||
| pKa | 9,76 | ||
| Propriétés physiques | |||
| T° fusion | 114 à 116 °C[1] | ||
| T° ébullition | 246 °C[1] | ||
| Solubilité | 250 mg·l-1 (eau, 20 °C)[1] | ||
| Masse volumique | 0,890 g·cm-3[3] | ||
| Point d’éclair | 132 °C[1] | ||
| Pression de vapeur saturante | 0,25 hPa (25 °C[3] | ||
| Précautions | |||
| SGH[1] | |||
 |
|||
| NFPA 704[3] | |||
| Transport[3] | |||
| Écotoxicologie | |||
| DL50 | 3 830 mg·kg-1 (rat, oral)[4] | ||
| LogP | 3,27[1] | ||
| Unités du SI et CNTP, sauf indication contraire. | |||
Utilité
Il fait partie de la liste des médicaments essentiels de l'Organisation mondiale de la santé (liste mise à jour en avril 2013)[8].
Toxicité
Le chloroxylénol est modérément à peu toxique pour l'être humain ou les autres mammifères selon l'Environmental Protection Agency qui le classe toutefois en catégorie I de toxicité pour les yeux (le plus haut niveau de toxicité) car il cause de sévères irritations des yeux[5].
Le chloroxylénol est toxique pour l'homme par ingestion. De sérieuses complications respiratoires ont été rapportées dans 7 à 8 % des cas d'ingestion de Dettol (dont le composé actif est le chloroxylénol) entrainant parfois la mort[9],[10],[11].
Par ailleurs le chloroxylénol est :
- pratiquement non toxique pour les oiseaux,
- modérément toxique pour les invertébrés d'eau douce,
- et hautement toxique pour les poissons[5].
Références
- Entrée de « 4-Chloro-3,5-dimethylphenol » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 9 juillet 2012 (JavaScript nécessaire)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Fiche Sigma-Aldrich du composé 4-Chloro-3,5-dimethylphenol, consultée le 9 juillet 2012.
- Journal of the American College of Toxicology. Vol. 4(5), Pg. 147, 1985.
- Chloroxylenol Reregistration Eligibility Decision (RED) sur le site de l'Environmental Protection Agency (EPA).
- (en) Joseph M. Ascenzi, Handbook of disinfectants and antiseptics, New York, M. Dekker, (ISBN 978-0-8247-9524-5, lire en ligne), « Chloroxylenol: an old-new antimicrobial »
- (en) Raza Aly and Howard I. Malbach et H Malbach, « Comparative antibacterial efficacy of a 2-minute surgical scrub with chlorhexidine gluconate, povidone-iodine, and chloroxylenol sponge-brushes », American Journal of Infection Control, vol. 16, no 4, , p. 173–7 (PMID 3189943, DOI 10.1016/0196-6553(88)90029-6)
- WHO Model List of Essential Medicines, 18th list, avril 2013
- (en) PK Lam, CK Chan, ML Tse et FL Lau, « Dettol poisoning and the need for airway intervention », Hong Kong Medical Journal, vol. 18, no 4, , p. 270–275 (PMID 22865169, lire en ligne).
- (en) G.M. Joynt, K.M. Ho et C.D. Gomersall, « Delayed upper airway obstruction: A life-threatening complication of Dettol poisoning », Anaesthesia, vol. 52, no 3, , p. 261-263 (ISSN 0003-2409, PMID 9124667).
- Lester Haines, 'Dettol Man' cleans himself to death.
Sources
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Chloroxylenol » (voir la liste des auteurs).
- Portail de la chimie

