Irinotécan
L'Irinotécan (Campto) est un médicament anticancéreux utilisé dans le traitement des cancers colorectaux.
| Irinotécan | |
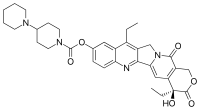
| |
| Identification | |
|---|---|
| Nom UICPA | [1,4’bipipéridine]-1’-carboxylate de (S)-4,11-diéthyl-3,4,12,14-tétrahydro-4-hydroxy- 3,14-dioxo1H-pyrano[3’,4’:6,7]-indolizino[1,2-b]quinoléin- 9-yle |
| No CAS | |
| No ECHA | 100.219.260 |
| Code ATC | L01 |
| DrugBank | APRD00579 |
| PubChem | 3750 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C33H38N4O6 [Isomères] |
| Masse molaire[1] | 586,678 ± 0,0317 g/mol C 67,56 %, H 6,53 %, N 9,55 %, O 16,36 %, |
| Données pharmacocinétiques | |
| Biodisponibilité | NA |
| Métabolisme | hépatique |
| Demi-vie d’élim. | 6 à 12 heures |
| Excrétion | |
| Unités du SI et CNTP, sauf indication contraire. | |
L'irinotécan est un pro-médicament dont le métabolite actif inhibe la topoisomérase 1 induisant des cassures de l'ADN préferentiellement dans les cellules cancéreuses.
La première AMM a été obtenue en France en 1995.
Historique
Dans le cadre d'un large programme sponsorisé par l'institut national du cancer américain portant sur les produits d'origine naturelle, en 1958 M.E. Wall en partenariat avec Jonathan Hartwel identifie in vitro l'action anticancéreuse d'un extrait alcoolique de feuilles issues d'un arbre utilisé en médecine traditionnelle chinoise : Camptotheca acuminata. L'identification de la fraction active de la plante par M. C. Wani permet l'isolement d'un alcaloïde à activité anticancéreuse nommé camptothécine.
Des études pré-cliniques utilisant la camptothécine ont été menées sur des souris démontrant l'activité biologique sur des modèles leucémiques. Des études cliniques précoces ont alors été lancées puis stoppées au début des années 1970 en raison d'une trop grande toxicité. Ce n'est que lors de l'identification de la cible moléculaire de la camptothécine en 1985 (la topoisomérase 1) que l’intérêt pour cette famille de composés a été ravivé. De nouvelles molécules analogues ont été synthétisées tels le topotécan et l'irinotécan (CPT-11). Ce dernier composé étant issu de collaborations de recherche entre la firme japonaise Yakult Honsha Co. et l'université Showa basée à Tokyo. Une alliance entre Yakult Honsha Co. et Daiichi Pharmaceutical a ensuite permis le développement de la molécule et obtenu son autorisation de mise sur le marché au Japon (1994), en France (1995) et aux États-Unis (1996).
Indications
Cancer colorectal métastatique
Depuis l'introduction du 5-fluorouracile en 1957, l'arrivée au milieu des années 1990 de l'irinotécan et de l'oxaliplatine a augmenté l'efficacité des chimiothérapies dans cette indication.
Première ligne de traitement
L'irinotécan est indiqué en association avec le 5-fluorouracile (5-FU)/acide folinique, le bévacizumab, le cétuximab (si statut KRAS non muté de la tumeur) ou la capécitabine.
Deuxième ligne de traitement
L'irinotécan est indiqué en monothérapie après échec d'un traitement par 5-FU/acide folinique.
Indications hors AMM
L'irinotécan peut également être utilisé en association avec le 5-FU et l'oxaliplatine (protocole FOLFIRINOX, FOLFOXIRI) et avec le 5-FU/acide folinique (protocole FOLFIRI).
D'après CercleFinance.com, le 17 juin 2020, « Ipsen annonce avoir obtenu la désignation " Fast Track " de la FDA pour l'irinotécan liposomal (ONIVYDE) en tant que traitement combiné en première ligne du cancer du pancréas métastatique. »[2].
Mécanisme d'action
L'irinotécan est une pro-drogue activée par la carboxylestérase préferentiellement dans le tissu tumoral en un métabolite actif, le SN-38 inhibant la topoisomérase 1. L'inhibition de la topoisomérase I entraine des cassures de l'ADN simple brin bloquant la réplication de l'ADN.
Pharmacocinétique
L'irinotécan présente des propriétés plus hydrosolubles que le SN-38, son métabolite actif le rendant facilement utilisable par voie intraveineuse.
Il existe une large variabilité inter individuelle concernant les concentrations du métabolite actif SN-38 et le modèle d'élimination est biphasique ou triphasique. Cette variabilité dépendant en partie du polymorphisme de l'UGTA1.
Le métabolite actif SN-38 est inactivé par glucuronidation par l'uridine diphosphate glucoronosyltransferase 1A1 (UGT1A1) et éliminé par excrétion biliaire et rénale. La clairance rénale d'élimination est diminuée de 40 % chez les patients avec une bilirubinémie comprise entre 1,5 et 3 fois la limite supérieure de la normale.
Des modèles de chronothérapie ont été développés basées sur des études animales suggérant une administration de nuit préferentielle, celle-ci diminuant les effets indésirables associés et entrainant une meilleure efficacité thérapeutique en particulier chez l'homme. Différents paramétres tels que le sexe, l'expression de certains gènes liés à l'horloge interne sont en cause[3].
Effets indésirables
L'irinotécan peut provoquer des nausées/vomissements, diarrhées aiguës ou tardives et des neutropénies. La molécule est alopéciante et peut entraîner un syndrome de type cholinergique cédant sous atropine. La diarrhée associée à l'irinotécan est sévère et cliniquement significative, entraînant parfois une déshydratation sévère nécessitant une hospitalisation ou une admission en unité de soins intensifs. Cette diarrhée sévère est associé à la composition du microbiote intestinale. En effet, bien qu'administré par voie intraveineuse, le métabolite actif de l'irinotécan (que l'on appelle plus simplement : "SN-38") est métabolisé par le foie par glucuroconjugaison puis éliminé par voie biliaire. Une fois dans les intestins, le SN-38 glucuroconjugué peut être pris en charge par les β-glucuronidases bactériennes de la flore intestinale qui séparent la molécule de glucose du SN-38. Ainsi, le SN-38 est de nouveau sous forme active et peut, alors, induire son activité cytotoxique sur les entérocytes provoquant, alors la diarrhée sévère[4]. Plus récemment (2008), il a été montré que l'administration d'irinotecan modifiait le microbiote intestinale augmentant, alors, le taux de bactéries productrices de β-glucuronidases (E. coli, Staphylococcus spp., Clostridium spp) ce qui, par lien de causalité, augmenterait au fur et à mesure la toxicité intestinale de l'irinotecan[5]. Les perspectives de ces recherches se portent, ainsi, sur la découverte d'inhibiteurs de β-glucuronidases[6], ainsi que l'utilisation de ces enzymes en tant que biomarqueurs de la toxicité intestinale de l'irinotecan[7].
Contre indication
- Maladie inflammatoire chronique de l'intestin et/ ou avec une occlusion intestinale
- Allergie à l'irinotécan
- Grossesse et allaitement
- Bilirubinémie supérieure à trois fois la limite de la normale
- Insuffisance médullaire sévère
- Millepertuis
Études cliniques
En association dans le traitement de première ligne du cancer colorectal métastatique
- En association avec le 5-fluorouracile/acide folinique : Essai de phase III
- En association avec le cétuximab : EMR 62 202 013
- En association avec le cétuximab après échec d'un traitement cytotoxique à base d'irinotécan : Étude EMR 62 202 007 et IMCL CP02 9923.
- En association avec le bévacizumab :Étude AVF2107g
- En association avec la capécitabine : Étude de phase III (CAIRO)
En monothérapie dans le traitement de deuxième ligne du cancer colorectal métastatique
Deux essais de phase III ont montré vs soins de support ou vs perfusion de 5-FU des médianes de survie augmentées (9,2 vs 6,5 mois) et (10,8 vs 8,5 mois) ainsi que des pourcentages de survie à 1 an augmentés (36% vs 14%) et (45% vs 32%) avec une préservation de la qualité de vie associée[8],[9].
Note
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Ipsen : A obtenu la désignation 'Fast Track' de la FDA, Tradingsat.com, 17 juin 2020
- « chronothérapie irinotecan »
- Kiyoshi Takasuna, Yoshio Kasai, Yutaka Kitano et Kazuhiko Mori, « Protective Effects ofKampoMedicines and Baicalin against Intestinal Toxicity of a New Anticancer Camptothecin Derivative, Irinotecan Hydrochloride (CPT-11), in Rats », Japanese Journal of Cancer Research, vol. 86, no 10, , p. 978–984 (ISSN 0910-5050, DOI 10.1111/j.1349-7006.1995.tb03010.x, lire en ligne, consulté le )
- Andrea M Stringer, Rachel J Gibson, Richard M Logan et Joanne M Bowen, « Faecal microflora and β-glucuronidase expression are altered in an irinotecan-induced diarrhea model in rats », Cancer Biology & Therapy, vol. 7, no 12, , p. 1919–1925 (ISSN 1538-4047 et 1555-8576, DOI 10.4161/cbt.7.12.6940, lire en ligne, consulté le )
- Syed Ahmad, Mark A. Hughes, Li-An Yeh et John E. Scott, « Potential Repurposing of Known Drugs as Potent Bacterial β-Glucuronidase Inhibitors », Journal of Biomolecular Screening, vol. 17, no 7, , p. 957–965 (ISSN 1087-0571 et 1552-454X, DOI 10.1177/1087057112444927, lire en ligne, consulté le )
- Ali N. Chamseddine, Michel Ducreux, Jean-Pierre Armand et Xavier Paoletti, « Intestinal bacterial β-glucuronidase as a possible predictive biomarker of irinotecan-induced diarrhea severity », Pharmacology & Therapeutics, vol. 199, , p. 1–15 (ISSN 0163-7258, DOI 10.1016/j.pharmthera.2019.03.002, lire en ligne, consulté le )
- (en) Cunningham D, « Randomised trial of irinotecan plus supportive care versus supportive care alone after fluorouracil failure for patients with metastatic colorectal cancer. », The Lancet, no 352(9138,
- (en) JY Douillard, « Irinotecan combined with fluorouracil compared with fluorouracil alone as first-line treatment for metastatic colorectal cancer: a multicentre randomised trial », The Lancet,
- Portail de la pharmacie
- Portail de la chimie