Complexe d'espèces
En biologie, un complexe d'espèces est un groupe d'organismes étroitement apparentés qui sont si semblables en apparence que les limites entre eux (permettant de les distinguer les uns des autres) sont souvent peu évidentes. Les termes qui sont parfois utilisés comme synonymes mais qui ont une signification plus précise sont les espèces cryptiques (cryptic species en anglais) qui concernent deux ou plusieurs espèces englobées sous un même nom d'espèce, les espèces sœurs (sibiling species) pour deux espèces cryptiques qui sont les plus étroitement apparentées l'une à l'autre, et les "troupeaux d'espèces" (species flocks) pour un groupe d'espèces étroitement apparentées qui vivent dans le même habitat. Dans le cadre de la classification taxonomique informelle, les groupes d'espèces, les agrégats d'espèces et les super-espèces sont également utilisés.

Deux ou plusieurs taxons qui étaient au départ considérés comme conspécifiques (de la même espèce) peuvent être subdivisés par la suite en taxons infraspécifiques (taxons au sein d'une espèce, comme les souches bactériennes ou les variétés végétales), mais il ne s'agit pas d'un complexe d'espèces.
Un complexe d'espèces constitue dans la plupart des cas un groupe monophylétique ayant un ancêtre commun, mais il existe des exceptions. Il peut représenter un stade précoce après la spéciation, mais peut aussi avoir été séparé de la branche évolutive considérée pendant une longue période sans que des différences morphologiques évoluent. La spéciation hybride peut être un élément moteur de l'évolution d'un complexe d'espèces.
Les complexes d'espèces existent dans tous les groupes d'organismes et sont identifiés par l'étude rigoureuse des différences entre les espèces individuelles en utilisant des détails morphologiques minutieux, des tests d'isolement reproductif ou des méthodes basées sur l'ADN, telles que la phylogénétique moléculaire et le barcoding moléculaire. L'existence d'espèces extrêmement similaires peut résulter en une sous-estimation de la diversité des espèces au niveau local et global. La reconnaissance d'espèces similaires mais distinctes est importante dans le cadre de la lutte contre les maladies et les parasites et dans la biologie de la conservation, bien que le tracé de lignes de démarcation entre les espèces puisse être difficile en soi à mettre en place.
Définition
Un complexe d'espèces est généralement considéré comme un groupe d'espèces proches, mais distinctes[5]. Il est évident que ce concept est étroitement lié à la définition d'une espèce. La biologie moderne définit une espèce comme "une lignée de métapopulation évoluant séparément", mais reconnaît que les critères de délimitation des espèces peuvent dépendre du groupe étudié[6]. Ainsi, de nombreuses espèces définies comme telles auparavant, en se basant uniquement sur leur similarité morphologique, se sont avérées être en fait plusieurs espèces distinctes lorsque d'autres critères, tels que la différenciation génétique ou l'isolement reproductif, sont appliqués[7].
Une utilisation plus restreinte applique le terme aux espèces proches entre lesquelles l'hybridation s'est produite ou se produit, ce qui conduit à des formes intermédiaires et à des frontières d'espèces floues[8]. La classification informelle, les superespèces, peut être illustrée par le papillon Hespérie de la mauve, qui est une superespèce qui se divise encore en trois sous-espèces[9].
Certains auteurs appliquent le terme à une espèce présentant une variabilité intraspécifique, ce qui pourrait être le signe d'une spéciation en cours ou naissante. C'est le cas par exemple des espèces annulaires[10],[11] ou des espèces ayant des sous-espèces, pour lesquelles il n'est souvent pas clair si elles doivent être considérées comme des espèces distinctes ou non[12].
Concepts liés
Plusieurs termes sont utilisés comme synonymes d'un complexe d'espèces, mais certains d'entre eux peuvent également avoir une signification légèrement différente ou plus étroite. Dans les codes de nomenclature de la zoologie et de la bactériologie, aucun rang taxonomique n'est défini entre le niveau de sous-genre et le niveau d'espèce[13],[14], mais le code botanique définit quatre rangs en dessous des genres (section, sous-section, série et sous-série)[15]. Différentes alternatives taxonomiques informelles ont été utilisées pour désigner un complexe d'espèces.
Espèces cryptiques (cryptic species)
Aussi appelées races physiologiques[16] (peu commun). Ce terme décrit « des espèces distinctes qui sont classées à tort (et cachées) sous un seul nom d'espèce »[17]. Plus généralement, ce terme est souvent utilisé lorsque les espèces, même si elles sont connues pour être distinguables, ne peuvent être distinguées de manière fiable sur la base de leur morphologie. Le terme "race physiologique" ne doit pas être confondu avec "race physiologique" au sens de "proles".
Espèces apparentées ou sœurs (sibling species)
Également appelées espèces aphaniques. Ce terme, introduit par Ernst Mayr en 1942[18], a d'abord été utilisé avec la même signification que celle des espèces cryptiques[7], mais des auteurs ultérieurs ont souligné l'origine phylogénétique commune[19]. Un article récent définit les espèces sœurs comme des "espèces sœurs cryptiques", « deux espèces qui sont les plus proches (phylogénétiquement) l'une de l'autre et qui n'ont pas été distinguées l'une de l'autre sur le plan taxonomique »[17].
Troupeau d'espèces (species flock)
Aussi appelé essaim d'espèces. Il s'agit d'un « groupe monophylétique d'espèces étroitement apparentées vivant toutes dans le même écosystème »[17]. Inversement, le terme a également été appliqué de manière très large à un groupe d'espèces étroitement apparentées qui peuventt être variables et répandues[20].
Super-espèce (superspecies)
Parfois utilisé comme rang taxonomique informel pour un complexe d'espèces articulé autour d'une espèce "représentative"[21],[22]. Popularisé par Bernhard Rensch et plus tard Ernst Mayr, avec l'exigence initiale que les espèces formant une super-espèce doivent avoir des distributions allopatriques[23]. Pour les espèces composant une super-espèce, on a proposé le terme d'allo-espèce[23].
Agrégat d'espèces (species aggregate)
Utilisé pour désigner un complexe d'espèces, en particulier dans les taxons végétaux où la polypoïdie et l'apomixie sont courantes. Les synonymes historiques sont les collectiva d'espèces (species collectiva), introduites par Adolf Engler, les conespèces (conspecies) et les grex[24]. Les composants d'un agrégat d'espèces ont été appelés ségrégats ou microespèces[24]. On utilise l'abréviation agg. après le nom binominal de l'espèce[8],[25].
Identification
Distinguer des espèces proches au sein d'un complexe nécessite l'étude de différences souvent très subtiles. Les différences morphologiques peuvent être infimes et visibles uniquement par l'utilisation de méthodes adaptées, telles que la microscopie. Cependant, il arrive que des espèces distinctes ne présentent aucune différence morphologique[17], auquel cas d'autres caractères, tels que le cycle de vie, le comportement, la physiologie et la caryotype de l'espèce, peuvent être explorés. Par exemple, les chants territoriaux sont indicatifs d'une espèce chez les grimpereaux, un genre d'oiseaux qui présente peu de différences morphologiques entre les individus[29]. Les tests d'accouplement sont courants dans l'étude de certains groupes, comme les champignons, pour confirmer l'isolement reproductif de deux espèces[27].
L'analyse des séquences d'ADN devient de plus en plus standard pour la reconnaissance des espèces et peut, dans de nombreux cas, être la seule méthode fiable[17]. Différentes méthodes sont utilisées pour analyser ces données génétiques, telles que la phylogénétique moléculaire ou le barcoding moléculaire. Ces méthodes ont largement contribué à la découverte d'espèces cryptiques[17],[30], dont des espèces emblématiques comme l'amanite tue-mouches[2] ou les éléphants d'Afrique[3].
La similitude peut être trompeuse : sur les images ci-dessus, la salamandre de Corse (à gauche) était auparavant considérée comme une sous-espèce de la salamandre tachetée (à droite), mais elle est en fait plus proche de la salamandre noire qui ne possède pas de taches (au centre)[31].
Évolution et écologie
Processus de spéciation

Les espèces formant un complexe ont généralement divergé très récemment les unes des autres, ce qui permet parfois de retracer le processus de spéciation. Les espèces dont les populations sont différenciées, comme les espèces annulaires, sont parfois considérées comme un exemple de spéciation précoce et continue, c'est-à-dire un complexe d'espèces en formation. Néanmoins, des espèces similaires mais distinctes peuvent parfois être isolées pendant longtemps sans que des différences évoluent, un phénomène connu sous le nom de "stase morphologique"[17]. Par exemple, la grenouille amazonienne Pristimantis ockendeni est en fait constituée d'au moins trois espèces différentes qui ont divergé il y a plus de 5 millions d'années[32].
La sélection stabilisatrice a été invoquée comme une force maintenant la similarité dans les complexes d'espèces, en particulier si elles s'adaptent à des environnements spéciaux, comme un hôte dans le cas des symbiotes ou des environnements extrêmes, et qui contraindrait les directions possibles de l'évolution : dans ces cas, il ne faut pas s'attendre à une sélection fortement divergente[17]. De plus, la reproduction asexuée, comme par l'apomixie chez les plantes, peut séparer les lignées sans produire un grand degré de différenciation morphologique.
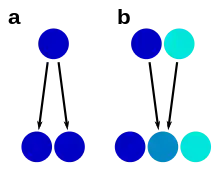
Aires de répartition et habitats
Il n'y pas de consensus sur le fait que les membres d'un groupe d'espèces partagent ou non une aire de répartition. Une source du département d'agronomie de l'université d'État de l'Iowa indique que les membres d'un groupe d'espèces ont généralement des aires de répartition qui se chevauchent partiellement mais les membres ne se croisent pas entre eux[33]. Un dictionnaire de zoologie (Oxford University Press, 1999) décrit un groupe d'espèces comme un complexe d'espèces apparentées qui existent de manière allopatrique et explique que « le regroupement peut souvent être soutenu par des croisements expérimentaux dans lesquels seules certaines paires d'espèces produiront des hybrides »[34]. Les exemples donnés ci-dessous peuvent soutenir les deux utilisations du terme "groupe d'espèces".
Souvent, l'existence de tels complexes ne deviennent pas évidente jusqu'à ce qu'une nouvelle espèce ne soit introduite dans le système, ce qui fait tomber les barrières existantes entre les espèces d'alors. Un exemple est l'introduction de la limace espagnole en Europe du Nord, où le croisement avec la limace noire et la limace rouge locales, qui étaient traditionnellement considérées comme des espèces clairement distinctes qui ne se sont pas croisées, montre qu'il peut s'agir en fait simplement de sous-espèces de la même espèce[35].
Lorsque des espèces étroitement apparentées coexistent en sympatrie, il est souvent particulièrement difficile de comprendre comment les espèces similaires persistent sans être en compétition entre elles. La différenciation de niche est l'un des mécanismes invoqués pour expliquer cela. En effet, des études menées dans certains complexes d'espèces suggèrent que la divergence des espèces est allée de pair avec la différenciation écologique, les espèces préférant désormais des microhabitats différents[36]. Des méthodes similaires ont également permis de constater que la grenouille amazonienne Eleutherodactylus ockendeni est en fait constituée d'au moins trois espèces différentes qui ont divergé il y a plus de 5 millions d'années[32].
Un "troupeau d'espèces" peut apparaître lorsqu'une espèce pénètre dans une nouvelle zone géographique et se diversifie pour occuper diverses niches écologiques, un processus connu sous le nom de radiation évolutive (adaptive radiation). Le premier troupeau d'espèces à être reconnu comme tel est celui des 13 espèces de pinsons de Darwin des îles Galápagos décrit par Charles Darwin.
Implication pratiques
Estimations de biodiversité
Il a été suggéré que les complexes d'espèces cryptiques sont très communs dans l'environnement marin[37]. Cette suggestion est venue avant l'analyse détaillée de nombreux systèmes en utilisant des données de séquences d'ADN, mais s'est avérée correcte[38]. L'utilisation accrue de la séquence d'ADN dans l'étude de la diversité des organismes (également appelée phylogéographie et barcoding moléculaire) a conduit à la découverte d'un grand nombre de complexes d'espèces cryptiques dans tous les habitats. Chez le bryozoaire marin Celleporella hyalina, des analyses morphologiques détaillées et des tests de compatibilité d'accouplement entre les isolats identifiés par l'analyse des séquences d'ADN ont permis de confirmer que ces groupes étaient constitués de plus de 10 espèces écologiquement distinctes, qui divergeaient depuis plusieurs millions d'années[39].
Les preuves de l'identification d'espèces cryptiques ont conduit certains à conclure que les estimations actuelles de la richesse spécifique mondiale sont trop faibles[40].
Lutte contre les maladies et les agents pathogènes
Les nuisibles, les espèces qui provoquent des maladies et leurs vecteurs, ont une importance directe pour l'humanité. Lorsqu'on découvre qu'il s'agit de complexes d'espèces cryptiques, l'écologie et la virulence de chacune de ces espèces doivent être réévaluées afin d'élaborer des stratégies de lutte appropriées ; par exemple, les espèces cryptiques du genre de moustique Anopheles, vecteur du paludisme, les champignons responsables de la cryptococcose, ou encore les espèces sœurs de Bactrocera tyroni, la mouche des fruits du Queensland. Curieusement, ce ravageur est impossible à distinguer de deux espèces sœurs, sauf que B. tyroni inflige des dégâts considérables et dévastateurs aux cultures fruitières australiennes, alors que ses espèces sœurs non[41].
Voir aussi
Notes
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Species complex » (voir la liste des auteurs).
Références
- Marcel A. Caminer et Santiago R. Ron, « Systematics of treefrogs of the Hypsiboas calcaratus and Hypsiboas fasciatus species complex (Anura, Hylidae) with the description of four new species », ZooKeys, no 370, , p. 1–68 (ISSN 1313-2989, PMID 24478591, PMCID 3904076, DOI 10.3897/zookeys.370.6291, lire en ligne, consulté le )
- József Geml, Rodham E. Tulloss, Gary A. Laursen et Nina A. Sazanova, « Evidence for strong inter- and intracontinental phylogeographic structure in Amanita muscaria, a wind-dispersed ectomycorrhizal basidiomycete », Molecular Phylogenetics and Evolution, vol. 48, no 2, , p. 694–701 (ISSN 1095-9513, PMID 18547823, DOI 10.1016/j.ympev.2008.04.029, lire en ligne, consulté le )
- A. L. Roca, N. Georgiadis, J. Pecon-Slattery et S. J. O'Brien, « Genetic evidence for two species of elephant in Africa », Science (New York, N.Y.), vol. 293, no 5534, , p. 1473–1477 (ISSN 0036-8075, PMID 11520983, DOI 10.1126/science.1059936, lire en ligne, consulté le )
- (en) P. Moran & I. Kornfield, « Retention of an ancestral polymorphism in the Mbuna species flock (Teleostei: Cichlidae) of Lake Malawi », Molecular Biology and Evolution, vol. 10, , p. 1015-1015 (lire en ligne [PDF])
- J K Brown, D R Frohlich et R C Rosell, « The Sweetpotato or Silverleaf Whiteflies: Biotypes of Bemisia tabaci or a Species Complex? », Annual Review of Entomology, vol. 40, no 1, , p. 511–534 (ISSN 0066-4170, DOI 10.1146/annurev.en.40.010195.002455, lire en ligne, consulté le )
- Kevin De Queiroz, « Species concepts and species delimitation », Systematic Biology, vol. 56, no 6, , p. 879–886 (ISSN 1063-5157, PMID 18027281, DOI 10.1080/10635150701701083, lire en ligne, consulté le )
- (en) Ernst Mayr, Populations, Species, and Evolution: An Abridgment of Animal Species and Evolution, Harvard University Press, (ISBN 978-0-674-69013-4, lire en ligne)
- Elvira Hörandl, Johann Greilhuber, Katarina Klímová et Ovidiu Paun, « Reticulate evolution and taxonomic concepts in the Ranunculus auricomus complex (Ranunculaceae): insights from analysis of morphological, karyological and molecular data », Taxon, vol. 58, no 4, , p. 1194–1215 (ISSN 0040-0262, PMID 20401184, PMCID 2855680, lire en ligne, consulté le )
- (en) R. Jong, Superspecies Pyrgus malvae (Lepidoptera: Hesperiidae) in the East Mediterranean, with notes on phylogenetic and biological relationships, Rijksmuseum van Natuurlijke Historie,
- (en) Craig Moritz, Christopher J. Schneider et David B. Wake, « Evolutionary Relationships Within the Ensatina Eschscholtzii Complex Confirm the Ring Species Interpretation », Systematic Biology, vol. 41, no 3, , p. 273–291 (ISSN 1063-5157, DOI 10.1093/sysbio/41.3.273, lire en ligne, consulté le )
- (en) B. W. Bowen, A. L. Bass, L. A. Rocha et W. S. Grant, « Phylogeography of the Trumpetfishes (aulostomus): Ring Species Complex on a Global Scale », Evolution, vol. 55, no 5, , p. 1029–1039 (ISSN 1558-5646, DOI 10.1111/j.0014-3820.2001.tb00619.x, lire en ligne, consulté le )
- Martha M. Muñoz, Nicholas G. Crawford, Thomas J. McGreevy et Nicholas J. Messana, « Divergence in coloration and ecological speciation in the Anolis marmoratus species complex », Molecular Ecology, vol. 22, no 10, , p. 2668–2682 (ISSN 1365-294X, PMID 23611648, DOI 10.1111/mec.12295, lire en ligne, consulté le )
- Ride WD, Cogger HG, Dupuis C, Kraus O, Minelli A, Thompson FC, Tubbs PK, International Code of Zoological Nomenclature, Londres, The International Trust for Zoological Nomenclature, (ISBN 978-0853010067, lire en ligne), chap. 9 (« Genus-group nominal taxa and their names »)
- International Code of Nomenclature of Bacteria: Bacteriological Code, 1990 Revision, ASM Press, (ISBN 978-1-55581-039-9, PMID 21089234, lire en ligne)
- (en) F. R. Barrie et al., International Code of Nomenclature for algae, fungi and plants (Melbourne Code), vol. 154, Königstein: Koeltz Scientific Books, J. McNeill, , 240 p. (lire en ligne)
- (en) Christopher G. Morris, Academic Press Dictionary of Science and Technology, San Diego / Londres, (ISBN 978-0-12-200400-1, lire en ligne), p. 1643
- (en) Ernst Mayr, Systematics and the Origin of Species, from the Viewpoint of a Zoologist, Harvard University Press, (ISBN 978-0-674-86250-0, lire en ligne)
- (en) George C. Steyskal, « The Meaning of the Term ‘Sibling Species’ », Systematic Biology, vol. 21, no 4, , p. 446–446 (ISSN 1063-5157, DOI 10.1093/sysbio/21.4.446, lire en ligne, consulté le )
- S. A. Hodges et M. L. Arnold, « Columbines: a geographically widespread species flock », Proceedings of the National Academy of Sciences of the United States of America, vol. 91, no 11, , p. 5129–5132 (ISSN 0027-8424, PMID 8197196, DOI 10.1073/pnas.91.11.5129, lire en ligne, consulté le )
- (en) Antonio Fontdevila, Carles Pla, Esteban Hasson et Marvin Wasserman, « Drosophila koepferae: a New Member of the Drosophila serido (Diptera: Drosophilidae) Superspecies Taxon », Annals of the Entomological Society of America, vol. 81, no 3, , p. 380–385 (ISSN 0013-8746, DOI 10.1093/aesa/81.3.380, lire en ligne, consulté le )
- Graham P. Wallis et J. W. Arntzen, « MITOCHONDRIAL-DNA VARIATION IN THE CRESTED NEWT SUPERSPECIES: LIMITED CYTOPLASMIC GENE FLOW AMONG SPECIES », Evolution; International Journal of Organic Evolution, vol. 43, no 1, , p. 88–104 (ISSN 1558-5646, PMID 28568488, DOI 10.1111/j.1558-5646.1989.tb04209.x, lire en ligne, consulté le )
- (en) Dean Amadon, « The Superspecies Concept », Systematic Biology, vol. 15, no 3, , p. 245–249 (ISSN 1063-5157, DOI 10.2307/sysbio/15.3.245, lire en ligne, consulté le )
- (en) V. H. Heywood, The "species aggregate" in theory and practice, Montréal, VH Heywood; Löve Á. (eds.). Symposium on Biosystematics, organized by the International Organization of Biosystematists, Montreal, October 1962, , p. 26–36
- (en) Maaria Kankare, Saskya Van Nouhuys et Ilkka Hanski, « Genetic Divergence Among Host-Specific Cryptic Species in Cotesia melitaearum Aggregate (Hymenoptera: Braconidae), Parasitoids of Checkerspot Butterflies », Annals of the Entomological Society of America, vol. 98, no 3, , p. 382–394 (ISSN 0013-8746, DOI 10.1603/0013-8746(2005)098[0382:GDAHCS]2.0.CO;2, lire en ligne, consulté le )
- (en) Graham P. Wallis, Karen F. Judge, Julie Bland et Jonathan M. Waters, « Genetic diversity in New Zealand Galaxias vulgaris sensu lato (Teleostei: Osmeriformes: Galaxiidae): a test of a biogeographic hypothesis », Journal of Biogeography, vol. 28, no 1, , p. 59–67 (ISSN 1365-2699, DOI 10.1046/j.1365-2699.2001.00535.x, lire en ligne, consulté le )
- (en) Y.-C. Dai, E. J. Vainio, J. Hantula et T. Niemelä, « Investigations on Heterobasidion annosum s.lat. in central and eastern Asia with the aid of mating tests and DNA fingerprinting », Forest Pathology, vol. 33, no 5, , p. 269–286 (ISSN 1439-0329, DOI 10.1046/j.1439-0329.2003.00328.x, lire en ligne, consulté le )
- (en) Kobeke Van de Putte, Jorinde Nuytinck, Dirk Stubbe et Huyen Thanh Le, « Lactarius volemus sensu lato (Russulales) from northern Thailand: morphological and phylogenetic species concepts explored », Fungal Diversity, vol. 45, no 1, , p. 99–130 (ISSN 1878-9129, DOI 10.1007/s13225-010-0070-0, lire en ligne, consulté le )
- (en) Dieter Thomas Tietze, Jochen Martens et Yue-Hua Sun, « Molecular phylogeny of treecreepers (Certhia) detects hidden diversity† », Ibis, vol. 148, no 3, , p. 477–488 (ISSN 1474-919X, DOI 10.1111/j.1474-919X.2006.00547.x, lire en ligne, consulté le )
- Isabel Marques, Sean A. Montgomery, Michael S. Barker et Terry D. Macfarlane, « Transcriptome-derived evidence supports recent polyploidization and a major phylogeographic division in Trithuria submersa (Hydatellaceae, Nymphaeales) », The New Phytologist, vol. 210, no 1, , p. 310–323 (ISSN 1469-8137, PMID 26612464, DOI 10.1111/nph.13755, lire en ligne, consulté le )
- S. Steinfartz, M. Veith et D. Tautz, « Mitochondrial sequence analysis of Salamandra taxa suggests old splits of major lineages and postglacial recolonizations of central Europe from distinct source populations of Salamandra salamandra », Molecular Ecology, vol. 9, no 4, , p. 397–410 (ISSN 0962-1083, PMID 10736043, DOI 10.1046/j.1365-294x.2000.00870.x, lire en ligne, consulté le )
- Kathryn R. Elmer, José A. Dávila et Stephen C. Lougheed, « Cryptic diversity and deep divergence in an upper Amazonian leaflitter frog, Eleutherodactylus ockendeni », BMC evolutionary biology, vol. 7, , p. 247 (ISSN 1471-2148, PMID 18154647, PMCID 2254618, DOI 10.1186/1471-2148-7-247, lire en ligne, consulté le )
- (en) Iowa State University Department of Agronomy, « What is a weed? »
- « Species Group | Encyclopedia.com », sur www.encyclopedia.com (consulté le )
- (en-US) « Spanish Slug: How to Identify and Control Spanish Slugs | Tips and Tricks », sur Slughelp, (consulté le )
- (en) A. Borzee et al., « Temporal and spatial differentiation in microhabitat use: Implications for reproductive isolation and ecological niche specification. », Integrative Zoology, 5e série, vol. 11, , p. 375-387 (lire en ligne)
- Nancy Knowlton, « Sibling Species in the Sea », Annual Review of Ecology and Systematics, vol. 24, no 1, , p. 189–216 (ISSN 0066-4162, DOI 10.1146/annurev.es.24.110193.001201, lire en ligne, consulté le )
- (en) N. Knowlton, « Molecular genetic analyses of species boundaries in the sea », Hydrobiologia, vol. 420, no 1, , p. 73–90 (ISSN 1573-5117, DOI 10.1023/A:1003933603879, lire en ligne, consulté le )
- Africa Gómez, Peter J. Wright, David H. Lunt et Juan M. Cancino, « Mating trials validate the use of DNA barcoding to reveal cryptic speciation of a marine bryozoan taxon », Proceedings. Biological Sciences, vol. 274, no 1607, , p. 199–207 (ISSN 0962-8452, PMID 17035167, PMCID 1685843, DOI 10.1098/rspb.2006.3718, lire en ligne, consulté le )
- (en) Martin R. Speight et Peter A. Henderson, Marine Ecology: Concepts and Applications, John Wiley & Sons, (ISBN 978-1-118-68731-4, lire en ligne)
- (en) A. R. Clarke, K. S. Powell, C. W. Weldon et P. W. Taylor, « The ecology of Bactrocera tryoni (Diptera: Tephritidae): what do we know to assist pest management? », Annals of Applied Biology, vol. 158, no 1, , p. 26–54 (ISSN 1744-7348, DOI 10.1111/j.1744-7348.2010.00448.x, lire en ligne, consulté le )
Articles connexes
- Portail de la biologie






.jpg.webp)