Cellule électrochimique
Une cellule électrochimique est un appareil capable de générer de l'énergie électrique à partir de réactions chimiques ou d'utiliser de l'énergie électrique pour provoquer des réactions chimiques. Les cellules électrochimiques qui génèrent un courant électrique sont appelées cellules voltaïques ou cellules galvaniques et celles qui génèrent des réactions chimiques, par électrolyse par exemple, sont appelées cellules électrolytiques[1],[2]. Un exemple courant d'une cellule galvanique est une norme de 1,5 volt[3], cellules destinées à l'usage des consommateurs. Une batterie se compose d'une ou plusieurs cellules, connectées en parallèle, en série ou en série et parallèle.
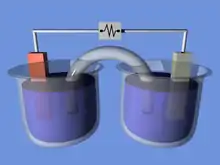
Une configuration de cellule électrochimique de démonstration ressemblant à la cellule Daniell. Les deux demi-cellules sont reliées par un pont salin portant des ions entre elles. Les électrons circulent dans le circuit externe.
Voir aussi
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Electrochemical cell » (voir la liste des auteurs).
- « Electrolytic Cells », hyperphysics.phy-astr.gsu.edu (consulté le )
- « Electrochemical Cells », hyperphysics.phy-astr.gsu.edu (consulté le ) : « Electrochemical cells which generate an electric current are called voltaic cells or galvanic cells, and common batteries consist of one or more such cells. In other electrochemical cells an externally supplied electric current is used to drive a chemical reaction which would not occur spontaneously. Such cells are called electrolytic cells. »
- « Byjus ( a tutorial site) »
- Portail de l’électricité et de l’électronique
- Portail de la chimie
Cet article est issu de Wikipedia. Le texte est sous licence Creative Commons - Attribution - Partage dans les Mêmes. Des conditions supplémentaires peuvent s'appliquer aux fichiers multimédias.