Acétate de potassium
L'acétate de potassium de formule semi-développée CH3COOK est un sel de l'acide acétique et du potassium.
| Acétate de potassium | |
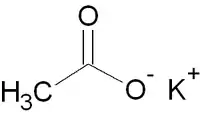
| |
| Identification | |
|---|---|
| Nom UICPA | Éthanoate de potassium |
| No CAS | |
| No ECHA | 100.004.385 |
| No CE | 204-822-2 |
| Code ATC | |
| PubChem | |
| No E | E261 |
| FEMA | 2920 |
| SMILES | |
| InChI | |
| Apparence | poudre blanche déliquescente |
| Propriétés chimiques | |
| Formule | C2H3KO2 |
| Masse molaire[1] | 98,1423 ± 0,0025 g/mol C 24,48 %, H 3,08 %, K 39,84 %, O 32,6 %, |
| Propriétés physiques | |
| T° fusion | 292 °C |
| Solubilité | 2 000 g·kg-1 (eau) |
| Masse volumique | 1,57 g·cm-3, solide |
| Précautions | |
| NFPA 704 | |
| Composés apparentés | |
| Autres cations | Acétate de sodium |
| Unités du SI et CNTP, sauf indication contraire. | |
L'acétate de potassium est un additif alimentaire autorisé en Europe (numéro E261). Il est classé comme conservateur alimentaire et correcteur de pH[2].
La combustion de l'acétate de potassium donne une flamme de couleur bleue.
L'acétate de potassium peut être utilisé pour extraire l'eau du mélange azéotropique éthanol-eau[3]. Le sel réduit la pression vapeur du solvant dans lequel il est le plus soluble. La séparation des solvants se fait ensuite par distillation.
L'acétate de potassium en solution aqueuse (pH faible 8,2) peut être utilisé pour l'extinction d'incendie essentiellement dans les cuisines à cause des huiles et des graisses qui gardent la chaleur. Il forme une mousse comme du savon au contact d'une surface chaude, ce qui étouffe le feu. Il se nettoie facilement et n'est pas toxique.
L'acétate de potassium est également utilisé comme "déglaçant" pour lutter contre le verglas, par exemple sur les pistes de l'aéroport de Montréal-Trudeau[4]. Il est employé en remplacement du sel (NaCl), plus corrosif, et de l'urée, plus toxique.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « Noms de catégorie et système international de numérotation des additifs alimentaires », CAC/GL 361989, sur www.codexalimentarius.net, Codex Alimentarius, (consulté le ), p. 1-35
- Eva-Katrine Hilmen, « Separation of Azeotropic Mixtures: Tools for Analysis and Studies on Batch Distillation Operation », Norwegian University of Science and Technology, Dept. of Chemical Engineering,
- Le Monde du 22/12/2010 "Les recettes de l'aéroport de Montréal pour contrer la neige et le verglas" ainsi que sur le site de l'aéroport de Montréal http://www.admtl.com/APropos/Environnement/AeroEco.aspx
- Portail de la chimie
- Portail de l’hématologie
- Portail de la pharmacie
