Vaccin contre la grippe saisonnière
Le vaccin saisonnier contre la grippe saisonnière (ou influenza) est composé de deux virus de souches A (généralement une souche H1N1 et une autre H3N2) et d'un virus de souche B. Les particules virales contenues dans le vaccin sont inactivées chimiquement[1],[2].
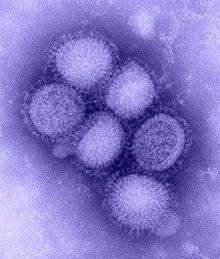
Virus de la grippe
La grippe saisonnière résulte de l'infection par un virus de la famille des orthomixovirus, de la famille des virus ARN simple brin, qui sont naturellement sujet lorsqu'ils sont dupliqués dans les cellules de l'hôte, à des erreurs de réplication de leur matériel génétique, ce qui occasionne des mutations permettant au virus d'échapper au système immunitaire de l'hôte (c'est pourquoi un nouveau vaccin est à produire chaque année, pour pallier de nouvelles résistances du virus face aux anticorps produits par l'organisme[3].
Ce virus est entouré d'une enveloppe contenant deux protéines spécifiques à ce type de virus : l'hémagglutinine et la neuraminidase[4], qui sont construites chacune avec plusieurs petites variations lors de la réplication virale, permettant une grande diversité de souches virales. 19 sous-types d'hémagglutinine et 9 sous types de neuraminidases sont connus.
Depuis les dernières pandémies grippales de 1968 et 1977-78[5], les sous-types circulant les plus courants sont H1 et H3 pour les hémagglutinines et N1 ou N2 pour les neuraminidases. Et les combinaisons H1N1 et H3N2 sont les types de virus A qui circulent le chez l'humain depuis quelques années.
Souches recommandées par l'OMS pour la composition de vaccins contre la grippe saisonnière
Chaque année, l'OMS publie sur son site internet ses recommandations pour la composition des vaccins diffusés dans les hémisphères nord et sud[6]. Les recommandations faites pour la saison grippale suivante (hiver) se basent sur la caractérisation des souches qui circulent dans l'autre hémisphère durant la saison courante : ainsi fin septembre 2013, l'OMS, sur la base des observations au démarrage de la saison grippale de l'hiver 2013-2014 de l'hémisphère nord, a publié ses recommandations pour la saison grippale de l'hiver 2014 de l'hémisphère sud (qui a démarré en février-mars 2014, et permettra quant à elle la publication des recommandations pour l'hiver 2014-2015 de l'hémisphère nord). Ce système vise à détecter l'apparition et/ou la propagation de nouvelles souches et variants, qui seront susceptibles d'infecter un plus grand nombre de personnes (car n'ayant pas encore été en contact avec les nouveaux antigènes), et sur le fait que chacun des deux hémisphères joue le rôle de réservoir infectieux pour l'autre hémisphère, pendant son été (période de quasi absence de circulation du virus dans la population).
Le tableau ci-dessous présente les recommandations de l'OMS pour les années 2008 à 2017[6] :
| Saison
(hémisphère) |
A(H1N1) | A(H3N2) | B | B (tétravalent) |
|---|---|---|---|---|
| 2008 (sud) | A/Solomon Islands/3/2006 | A/Brisbane/10/2007 | B/Florida/4/2006 | |
| 2008-2009 (nord) | A/Brisbane/59/2007 | A/Brisbane/10/2007 | B/Florida/4/2006 | |
| 2009 (sud) | A/Brisbane/59/2007 | A/Brisbane/10/2007 | B/Florida/4/2006 | |
| 2009-2010 (nord) | A/Brisbane/59/2007 | A/Brisbane/10/2007 | B/Brisbane/60/2008 | |
| Year | A(H1N1) pdm09 | A(H3N2) | B | B (tétravalent) |
| 2010 (sud) | A/California/7/2009 | A/Perth/16/2009 | B/Brisbane/60/2008 | |
| 2010-2011 (nord) | A/California/7/2009 | A/Perth/16/2009 | B/Brisbane/60/2008 | |
| 2011 (sud) | A/California/7/2009 | A/Perth/16/2009 | B/Brisbane/60/2008 | |
| 2011-2012 (nord) | A/California/7/2009 | A/Perth/16/2009 | B/Brisbane/60/2008 | |
| 2012 (sud) | A/California/7/2009 | A/Perth/16/2009 | B/Brisbane/60/2008 | |
| 2012-2013 (nord) | A/California/7/2009 | A/Victoria/361/2011 | B/Wisconsin/1/2010 | |
| 2013 (sud) | A/California/7/2009 | A/Victoria/361/2011 | B/Wisconsin/1/2010 | |
| 2013-2014 (nord) | A/California/7/2009 or A/Christchurch/16/2010 | A/Texas/50/2012 or A/Victoria/361/2011 | B/Massachusetts/2/2012 | B/Brisbane/60/2008 or B/Brisbane/33/2008 |
| 2014 (sud) | A/California/7/2009 or A/Christchurch/16/2010 | A/Texas/50/2012 or A/Victoria/361/2011 | B/Massachusetts/2/2012 | B/Brisbane/60/2008 |
| 2014-2015 (nord) | A/California/7/2009 | A/Texas/50/2012 | B/Massachusetts/2/2012 | B/Brisbane/60/2008 |
| 2015 (sud) | A/California/7/2009 | A/Switzerland/9715293/2013 | B/Phuket/3073/2013 | B/Brisbane/60/2008 |
| 2015-2016 (nord) | A/California/7/2009 | A/Switzerland/9715293/2013 | B/Phuket/3073/2013 | B/Brisbane/60/2008 |
| 2016 (sud) | A/California/7/2009 | A/Hong Kong/4801/2014 | B/Brisbane/60/2008 | B/Phuket/3073/2013 |
| 2016-2017 (nord) | A/California/7/2009 | A/Hong Kong/4801/2014 | B/Brisbane/60/2008 | B/Phuket/3073/2013 |
| 2017 (sud) | A/Michigan/45/2015 | A/Hong Kong/4801/2014 | B/Brisbane/60/2008 | B/Phuket/3073/2013 |
| 2017-2018 (nord) | A/Michigan/45/2015 | A/Hong Kong/4801/2014 | B/Brisbane/60/2008 | B/Phuket/3073/2013 |
| 2018 (sud) | A/Michigan/45/2015 | A/Singapore/INFIMH-16-0019/2016 | B/Phuket/3073/2013 | B/Brisbane/60/2008 |
À partir de la saison de l'hémisphère nord 2013-2014, l'OMS recommande l'utilisation de vaccins quadrivalents, associant deux souches B.
Chaque changement dans la composition recommandée traduit l'émergence d'une nouvelle souche, susceptible d'infecter une large partie de la population.
On note ainsi sur ce tableau la prise en compte à partir de 2010 du nouveau virus A(H1/N1) pdm09 lié à la pandémie grippale de 2009, souche notée A/California/7/2009, et à partir de 2018, de l'apparition d'une nouvelle souche H3N2 à l'origine de l'épidémie de grippe importante de l'hiver 2017-2018 dans l'hémisphère nord. Cette souche n'ayant pas été incluse dans les vaccins de la saison 2017-2018, les personnes vaccinées en début de saison grippale 2017-18 n'ont pas bénéficié d'une protection optimale contre ces nouveaux variants (mutation N121K dans l'hémagglutinine, et modifications antigéniques dans la neuraminidase)[7].
Fabrication du vaccin contre la grippe
Le virus est tout d'abord cultivé en grande quantité en l'inoculant dans des œufs embryonnés de poule, qui servent de lieu de reproduction. Par la suite, les particules virales sont inactivées par des solutions chimiques telles le formaldéhyde et le β-propiolactone.
La liste suivante[8] détaille les excipients présents dans les vaccins antigrippaux communs :
- Celvapan (A-H1N1 2009) : formaldéhyde, trométamol(d), Benzonase, polysorbate 80, ovalbumine (œuf) et protéines de poulet
- Focetria (A-H1N1 2009) : formaldéhyde, bromure de cétrimonium, kanamycine(a), néomycine(a), squalène, ovalbumine (œuf) et protéines de poulet
- Pandemrix (A-H1N1 2009): formaldéhyde, gentamicine(a), mercurothiolate sodique(b), désoxycholate de sodium, octoxinol 9, squalène, polysorbate 80(c), ovalbumine (œuf) et protéines de poulet
- Agrippal : formaldéhyde, bromure de cétrimonium, kanamycine(a), néomycine(a), polysorbate 80(c), ovalbumine (œuf) et protéines de poulet
- Fluarix : formaldéhyde, gentamicine(a), mercurothiolate sodique(b), désoxycholate de sodium, octoxinol 9, polysorbate 80(c), ovalbumine (œuf) et protéines de poulet
- Fluvirine : bêta-propiolactone, formaldéhyde, néomycine(a), polymyxine B(a), mercurothiolate sodique(b), nonoxinol 9, ovalbumine (œuf) et protéines de poulet
- Gripguard : formaldéhyde, kanamycine(a), néomycine(a), bromure de cétrimonium, squalène, adjuvant MF59C.1 (mélange de polysorbate 80, squalène, trioléate de sorbitan, citrate de sodium, acide citrique et eau), ovalbumine (œuf) et protéines de poulet
- Immugrip : formaldéhyde, néomycine(a), octoxinol 9, ovalbumine (œuf) et protéines de poulet
- Influvac : formaldéhyde, bromure de cétrimonium, gentamicine(a) néomycine(a), mercurothiolate sodique(b), polysorbate 80(c), ovalbumine (œuf) et protéines de poulet
- Intanza : formaldéhyde, néomycine(a), octoxinol 9, ovalbumine (œuf) et protéines de poulet
- Mutagrip : formaldéhyde, néomycine(a), octoxinol 9, ovalbumine (œuf) et protéines de poulet
- Previgrip : formaldéhyde, éther éthylique, polymyxine B(a), polysorbate 80(c), ovalbumine (œuf) et protéines de poulet
- Tetagrip : formaldéhyde, néomycine(a), octoxinol 9, anatoxine/protéine tétanique (comme adjuvant), ovalbumine (œuf) et protéines de poulet
- Vaxigrip : formaldéhyde, néomycine(a), octoxinol 9, ovalbumine (œuf) et protéines de poulet
Remarques : (a) : antibiotiques ; (b) : dérivé du mercure, antiseptique et inhibiteur de certaines enzymes ; (c) : contre-indiqués en cas d'intolérance au fructose ; (d) : alcalinisant et irritant pour les cellules.
Pour ce qui est du choix des souches virales, il est effectué par l'Organisation mondiale de la santé (OMS) qui fait un suivi des épidémies mondiales de grippe tout au long de l'année. Elle choisit ensuite les souches les plus à risque d'émerger et de causer une épidémie[9]. Cela peut parfois permettre la production de vaccin très efficace lorsque le virus choisi pour la fabrication du vaccin est identique aux réelles souches émergentes. Il peut parfois arriver que les souches qui causent les épidémies soient différentes de celles attendues, ce qui n'amène aucune protection pour les gens vaccinés, car les anticorps produits grâce au vaccin ne réagissent pas avec le virus réel.
Mode d'action du vaccin
Étant donné que le vaccin contre la grippe ne contient que des virus inactivés (tués), l'ajout d'un adjuvant est de mise afin de permettre la mise en place d'une réponse immunitaire assez forte pour permettre la production d'anticorps et de cellules mémoires. Le virus lui-même n'est pas capable d'engendrer une réponse immunitaire forte, car il ne peut pas se répliquer dans les cellules qu'il infecte et ne représente donc pas de danger imminent pour l'hôte. Le rôle de l'adjuvant présent dans le vaccin est de présenter le virus de façon adéquate aux cellules du système immunitaire afin d'activer à la fois la réponse humorale et la réponse cellulaire[2]. Cela permet la formation d'une plus grande quantité d'anticorps, majoritairement des anti-hémagglutinines[10], et il permet également la formation de lymphocytes mémoires qui, grâce à leur durée de vie allongée et leur facilité d'activation, permettront au système immunitaire de réagir plus rapidement et plus efficacement lors d'une rencontre ultérieure avec le même virus ou un virus similaire. Plus la ressemblance entre les deux virus est grande, meilleure sera la réponse immunitaire[11].
Les vaccins actuellement commercialisés en France, ne contiennent pas d'adjuvant.[12]
Effets indésirables
Cette section ne cite pas suffisamment ses sources (décembre 2013). Pour l'améliorer, ajoutez des références vérifiables [comment faire ?] ou le modèle {{Référence nécessaire}} sur les passages nécessitant une source. |
Des symptômes peuvent survenir 12 à 48 heures après vaccination. On peut constater une fièvre et un état grippal qui se dissipe généralement très vite.
Les adjuvants comme l'aluminium[13] et le squalène sont de plus en plus dénoncés par les dernières recherches.
Personnes à risque
En France, la vaccination contre la grippe est recommandée pour les personnes de plus de 6 mois appartenant à un groupe à risque de complications[14] (personnes âgées de plus de 65 ans, personnes atteintes d’asthme sévère ou de maladies pulmonaires chroniques, personnes présentant une faiblesse immunitaire grave).
Les personnes les plus visées par les campagnes de vaccination saisonnière contre la grippe sont :
- les jeunes enfants entre 6 et 23 mois, car leur système immunitaire est fonctionnel mais encore immature étant donné qu'ils ont peu été en contact avec des virus, dont celui de la grippe,
- les personnes atteintes de maladies chroniques (des maladies nécessitant un suivi médical), comme les maladies cardiaques, l'asthme, l'emphysème, la fibrose kystique, le diabète, etc., car leur système immunitaire est diminué par la lutte constante contre leur propre maladie,
- les femmes enceintes en étant à leur deuxième ou troisième trimestre de grossesse, car la grippe pourrait avoir des conséquences néfastes sur le développement ou la santé du fœtus en plus d'être plus dommageable pour la mère,
- les femmes enceintes souffrant de maladies chroniques quel que soit le stade d'avancement de leur grossesse,
- les personnes âgées de plus de 65 ans, car avec l'âge, la mémoire du système immunitaire est moins efficace, les cellules mémoires survivent moins longtemps dans l'organisme et l'efficacité de réponse du système immunitaire en général est moins grande.
De plus, la vaccination est fortement recommandée pour les personnes dans l'entourage d'un bébé de moins de 6 mois, car son système immunitaire est encore immature, l'entourage d'une personne immunodéprimée car cette dernière a un système immunitaire affaibli qui serait incapable de s'opposer à une infection virale. Les travailleurs de la santé devraient également se faire vacciner car ils sont très à risque de contracter le virus dans leur milieu de travail. Cette vaccination a pour but de diminuer les risques de transmettre le virus à des gens qui sont plus susceptibles de développer de graves problèmes de santé lors d'une infection par le virus de la grippe, car ils ne seraient pas capables de se défendre contre l'infection et pourraient développer une forme plus grave de la grippe[1]. Il a également été prouvé que la quantité d'anticorps antigrippaux dans l'organisme chute rapidement après six mois, d'où, encore une fois, la nécessité de la vaccination à chaque année pour rebâtir la mémoire du système immunitaire[1].
Une des questions posées et sans vraie réponse, à ce stade, est l'intérêt de la vaccination des personnels de l'enseignement. Cette question est posée, car les lieux d'enseignement sont des lieux fréquents d'explosion virale d'une part, d'autre part, depuis la multiplication des voyages scolaires, notamment à l'étranger, ce peut aussi être un lieu de réarrangement viral.
Efficacité et utilité du vaccin annuel
Le vaccin antigrippal ne peut jamais être prédictif ni efficace à 100 %, car les souches virales en circulation évoluent et se recombinent régulièrement ; elles ne seront donc jamais exactement identiques à celles inoculées par la vaccination. Plus les ressemblances sont grandes, meilleure est l'efficacité de la protection, car les anticorps produits grâce au vaccin ciblent alors mieux les virus qui infectent l'organisme[9].
Faute de temps et de moyens pour réaliser des études randomisées en double aveugle évaluant l'efficacité d'un nouveau vaccin saisonnier sur un échantillon significatif de vrais patients évaluées sur des critères cliniques, l'autorisation de mise sur le marché (AMM) est chaque année délivrée par les autorités sanitaires sur la base de la seule « efficacité sérologique » estimée d’après le taux d'anticorps titrés au cours d’essais cliniques limités[15].
L'utilité et l'efficacité écoépidémiologique du vaccin anti-grippe pour la population générale ne peuvent donc être évaluées qu'après la vague de grippe saisonnière (...au mieux par rapport aux année précédentes, et à ce jour sans comparaison possible avec un groupe témoin non vacciné ou un groupe exposé à l'effet placebo. Son efficacité est donc généralement appréciée par des calculs et simulations dont les résultats dépendent beaucoup des hypothèses choisies).
Dans un cas de figure, l'efficacité vaccinale est plus facile à évaluer : celui de quelques populations mieux suivies ou pour les patients en consultations ambulatoires (hospitalisations courtes où le diagnostic peut être validé par un test permettant d'identifier la souche du virus en cause ; dans ces cas, selon une méta-analyse publiée par The Lancet en 2012, l'efficacité du vaccin varie de 40 à 60% [16], voire est presque nulle comme durant l’hiver 2014-2015 où le vaccin n'a pas même pu protéger 10% des vaccinés[17],[18].
La protection offerte par ce vaccin dépend d'au moins 3 facteurs :
- l'adéquation entre les souches utilisées pour produire le vaccin et les souches circulant réellement durant la saison grippale (Ainsi en France en 2015-2016, il y a eu une « inadéquation entre la souche B/Yamagata contenue dans le vaccin 2015-2016 et la souche circulante B/Victoria »[19]) ;
- du type de virus infectant un patient ou dominant parmi les virus en circulation. Ainsi ;
- l'efficacité contre l'influenza A/H1N1 est en moyenne de 61 % ;
- l'efficacité contre l'influenza B,1 est en moyenne de 54 % ;
- mais elle a chuté à 33 % en moyenne contre l’influenza A/H3N2 selon une méta-analyse publiée par The Lancet en 2016 [20], ce qui est problématique car la souche A/H3N2 était la cause de plus des trois quarts des hospitalisations[21] et de la mortalité induite par la grippe annuelle aux Etats-Unis[22]. - du « terrain » de la personne vaccinée, c'est à dire de facteurs dépendant de l'âge, de l'état de santé et des antécédents médicaux du patient concerné. Le vaccin offre une meilleure protection aux adolescents et aux adultes en bonne santé, car leur système immunitaire est plus apte à produire une réponse immune efficace contre la souche vaccinale et contre le virus naturel[9]. Pour les jeunes enfants (au système immunitaire fonctionnel mais encore immature) et pour les personnes âgées (au système immunitaire moins performant) ou pour les immunodéprimés le vaccin permettra surtout de diminuer la durée et l'intensité des symptômes dans le cas d'une grippe suffisamment ultérieure à la vaccination[9].
Réémergence d'anciennes souches grippales
Un autre point important en faveur de la vaccination saisonnière est la réémergence d'anciennes souches virales très contagieuses et/ou hautement pathogènes de grippe. Ainsi a-t-on montré une grande similitude entre l'hémagglutinine du virus H1N1 de 2009 et celui de la grippe espagnole de 1918[23],[24] qui a fait des millions de mort à travers le monde. La population actuelle n'ayant jamais été en contact avec ce virus, elle n'a aucun anticorps ciblant ce virus. C'est la raison pour laquelle une vaccination de masse fut mise en place. un autre risque est la réémergence d'un virus H2N2 pour lequel la population n'a pas été en contact depuis la « grippe asiatique de 1957 » (seconde pandémie grippale du XXe siècle, qui a probablement fait 2 millions de morts)[réf. nécessaire].
Ces réémergences sont possible grâce à l'existence de réservoirs animaux et/ou de recombinaisons virales (« réassortiment »). La grippe est une zoonose, c'est à dire que ses virus touchent à la fois des humains et certains taxons animaux (oiseaux et certains mammifères non-humains, éventuellement porteurs asymptomatiques). Dans ces réservoirs (a priori principalement porcins et aviaires) les virus se dupliquent et mutent puis peuvent être retransmis à l'homme qui ne dispose pas toujours des anticorps efficaces contre les virus aux protéines mutées. La vaccination vise à faire produite par l'organisme des anticorps aptes à cibler ces protéines mutées avant que le vrai virus n'infecte l'hôte, afin que ce dernier puisse se défendre adéquatement contre l'infection virale. Mais cette vaccination ne sera efficace que si la souche du virus qui infecte le patient est l'une de celles prévues par les fabricants du vaccin de l'année, et si le virus n'a pas significativement à nouveau muté depuis le moment où le vaccin a été produit.
Vers un vaccin universel ?
Cette section ne cite pas suffisamment ses sources (août 2012). Pour l'améliorer, ajoutez des références vérifiables [comment faire ?] ou le modèle {{Référence nécessaire}} sur les passages nécessitant une source. |
Les compagnies pharmaceutiques[Lesquelles ?] cherchent à créer un vaccin universel contre la grippe, qui serait capable de reconnaître tous les virus d'une même souche voire ceux de toutes les souches[25].
Les recherches portent notamment sur l'utilisation d'un deuxième vaccin pour permettre une activation plus grande du système immunitaire, ou sur un vecteur antiviral qui contiendrait le gène codant une partie constante de la protéine hémagglutinine qui semble concentrer les mutations observables dans certaines zones d'hyper-variabilité au sein de la structure de la protéine, alors que d'autres zones sont hautement conservées. Ce sont ces zones qui sont encodées dans les vecteurs et contre lesquelles les anticorps sont formés[25].
Plusieurs anticorps (dont CR9114) capables de neutraliser différents sous-types de virus de la grippe B ont été découverts[25], mais comme dans les cas du VIH (virus de l’immunodéficience humaines) et du virus de l’hépatite B qui mutent également sans cesse pour échapper au système immunitaire de leur hôte[25], construire un vaccin universel nécessite encore de mieux comprendre toutes les interactions entre le virus et les cellules du système immunitaire.
Divers
Ce vaccin fait partie de la liste des médicaments essentiels de l'Organisation mondiale de la santé (liste mise à jour en avril 2013)[26].
Notes et références
- http://www.msss.gouv.qc.ca/sujets/prob_sante/influenza/index.php?vaccination
- (en) http://www.nature.com/icb/journal/v89/n3/full/icb2010152a.html
- (en) https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2643340/?tool=pmcentrez
- [PDF] http://nlsn.free.fr/grippe/grippe.pdf
- Jeffery K. Taubenberger et John C. Kash, « Influenza Virus Evolution, Host Adaptation, and Pandemic Formation », Cell Host & Microbe, vol. 7, no 6, , p. 440–451 (DOI 10.1016/j.chom.2010.05.009, lire en ligne)
- (en) « WHO recommendations on the composition of influenza virus vaccines », sur www.who.int (consulté le 10 octobre 2013)
- (en) « Recommended composition of influenza virus vaccines for use in the 2018 southern hemisphere influenza season », sur who.int, (consulté le 9 janvier 2018)
- http://www.infovaccin.fr/composants.html
- http://www.msss.gouv.qc.ca/sujets/prob_sante/influenza/index.php?foire_aux_questions#logo_msss
- L'influenza - Maladies évitables par la vaccination - Agence de la santé publique du Canada
- http://www.phac-aspc.gc.ca/im/vpd-mev/influenza-fra.php
- Isabelle Cochois, « Vaccination contre la grippe 2017-2018 : en pratique », Dictionnaire Vidal, (lire en ligne)
- https://www.sciencesetavenir.fr/sante/alerte-a-la-toxicite-de-l-aluminium_28665, "Alerte à la toxicité de l'aluminium", Loïc Chauveau, sciencesetavenir.fr, 04.03.2015
- (fr)https://www.grippenet.fr/fr/la-grippe/le-vaccin/
- Morer I & Cano F (2008) Actualisation annuelle des vaccins grippaux : production, contrôle, AMM. XIIIème Journée Nationale des GROG – Paris, le 13 novembre
- Osterholm M.T, Kelley N.S, Sommer A & Belongia E.A (2012). Efficacy and effectiveness of influenza vaccines : a systematic review and meta-analysis | Lancet Infect Dis. |;12(1):36-44
- British Columbia Center for Disease Control () Canadian Sentinel Practitioner Surveillance Network (SPSN) vaccine effectiveness (VE) estimates against laboratory-confirmed medically-attended influenza, 2004-05 to 2015-16 seasons
- Skowronski D.M, Chambers C, Sabaiduc S, De Serres G, Winter A.L, Dickinson J.A et al. A perfect storm : Impact of genomic variation and serial vaccination on low influenza vaccine effectiveness during the 2014-15 season. Clin Infect Dis. 2016 ;63(1):21-32.
- Janin H (2017) La grippe durant l’épidémie 2015-2016 : caractère tardif, gravité clinique et émergence du virus B Victoria |Thèse Université de Bordeaux ; Médecine humaine et pathologie. 2017〈dumas-01611698〉
- Belongia E.A et al. (2016 ) Variable influenza vaccine effectiveness by subtype : a systematic review and meta-analysis of test-negative design studies. Lancet Infect Dis. ;16(8):942-51.
- Thompson W. et al. (2004) Influenza-associated hospitalizations in the United States. JAMA;292(11):1333-40
- Thompson W.et al. (2003) Mortality associated with influenza and respiratory syncytial virus in the United States. JAMA. ;289(2):179-86
- (en) http://www.nature.com/nature/journal/v471/n7337/full/471157a.html
- (en) http://www.nature.com/ncomms/journal/v1/n3/full/ncomms1026.html
- Dreyfus C (2013) Vers un vaccin universel contre la grippe ?. médecine/sciences, 29(1), 22-25.
- WHO Model List of Essential Medicines, 18th list, avril 2013
Voir aussi
Articles connexes
- Portail de la médecine
- Portail de la virologie