Tartrate
Le dianion tartrate est l'ion de formule brute C4H4O62− et semi-développée −OOC-(CHOH)2-COO−. C'est la base conjuguée de l'acide tartrique, un acide dicarboxylique. On appelle aussi tartrate un sel ou un ester de l'acide tartrique. Le sel le plus commun est le (2R,3R)-bitartrate de potassium, un énantiomère présent dans le raisin et le vin[1].
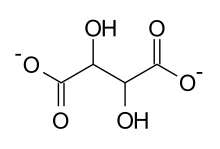
Structure du dianion tartrate
En 1848, Louis Pasteur a découvert la résolution chirale dans la cristallisation du tartrate double de sodium et d'ammonium tétrahydraté racémique[1].
Les sels paratartrates (rac-tartrates, racémates) sont les sels de l'acide tartrique racémique.
Les ions tartrates sont utilisés dans la liqueur de Fehling pour tester la présence d'aldéhydes.
Exemples
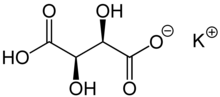
(+)-(R,R)-Bitartrate de potassium.

Tartrate de dipotassium.

Résidus de tartre après nettoyage cuves.
- tartrates de sodium, E335 :
- tartrates de potassium, E336 :
- bitartrate de potassium (tartrate de monopotassium, « crème de tartre », un sous-produit de la vinification), E336(i) ;
- tartrate de dipotassium (en), E336(ii) ;
- tartrate double de sodium et de potassium (sel de Seignette, un sel double), E337 ;
- tartrate de calcium, E354 ;
- tartrate de stéaryle (en) (tartrate de stéaryle palmityle), E483 ;
- tartrate de choline, E1001(v).
- Sels
- acétotartrate d'aluminium (en) ;
- tartrate d'antimoine et de potassium ;
- tartrate ferreux (en).
- Esters
- tartrate de diéthyle ;
- tartrate de diisopropyle (en).
Références
- (en) H. D. Flack, « Louis Pasteur's discovery of molecular chirality and spontaneous resolution in 1848, together with a complete review of his crystallographic and chemical work », Acta Crystallogr. Sect. A, vol. 65, , p. 371–389 (PMID 19687573, DOI 10.1107/S0108767309024088, lire en ligne [PDF], consulté le ).
- Codex Alimentarius, vol. 1A, , 2e éd. (lire en ligne), p. 143,170.
Voir aussi
- Portail de la chimie
- Alimentation et gastronomie
- Portail de la vigne et du vin
Cet article est issu de Wikipedia. Le texte est sous licence Creative Commons - Attribution - Partage dans les Mêmes. Des conditions supplémentaires peuvent s'appliquer aux fichiers multimédias.