Sarcoïdose
La sarcoïdose ou maladie de Besnier-Boeck-Schaumann (communément dénommée BBS) ou lymphogranulomatose bénigne est une maladie inflammatoire systémique de cause inconnue. Elle atteint préférentiellement les poumons, mais peut atteindre n'importe quel autre organe, notamment la peau ou les ganglions lymphatiques. La sarcoïdose se manifeste par la présence d'amas de cellules inflammatoires nommés granulomes, avec des conséquences variables selon les organes touchés.
Pour les articles homonymes, voir BBS.
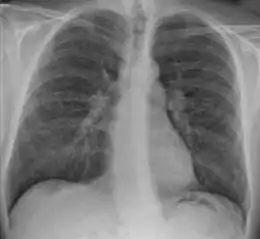
| Spécialité | Hématologie, dermatologie, pneumologie et ophtalmologie |
|---|
| CIM-10 | D86 |
|---|---|
| CIM-9 | 135 |
| OMIM | 181000 |
| DiseasesDB | 11797 |
| MedlinePlus | 000076 |
| eMedicine | 301914 |
| eMedicine | med/2063 |
| MeSH | D012507 |
| Symptômes | Toux et dyspnée |
| Traitement | Ibuprofène et méthotrexate |
| Patient UK | Sarcoidosis-pro |
![]() Mise en garde médicale
Mise en garde médicale
Généralement sans gravité, elle guérit spontanément sauf chez 20 % des malades chez lesquels elle provoque des complications respiratoires menaçantes en évoluant vers une fibrose pulmonaire[1],[2], ce qui justifie un diagnostic précoce et un suivi régulier basés sur l'observation clinique, immunologique et radiologiques.
Il n'existe pas à ce jour de traitement spécifique, et les indications pour commencer un traitement sont rares.
Épidémiologie
La sarcoïdose touche des hommes ou femmes de tout âge (généralement entre 30 et 50 ans) et de toute origine ethnique.
Une étude conduite à Détroit, aux États-Unis, relève que la population noire est plus souvent touchée[3] avec une prédominance féminine. Les formes de sarcoïdose dans ces populations sont en outre plus graves[4]. Chez les Blancs, on note une égale fréquence de survenue chez les hommes et chez les femmes[réf. nécessaire].
Son incidence varie sur la planète, avec, par exemple, pour l'Europe, un gradient nord-sud (640 pour 100 000 habitants en Suède contre 0,4 pour 100 000 habitants en Espagne)[réf. nécessaire], un gradient sud-nord aux États-Unis (proportion de noirs-américains plus importante au sud). Son incidence tend à augmenter, même si l'hypothèse d'un meilleur dépistage ne peut être écartée[5].
En France, la prévalence est de 10 pour 100 000 habitants[réf. nécessaire].
Dans la plupart des cas, la sarcoïdose affecte l'interstitium pulmonaire et les ganglions médiastinaux.
Causes
Elles sont généralement inconnues et éventuellement multiples.
- L'inhalation de poussières ou de certaines particules (poudre/pigment de toner par exemple) peut être en cause[6].
- La présence d'anticorps ciblant les bactéries du genre Borrelia est souvent retrouvée[7] ce qui laisse supposer que la maladie de Lyme (à la suite d'une piqure de tique) peut être une cause ou un facteur favorisant. Cette supposition a été confortée par une étude japonaise du Département d'ophtalmologie, la ville de Yokohama University School of Medicine, au Japon[8]. Selon cette étude plus du tiers des malades étaient infectés par la borréliose de type Borrelia burgdorferi.
- L'exposition à des insecticides ou une vie en milieu agricole est un facteur de risque[9]. L'exposition à d'autres toxiques diffus dans les poussières inhalées pourrait jouer un rôle, avec, par exemple, une augmentation de la fréquence de la maladie chez les pompiers intervenus lors des attentats du World Trade Center[10].
- Se faire tatouer, rarement a été relié à une sarcoïdose, sans que le mécanisme ou un lien direct de cause à effet ait pu être expliqué[11],[12], jusqu'à 30 ans plus tard et y compris pour des tatouages cosmétiques[13], la maladie pouvant présenter une forme localisée ou systémique[14].
- Le tabagisme a été mis en cause par une étude [9].
- Il existe enfin probablement un facteur génétique : il existe des formes familiales[15], chez des jumeaux[16] et un risque multiplié par cinq si un membre proche de la famille est atteint[17]. Une mutation sur le gène BTNL2[18] codant une immunoglobuline, ou sur le ANXA11[19] pourrait intervenir dans le développement de la maladie. La gravité de la maladie semble dépendre de certains groupes HLA, ceux porteurs du HLA-DRB1*03 ayant des formes avec guérison spontanée et ceux du HLA-DRB1*14 ou HLA-DRB1*15, des formes plus chroniques[20].
Physiopathologie
Le mécanisme de la survenue de la maladie reste flou. L'une des hypothèses fait intervenir une immunité à médiation cellulaire contre un antigène, pour l'instant inconnu, sur un terrain génétique prédisposé[21]. L'un des possibles antigènes serait une mycobactérie, de l'ADN mycobactérien étant fréquemment associé aux cas de sarcoïdoses[22],[23] et une catalase-peroxydase mycobactérienne étant identifiée dans la moitié des cas[24].
Les mécanismes immunologiques responsables de la sarcoïdose sont connus. La chronologie de l’inflammation sarcoïdosique a été particulièrement bien étudiée au niveau du poumon. Elle se caractérise par des désordres immunologiques, qui expliquent ses répercussions sur l’organisme. On distingue trois phases différentes qui se succèdent : l’alvéolite lymphocytaire et macrophagique, la phase granulomateuse, et finalement la fibrose (facultative).
L’alvéolite lymphocytaire et macrophagique
Le système immunitaire produit une réponse très forte à un antigène inconnu, ce qui entraîne :
- une accumulation de lymphocytes CD4+ activés qui se concentrent dans les alvéoles du poumon, provoquant une alvéolite. Ces lymphocytes sécrètent des médiateurs pro-inflammatoires (notamment l’interleukine 2 et le facteur chimiotactique des monocytes MCP-1) ;
- ils entraînent aussi une activation des lymphocytes B, qui sécrètent en réponse des anticorps (les gammaglobulines) ;
- des macrophages activés sont attirés par l'activation des lymphocytes CD4.
La phase granulomateuse
- les macrophages activés s'accumulent aussi dans le poumon. Ils sécrètent notamment l'enzyme de conversion de l'angiotensine et forment des granulomes tuberculoïdes ;
- une anergie tuberculinique est fréquente (absence de réaction du corps au test de la tuberculose malgré une vaccination par le BCG), liée à une lymphopénie (baisse du nombre de lymphocytes « normaux », mais il n'y a pas d'immunodépression).
La fibrose
À terme, les granulomes entraînent une fibrose pulmonaire, principale complication pulmonaire de la sarcoïdose.
Signes cliniques
L'atteinte des poumons est quasi constante : il y a 90 % de risque que les poumons soient atteints[5]. Cependant les symptômes tels que des douleurs à la poitrine, essoufflements ou une toux sèche ne se manifestent que chez 33 % des personnes concernées.
Chez 33 % des personnes atteintes on observe une inflammation des ganglions.
La peau est atteinte dans un tiers des cas[21], avec apparition de petites boules de couleur rouge, très douloureuses (érythème noueux), avec — éventuellement — des taches ou plaques d'aspect peu spécifique. La reconnaissance des lésions cutanées est importante car la biopsie de ces dernières est facile et amène le diagnostic.
L’œil est touché dans 10 à 25 % des cas, avec rougeur, vision floue, démangeaisons. Ces signes correspondent à une uvéite granulomateuse, typiquement antérieure et chronique. L'examen à la lampe à fente montre des précipités rétro-descemétiques, des adhérences (synéchies), des nodules de l'iris[25]. Une conjonctivite, une uvéite intermédiaire ou postérieure très exsudative avec présence de granulome au fond d’œil peuvent y être associées.
Les douleurs articulaires sont fréquentes. Elles sont dues à des arthrites (inflammation des articulations). Une augmentation du taux de calcium sanguin (hypercalcémie) n’est présente que dans 5 % des cas. Cela peut entraîner une fatigue importante et des nausées.
L’atteinte du cœur se voit dans 4 cas sur 10[26]. Sa fréquence est en fait variable selon les pays : comprise entre 20 % et 27 % aux États-Unis et allant jusqu'à 58 % au Japon. Le taux de mortalité de se chiffre à 40 % après 5 ans [27] Elle peut être silencieuse ou se manifester par des malaises, des signes d'insuffisance cardiaque, voire, une mort subite[28]. L'échocardiographie et l'IRM cardiaque peuvent montrer des anomalies non spécifiques.
L’atteinte du foie représente 20 % des cas. Cependant il n’y a pas souvent de symptômes (10 %).
Les signes observés, entre autres, dans le cas d'une neurosarcoïdose (atteinte cérébrale / système nerveux), peuvent être des vertiges rotatoires, perte d'équilibre, ceci étant une des formes les plus complexes et les plus graves de la sarcoïdose. Cette atteinte n'est décrite que dans moins d'un cas sur dix[29]. Un syndrome dépressif peut se voir en France dans un peu moins d'1/2 cas[21].
On peut observer une insuffisance rénale, des formations de calculs dans les urines ou une inflammation du nez et des sinus.
Dans sa forme typique, le syndrome de Löfgren associant érythème noueux, polyadénopathie et douleurs articulaires diffuses, suffit à faire poser le diagnostic sans que cela nécessite d'autres examens complémentaires.
Diagnostic
Le diagnostic n'est guère évident et peut être retardé, particulièrement dans les formes uniquement pulmonaires où le délai peut dépasser six mois[30].
L'établissement du diagnostic nécessite le recueil d'éléments de plusieurs ordres :
- cliniques : signes présentés par le patient (souvent aucun) ;
- radiologiques, presque constamment présents[31], où on distingue quatre stades :
- stade 1 : adénopathies médiastinales bilatérales et symétriques,
- stade 2 : adénopathies médiastinales et infiltrat/micronodules interstitiels,
- stade 3 : infiltrat/micronodules interstitiels sans adénopathies médiastinales,
- stade 4 : fibrose ;
- biologiques : absence de syndrome inflammatoire (sauf cas du syndrome de Löfgren), lymphopénie (diminution du nombre des lymphocytes), hypercalcémie (élévation de la concentration sérique de calcium libre) et hypercalciurie (élévation de la concentration urinaire de calcium), élévation de la concentration sérique de l'enzyme de conversion de l'angiotensine (inconstante et spécificité faible[5]) ;
- histologiques : la biopsie d'un granulome est nécessaire pour poser le diagnostic, sauf s'il existe un syndrome de Löfgren qui suffit à poser le diagnostic. On cherche le granulome le plus facilement accessible (peau, glande salivaire, adénopathie, bronches) dont l’étude microscopique objective un granulome sans nécrose caséeuse. En l'absence de lésions facilement accessibles, une médiastinoscopie peut être proposée, cette dernière pouvant être remplacée par une biopsie par fibroscopie bronchique et guidage par échographie endobronchial[32]. La tomographie par émission de positons permet de détecter des atteintes non évidentes[33] et d'orienter une biopsie ;
- le lavage bronchoalvéolaire (LBA) se caractérise par une hyperlymphocytose à lymphocytes CD4 dans les alvéoles pulmonaires (accumulation des lymphocytes dans les poumons) avec un rapport CD4/CD8 supérieur à 3,4.
Le scanner thoracique, plus précis, peut avantageusement remplacer la radiographie thoracique[31].
Le diagnostic de la sarcoïdose est anatomopathologique ; on doit déceler un granulome épithélioïde et gigantocellulaire sans nécrose caséeuse sur une biopsie de l'organe atteint (biopsie d'adénopathies le plus souvent). La biopsie du granulome qui permet le diagnostic de certitude n'est indiquée que dans les formes modérées à sévères qui nécessiteront un traitement.
Examens complémentaires
En cas de diagnostic de sarcoïdose, différents examens sont pratiqués pour déterminer quels sont les organes touchés par la maladie. Ces examens permettent de détecter les lésions de façon précoce et d’assurer ainsi un suivi médical adapté. On distingue deux grandes familles d’examens : les examens mettant en évidence une atteinte intra-pulmonaire et ceux mettant en évidence une atteinte extra-pulmonaire.
Les atteintes intra-pulmonaires peuvent être suspectées grâce à :
- des épreuves fonctionnelles respiratoires (EFR) permettent d’apprécier la sévérité, le retentissement de l’atteinte pulmonaire et l'évolution. Ce test est indolore et dure une trentaine de minutes. Typiquement, on relève :
- une spirométrie normale ou un syndrome restrictif,
- une analyse des gaz du sang normaux, une désaturation à l'effort, parfois une hypoxémie et une hypocapnie dans les formes sévères,
- un abaissement de la DLCO et de la DLCO rapportée au volume alvéolaire (KCO) ;
- la fibroscopie qui permettra un lavage bronchoalvéolaire et une biopsie des lésions granulomateuses n'est indiquée que dans les formes suffisamment sévères pour justifier un traitement ;
- la tomodensitométrie (ou scanner) est indiquée pour surveiller les formes sévères et diagnostiquer des lésions de fibrose[34]. Cet examen permet d’évaluer plus précisément l’état des poumons et de visualiser des lésions invisibles en radiographie standard.
Les atteintes extra-pulmonaires imposent un traitement urgent et efficace. Afin de les diagnostiquer, on réalise les examens suivants :
- un examen ophtalmologique ;
- des examens cardiaques, notamment la Scintigraphie myocardique au Thallium, l’IRM et l’électrocardiogramme[35] ;
- des explorations neurologiques : dans ces cas, l'apport du scanner et de l'IRM sont primordiaux ;
- un bilan rénal.
Diagnostic différentiel
Le diagnostic différentiel repose[36],[37] sur deux modalités :
- la présentation radioclinique,
- la présence de lésions granulomateuses,
| Avec granulome | Sans granulome | |
|---|---|---|
| Dans tous les cas |
|
|
| Adénopathies médiastinales | primo-infection de Tuberculose (rarement) si adénopathies unilatérales, lymphomes hodgkinien ou non (surtout en cas d'adénopathies antérieures) | métastases des cancers solides au stade clinique (cancer du poumon en général) |
| Atteinte pulmonaire | Pneumopathie d'hypersensibilité (médicamenteuse ou interstitielle idiopathique ; UIP, NSIP, AIP, BOOP, DIP, LIP) | Lymphangite carcinomateuse (surtout secondaire à un cancer médullaire de la thyroïde, histiocytose X, fibrose interstitielle diffuse primitive, amyloïdose pulmonaire diffuse |
| Atteinte extrathoracique | Lèpre, Syphilis, Lymphogranulomatose d'inoculation, granulomatose médicamenteuse, Maladie de Crohn, Cancer bronchopulmonaire, Maladie de Whipple… |
Évolutions
La sarcoïdose est une maladie qui disparaît dans 50 % des cas en moins de trois ans[42]. Le syndrome de Löfgren en particulier, guérit seul dans 90 % des cas. La mortalité associée à la maladie est comprise entre 0,5 % et 5 %[43]. Des complications sont possibles, mais très rares : atteinte cardiaque, méningite, fibrose respiratoire, insuffisance respiratoire chronique. L'apparition d'une hypertension artérielle pulmonaire est péjorative[44]. En dehors des cas sévères, aucun traitement n'est nécessaire (sinon, on propose une corticothérapie).
Traitement
La sarcoïdose peut guérir spontanément dans la majorité des cas. Pour cela, il faut distinguer entre les deux formes de la maladie : asymptomatique et symptomatique. Dans le premier cas, il n’est pas nécessaire de suivre un traitement quelconque. Un suivi clinique et biologique pendant une durée de six mois serait largement suffisant.
Les formes symptomatiques nécessitent un traitement médicamenteux notamment dans les formes de plus mauvais pronostic.
La prise en charge de la sarcoïdose a fait l'objet de plusieurs recommandations publiées par des sociétés savantes nationales ou internationales, dont celles de l'American Thoracic Society, datant de 1999[45], et celles, datant de 2008, de la British Thoracic Society[46].
Corticothérapie
Le traitement le plus utilisé est la corticothérapie (traitement par corticoïdes), que ce soit localement (corticoïdes sous forme inhalée, locale pour les uvéites antérieures ou injectable pour les uvéites postérieures) ou par voie générale.
Les indications formelles à la corticothérapie orale sont les localisations entrainant un risque vital ou fonctionnel majeur (cœur, système nerveux central, œil, muscle, hypercalcémie persistante) ou les localisations cutanées importantes (préjudice esthétique). Dans les formes seulement pulmonaires, seuls les patients symptomatiques présentant des anomalies radiologiques et fonctionnelles significatives doivent être traités d'emblée.
Le traitement corticoïde est prolongé, d'au moins 2 ans, à la dose initiale de 0,5 mg/kg/jour de prednisolone (parfois jusqu'à 1 mg/kg/jour). Les doses seront ensuite très lentement dégressives, avec de possibles rechutes lorsque les doses deviennent inférieures à 0,15 mg par jour et à l'arrêt du traitement. Dans certains traitements, la corticothérapie peut être instaurée avec en même temps le méthotrexate en injection sous-cutanée hebdomadaire ou sous forme de comprimés.
L'efficacité de la corticothérapie est plus grande si le traitement est instauré avant l'apparition de lésions irréversibles.
Alternatives à la corticothérapie
- Les immunosuppresseurs : Thalidomide, Méthotrexate, Azathioprine (Imurel), Ciclosporine A. Le méthotrexate pourrait, en particulier, diminuer les besoins en corticoïdes[47]. La cyclosporine s'avère non efficace dans cette indication[48].
- Les antipaludéens de synthèse, dont la chloroquine[49],[50] (surtout pour les formes exclusivement cutanées). 23 patients ont pris de la chloroquine durant 6 mois pour la moitié d'entre eux et durant 2 ans pour les autres, avec des effets indésirables principalement lors des posologies élevées, mais la molécule semble avoir freiné la dégradation des poumons de ceux qui l'ont utilisé (avec amélioration des symptômes, de la fonction pulmonaire, de l'enzyme de conversion de l'angiotensine et de l'image au scanner pulmonaire, et moins de risque de rechutes ou d'évolution rapide vers une fibrose pulmonaire).
- Les anticorps dirigé contre le TNF (tumor necrotizing factor)[51] : infliximab, etanercept ou adalimumab[52]. Les résultats sont, pour l'instant, mitigés[52],[53],[54].
D'autres molécules ont été testées : le Pentoxifylline pourrait diminuer les besoins en corticoïdes[55].
Les antioxydants n'ont aucun intérêt démontré dans la prise en charge de la sarcoïdose.
Historique
Jonathan Hutchinson (1828-1913) est le premier à avoir décrit la sarcoïdose en 1877[56].
Le dermatologue français Ernest Henri Besnier (1831-1909) décrivit en 1889 une lésion de la peau symétrique des extrémités.
Le dermatologue suédois Cæsar Peter Møller Boeck (1845-1917) mentionna en 1899 les lésions histologiques de la peau[57] et posa déjà alors le soupçon d’une maladie systémique. C’est pourquoi ces lésions sont appelées depuis lors comme étant la sarcoïdose de Boeck.
L’ophtalmologue danois Christian Frederick Heerfordt (1871-1953) décrit une infection fiévreuse de la conjonctive et, à cause des analyses du laboratoire, la classe comme étant due aux oreillons.
En 1924, le dermatologue suédois Jörgen Nilsen Schaumann (1879-1953) confirme la découverte de Boeck : il s’agit d’une maladie systémique de plusieurs organes. Schaumann dénomme la sarcoïdose « lymphogranulomatosis benigna », pour la distinguer du lymphome de Hodgkin.
Le Suédois Sven Halvar Löfgren (1910–1978) décrit en 1953 la forme aiguë, les « Trias », avec érythème noueux, arthrite et adénopathies ganglionnaires bi-hilaires.
Associations d'entraide
La sarcoïdose étant déjà connue depuis plus de cent ans et concernant une partie non négligeable de la population d’âge moyen, des organisations internationales se sont constituées comme pour d’autres maladies, ainsi les personnes concernées ont pu s’organiser et créer des cercles d’entraide. Ceux-ci travaillent souvent ensemble et se sont donné pratiquement les mêmes buts.
Un des buts principaux est l’information sur la sarcoïdose des personnes atteintes et de leur entourage. Il leur est le plus souvent très difficile de trouver des informations destinées au grand public. Vu les symptômes très variés et la nécessité de diagnostics différentiels et des connaissances relativement infimes de beaucoup de médecins en ce qui concerne cette maladie, ils doivent en être informés également d’une façon plus vaste. Un autre but est la sensibilisation du grand public pour les problèmes des malades, qui à cause de leurs symptômes diffus, sont placés dans la catégorie des « simulant ».
Aussi une meilleure qualité des soins et la prise en charge des patients atteints de sarcoïdose sont un des buts principaux des organisations. Souvent sont même demandés une meilleure structure pour les soins et des services ambulatoires spécialisés, ainsi qu’une recherche accrue des causes et des moyens thérapeutiques et de soulagement. La sensibilisation de la sphère politique, ainsi que des responsables de la santé et du social, joue aussi un rôle primordial. Beaucoup d’organisations d’entraide pour la sarcoïdose sont actives pour promouvoir la recherche concernant cette pathologie.
Divers
Robespierre aurait été atteint de cette maladie[58]. Bernie Mac est mort de cette maladie[59].
Notes et références
- (en) E. Neville, A. N. Walker et D. Geraint James, « Prognostic Factors Predicting the Outcome of Sarcoidosis: An Analysis of 818 Patients », QJM: An International Journal of Medicine, vol. 52, no 4, , p. 525–533 (ISSN 1460-2725, DOI 10.1093/oxfordjournals.qjmed.a067778, lire en ligne, consulté le )
- (en) Garima Singh, Sri Krishna jayadev Magani, Rinku Sharma, Basharat Bhat, Ashish Shrivastava, Madhusudhan Chinthakindi et Ashutosh Singh, « Structural, functional and molecular dynamics analysis of cathepsin B gene SNPs associated with tropical calcific pancreatitis, a rare disease of tropics : Table 1: The Single Nucleotide Polymorphisms in cathepsin B protein mined from literature », PeerJ, (PMID 16492714, DOI 10.7717/peerj.7425, lire en ligne, consulté le )
- (en) Benjamin A Rybicki, Marcie Major, John Popovich Jr, Mary J Maliank et Michael C Iannuzzi, « Racial Differences in Sarcoidosis Incidence : A 5-Year Study in a Health Maintenance Organization », American Journal of Epidemiology, vol. 145, no 3, , p. 234-241. (ISSN 1476-6256 et 0002-9262, PMID 9012596, résumé, lire en ligne).
- « La sarcoïdose »(Archive • Wikiwix • Archive.is • Google • Que faire ?) par le professeur B. Wallaert, université de Lille. « Présentation » du Dr I. Ghozlani.
- Trivieri MG, Spagnolo P, Birnie D et al. Challenges in cardiac and pulmonary sarcoidosis, JACC, 2020;76:1878-1901
- Rybicki, B. A., Amend, K. L., Maliarik, M. J., & Iannuzzi, M. C. (2004). Photocopier exposure and risk of sarcoidosis in African-American sibs. Sarcoidosis, vasculitis, and diffuse lung diseases: official journal of WASOG, 21(1), 49-55.
- A. M. Derler, K. Eisendle, M. Baltaci, G. Obermoser et B. Zelger, « High prevalence of'Borrelia-like'organisms in skin biopsies of sarcoidosis patients from Western Austria », Journal of Cutaneous Pathology, vol. 36, no 12, , p. 1262–1268 (PMID 19469874, DOI 10.1111/j.1600-0560.2009.01271.x)
- lire en ligne
- (en) Lee S. Newman, Cecile S. Rose, Eddy A. Bresnitz et al., « A Case Control Etiologic Study of Sarcoidosis : Environmental and Occupational Risk Factors », American Journal of Respiratory and Critical Care Medicine, vol. 170, no 12, , p. 1324-1330 (ISSN 1535-4970 et 1073-449X, PMID 15347561, DOI 10.1164/rccm.200402-249OC, résumé, lire en ligne).
- Perlman SE, FriedmanS, Galea S et al. Short-term and medium-term health effects of 9/11, Lancet, 2011;378:925–934
- Académie nationale de médecine, "« Piercings » et tatouages : la fréquence des complications justifie une réglementation", Bulletin de l'académie nationale de médecine, vol. 191, n° 9, 2007 ([PDF] lire en ligne)
- Ali SM, Gilliam AC, Brodell RT. (2008), Sarcoidosis appearing in a tattoo ; J Cutan Med Surg. jan-fév. 2008 ; 12(1):43-8.
- Antonovich DD, Callen JP (2005), Development of sarcoidosis in cosmetic tattoos ; Arch Dermatol. juillet 2005 ; 141(7):869-72.
- Hassam B, Heid E. (1992), Cutaneous sarcoid reaction in tattoo scars: four cases, two with systemic involvement ; Tunis Med. déc 1992; 70(12):587-9.
- (en) Benjamin A. Rybicki, Michael C. Iannuzzi, Margaret M. Frederick, Bruce W. Thompson, Milton D. Rossman, Eddy A. Bresnitz et al., « Familial Aggregation of Sarcoidosis : A Case-Control Etiologic Study of Sarcoidosis », American Journal of Respiratory and Critical Care Medicine, vol. 164, no 11, , p. 2085-2091 (ISSN 1535-4970 et 1073-449X, PMID 11739139, résumé, lire en ligne).
- (en) A. Sverrild, V. Backer, K. O. Kyvik, J. Kaprio, N Milman, C. B. Svendsen et S. F. Thomsen, « Heredity in sarcoidosis : a registry-based twin study », Thorax, vol. 63, no 10, , p. 894-896 (ISSN 1468-3296, DOI 10.1136/thx.2007.094060, résumé).
- (en) Michael C. Iannuzzi, « Genetics of Sarcoidosis », Seminars in Respiratory and Critical Care Medicine, New York, NY, Thieme Medical Publishers, vol. 28, no 1 « Sarcoidosis: Evolving Concepts and Controversies », , p. 15-21 (DOI 10.1055/s-2007-970330, résumé).
- (en) Ruta Valentonyte, Jochen Hampe et al., « Sarcoidosis is associated with a truncating splice site mutation in BTNL2 », Nature Genetics, vol. 37, no 4, , p. 357-364 (ISSN 1061-4036 et 1546-1718, DOI doi:10.1038/ng1519, résumé).
- Hofmann S, Franke A, Fischer A et al. Genome-wide association study identifies ANXA11 as a new susceptibility locus for sarcoidosis, Nat Genet, 2008;40:1103–1106
- Berlin M, Fogdell-Hahn A, Olerup O, Eklund A, Grunewald J, HLA-DR predicts the prognosis in Scandinavian patients with pulmonary sarcoidosis, Am J Respir Crit Care Med, 1997;156:1601–1605
- (en) Michael C. Iannuzzi et Joseph R. Fontana, « Sarcoidosis : Clinical Presentation, Immunopathogenesis, and Therapeutics », JAMA, vol. 305, no 4, , p. 391-399 (PMID 21266686, DOI 10.1001/jama.2011.10, résumé).
- 1.Li N, Bajoghli A, Kubba A, Bhawan J.Identification of mycobacterial DNA in cutaneous lesions of sarcoidosis. Jour Cutan Pathol. 1999 Jul;26(6):271-8.
- Drake WP, Pei Z, Pride DT, Collins RD, Cover TL, Blaser MJ. Molecular analysis of sarcoidosis tissues for mycobacterium species DNA. Emerg Infect Dis. 2002 Nov;8(11):1334-41. Reply
- (en) Zhimin Song, Lisa Marzilli, Brian M. Greenlee et al., « Mycobacterial catalase–peroxidase is a tissue antigen and target of the adaptive immune response in systemic sarcoidosis », The Journal of Experimental Medicine, vol. 201, no 5, , p. 755-767 (ISSN 1540-9538 et 0022-1007, DOI 10.1084/jem.20040429, résumé, lire en ligne).
- (en) Adriana A. Bonfioli et Fernando Orefice, « Sarcoidosis », Seminars in Ophthalmology, vol. 20, no 3, , p. 177-182 (ISSN 0882-0538 et 1744-5205, DOI 10.1080/08820530500231938, résumé).
- (en) Davendra Mehta, Steven A. Lubitz, Zev Frankel et al., « Cardiac Involvement in Patients with Sarcoidosis : Diagnostic and Prognostic Value of Outpatient Testing », Chest, vol. 133, no 6, , p. 1426-1435 (ISSN 0012-3692 et 1931-3543, DOI 10.1378/chest.07-2784, résumé, lire en ligne).
- (en) Kawano, Sayaka et al., « Sarcoidosis Manifesting as Cardiac Sarcoidosis and Massive Splenomegaly », Intern Med, vol. 51, , p. 65-69 (DOI 10.2169/internalmedicine.51.5247, lire en ligne, consulté le )
- Ekstrom K, Lehtonen J, Nordenswan HK et al. Sudden death in cardiac sarcoidosis: an analysis of nationwide clinical and cause-of-death registries, Eur Heart J, 2019;40:3121-3128
- (en) Elyse E. Lower et Kenneth L. Weiss, « Neurosarcoidosis », Clinics in Chest Medicine, vol. 29, no 3 « Sarcoidosis », , p. 475-492 (ISSN 0272-5231, DOI 10.1016/j.ccm.2008.03.016, résumé).
- (en) Marc A. Judson, Bruce W. Thompson, David L. Rabin et al., « The Diagnostic Pathway to Sarcoidosis », Chest, vol. 123, no 2, , p. 406-412 (ISSN 0012-3692 et 1931-3543, DOI 10.1378/chest.123.2.406, résumé, lire en ligne).
- Lynch 3rd JP, Ma YL, Koss MN, White ES, Pulmonary sarcoidosis, Semin Respir Crit Care Med, 2007;28:53-74
- Navani N, Lawrence DR, Kolvekar S et al. Endobronchial ultrasound-guided transbronchial needle aspiration prevents mediastinoscopies in the diagnosis of isolated mediastinal lymphadenopathy: a prospective trial, Am J Respir Crit Care Med, 2012;186:255–260
- (en) Alvin S. Teirstein, Josef Machac, Orlandino Almeida et al., « Results of 188 Whole-Body Fluorodeoxyglucose Positron Emission Tomography Scans in 137 Patients With Sarcoidosis », Chest, vol. 132, no 6, , p. 1949-1953 (ISSN 0012-3692 et 1931-3543, DOI 10.1378/chest.07-1178, résumé, lire en ligne).
- Criado E, Sanchez M, Ramirez J et al. Pulmonary sarcoidosis: typical and atypical manifestations at high-resolution CT with pathologic correlation, Radiographics, 2010;30:1567–1586
- Schuller JL, Olson MD, Zipse MM et al. Electrocardiographic characteristics in patients with pulmonary sarcoidosis indicating cardiac involvement, J Cardiovasc Electrophysiol, 2011;22:1243–1248
- « Diagnostic différentiel », Sarcoïdose, sur MEDinfos (consulté le ).
- A. Taytard, G. Prévot et A. Didier, « Sarcoïdose », sur la base documentaire Respir, .
- (en) Sandra R.M. Fernandes, Bernhard H. Singsen et Gary S. Hoffman, « Sarcoidosis and systemic vasculitis », Seminars in Arthritis and Rheumatism, vol. 30, no 1, , p. 33-46 (PMID 10966211, DOI 10.1053/sarh.2000.8364, résumé).
- (en) Robert M. Hoffmann, Maria-Christina Jung, Reinhard Motz, Christoph Göβl, Hans-Peter Emslander, Reinhard Zachoval et Gerd R. Pape, « Sarcoidosis associated with interferon-alpha therapy for chronic hepatitis C », Journal of Hepatology, vol. 28, no 6, , p. 1058-1063 (ISSN 0168-8278, résumé).
- Patrice Cacoub, Abdellah Sbaï, Camille Francès, Catherine Génesti, Pierre Hausfater et Jean-Charles Piette, « Sarcoïdose systémique au cours d'un traitement par interféron alpha pour une hépatite chronique virale C », Gastroentérologie clinique et biologique, vol. 24, no 3, , p. 364-366 (PMID 10804348, lire en ligne).
- « Le béryllium, métal discret mais dangereux », Dossier web, sur INRS, .
- « La sarcoïdose : Maladie de Besnier-Boeck-Schaumann », Encyclopédie Orphanet Grand Public, sur Orphanet, .
- « Sarcoïdose », sur Orphanet.
- (en) A. F. Shorr, D. L. Helman, D. B. Davies et S. D. Nathan, « Pulmonary hypertension in advanced sarcoidosis : epidemiology and clinical characteristics », European Respiratory Journal, vol. 25, no 5, , p. 783-788 (ISSN 0903-1936 et 1399-3003, DOI 10.1183/09031936.05.00083404, résumé, lire en ligne).
- (en) « Statement on Sarcoidosis », American Journal of Respiratory and Critical Care Medicine, American Thoracic Society, vol. 160, no 2, , p. 736-755 (ISSN 1535-4970 et 1073-449X, PMID 10430755, lire en ligne).
- (en) B. Bradley, H. M. Branley, J. J. Egan, M. S. Greaves, D. M. Hansell, N. K. Harrison et al., « Interstitial lung disease guideline : the British Thoracic Society in collaboration with the Thoracic Society of Australia and New Zealand and the Irish Thoracic Society », Thorax, vol. 63, no Suppl. 5, , v1-v58 (ISSN 1468-3296, DOI 10.1136/thx.2008.101691, résumé).
- (en) R. P. Baughman, D. B. Winget et E. E. Lower, « Methotrexate is steroid sparing in acute sarcoidosis : results of a double blind, randomized trial », Sarcoidosis, vasculitis, and diffuse lung diseases, vol. 17, no 1, , p. 60-66 (PMID 10746262).
- (en) Christoph P. Wyser, Emmerentia M. van Schalkwyk, Berthold Alheit, Philip G. Bardin et James R. Joubert, « Treatment of Progressive Pulmonary Sarcoidosis with Cyclosporin A : A Randomized Controlled Trial », American Journal of Respiratory and Critical Care Medicine, vol. 156, no 5, , p. 1371-1376 (ISSN 1535-4970 et 1073-449X, PMID 9372647, résumé, lire en ligne).
- (en) D. Davies, « Sarcoidosis treated with chloroquine », British Journal of Diseases of the Chest, vol. 57, no 1, , p. 30–36 (ISSN 0007-0971, DOI 10.1016/S0007-0971(63)80005-4, lire en ligne, consulté le )
- (en) Marcel Baltzan, Sanjay Mehta, Trevor H. Kirkham et Manuel G. Cosio, « Randomized Trial of Prolonged Chloroquine Therapy in Advanced Pulmonary Sarcoidosis », American Journal of Respiratory and Critical Care Medicine, vol. 160, no 1, , p. 192–197 (ISSN 1073-449X et 1535-4970, DOI 10.1164/ajrccm.160.1.9809024, lire en ligne, consulté le )
- (en) R. P. Baughman, E. .E Lower et M. Drent, « Inhibitors of Tumor Necrosis Factor (TNF) in sarcoidosis : Who, What, and How to use them », Sarcoidosis, vasculitis, and diffuse lung diseases, vol. 25, , p. 76-89 (PMID 19382527, lire en ligne).
- Yvan Jamilloux, Fleur Cohen-Aubart, Catherine Chapelon-Abric et Delphine Maucort-Boulch, « Efficacy and safety of tumor necrosis factor antagonists in refractory sarcoidosis: A multicenter study of 132 patients », Seminars in Arthritis and Rheumatism, vol. 47, no 2, , p. 288–294 (ISSN 1532-866X, PMID 28392046, DOI 10.1016/j.semarthrit.2017.03.005, lire en ligne, consulté le )
- (en) James P. Utz, Andrew H. Limper, Sanjay Kalra et al., « Etanercept for the Treatment of Stage II and III Progressive Pulmonary Sarcoidosis », Chest, vol. 124, no 1, , p. 177-185 (ISSN 0012-3692 et 1931-3543, DOI 10.1378/chest.124.1.177, résumé, lire en ligne).
- (en) Robert P. Baughman, Marjolein Drent, Mani Kavuru et al., « Infliximab Therapy in Patients with Chronic Sarcoidosis and Pulmonary Involvement », American Journal of Respiratory and Critical Care Medicine, vol. 174, no 7, , p. 795-802 (ISSN 1535-4970 et 1073-449X, PMID 16840744, DOI 10.1164/rccm.200603-402OC, résumé, lire en ligne).
- (en) M. K. Park, J. R. Fontana Jr, H. Babaali et al., « Steroid-Sparing effects of pentoxifylline in pulmonary sarcoidosis », Sarcoidosis, vasculitis and diffuse lung diseases, vol. 26, no 2, , p. 121-131 (PMCID PMC2946799, résumé, lire en ligne).
- (en) Sir Jonathan Hutchinson, « Anomalous diseases of skin and fingers : case of livid papillary psoriasis? », dans Illustrations of clinical surgery, London, J. & A. Churchill, (OCLC 11026298), p. 42-43.
- (en) C. Boeck, « Multiple benign sarcoid of the skin », J Cutan Genitourin Did, , p. 17543–17550.
- Charlier P, Froesch P, Robespierre: the oldest case of sarcoidosis?, Lancet, 2014;382:2068
- nouvel obs,
Voir aussi
Articles connexes
- Tumeur sarcoïde chez les équidés
Liens externes
- (en) WASOG World Association for Sarcoidosis and Other Granulomatous Disorders
- Europe
- European European Association of Patients Organizations of Sarcoidosis and other Granulomatous Disorders
- (Classé par ordre alphabétique) :
- Allemagne : DSV - Deutsche Sarkoidose Vereinigung
- Belgique : Vereniging voor sarcoïdosepatiënten (néerlandais)
- France : RISMS-Réseau International de Soutien des Malades de la Sarcoïdose
- France : Sarcoidose Infos, Site francophone sur la sarcoïdose
- Grèce : sarcoidosis.gr
- Italie : Site de l'Association italienne
- Norvège : Norsk Sarkoidose Forening
- Pays-Bas : Sarcoidose Belangenvereniging Nederland SBN
- Royaume-Uni : Sarcoidosis and Interstitial Lung Association S.I.L.A., Great-Britain
- Suisse : Schweizerische Sarkoidose-Vereinigung
- Autres pays :
- États-Unis :
- Canada :
- Portail de la médecine