Salive
La salive est un liquide biologique sécrété par les glandes salivaires, à l'intérieur de la bouche chez la plupart des animaux. La salivation est la production de la salive, tandis que l'insalivation est l'imprégnation des aliments par la salive au cours de leur passage dans la bouche et de leur mastication. Certains animaux ont une salive pouvant devenir allergène pour l'humain (après une morsure de tique par exemple).
Pour les articles homonymes, voir Bave.
Chez l'être humain, elle contient aussi de nombreuses cellules provenant de la langue et des muqueuses de la bouche, ce qui la fait utiliser pour l'échantillonnage de l'ADN individuel[1].
De nombreux virus et bactéries pathogènes pour l'homme et divers animaux sauvages ou d'élevage, transportés par des moustiques, des mouches piqueuses ou les tiques utilisent la salive de leur vecteur pour s'introduire dans l'organisme qu'ils vont infecter (virus de la rage par exemple). Mais d'autres virus (arbovirus...) et des bactéries (borrelia) utilisent aussi certaines réponses immunitaires (innées et/ou adaptatives) de l'hôte infecté vis-à-vis de cette salive pour plus facilement infecter leur hôte et parfois - au moins durant un certain temps - échapper au système immunitaire de l'hôte[2].
Chez l'être humain
Fonctions
En lien avec le système nerveux[3], la salive joue un rôle d'humidification et de lubrification des particules alimentaires, préparant ainsi les aliments à leur digestion. Chez l'être humain et d'autres mammifères, elle contribue directement à la digestion de l'amidon (à condition que la nourriture ne soit pas chaude ; l'amylase salivaire étant dégradée au-dessus de 37 °C).
La salive, en mettant en solution les composants des aliments, favorise la stimulation gustative. Ce qui explique que les personnes atteintes du syndrome sec ont une altération du goût. En effet, la salivation est un acte réflexe, mais qui a également une composante culturelle acquise : une "bonne" odeur ou la vue d'un gâteau peut faire saliver. La salivation peut aussi être provoquée par des douleurs, une sensation agréable, voire un souvenir, autant que par le contact mécanique avec les aliments. Elle est au cœur de l'expérience de Pavlov.
Elle facilite le glissement des organes buccaux les uns sur les autres, et notamment lors des 3 000 déglutitions salivaires quotidiennes[4]. Chez l'adulte, ceci correspond à deux déglutitions par minute, de jour comme de nuit.
Le rôle lubrifiant de la salive est non seulement important pour le transit buccal des aliments, mais aussi pour la phonation, en diminuant les frictions inter-muqueuses. La production de sons serait impossible si la bouche restait sèche[5].
Elle a un rôle de défense contre les microbes. Elle permet de prévenir les infections, notamment les caries, en particulier grâce aux mucines qui empêchent les bactéries de se coller aux dents. Elle contient le système sialoperoxydase produisant l'anion antimicrobien hypothiocyanite et a ainsi un rôle de protection de l'œsophage.
La salive a aussi — dans une certaine mesure et contre certains organismes ou virus — des propriétés désinfectantes. On a récemment montré in vitro que par exemple la salive sous-mandibulaire humaine diminue l'infectivité du virus de l'immunodéficience humaine de type 1 (VIH-1). Une fractions protéiques dotée d'une activité anti-VIH a pu être isolée et purifiée dans la salive et a été testée pour sa capacité à inhiber l'infection ; deux glycoprotéines sialiées de poids moléculaire élevé dont été identifiées : l'agglutinine salivaire et la mucine, ainsi que plusieurs protéines de poids moléculaire inférieur encore à décrire. Ces protéines salivaires spécifiques semblent interagir avec le VIH-1 via la Gp120 avec comme résultant une baisse de l'infectivité, notamment en provoquant (rôle probable de la mucine) une agrégation des virus. Cette action n'a été observée que pour le VIH 1 et non pour d'autres adénovirus, ni pour le virus Herpes simplex type 1 (HSV-1), l'HIV-2, ou le virus de l'immunodéficience simienne[6],[7].
Inversement la salive peut être source d'infection et de réinfections du ou de la partenaires lors de relations sexuelles où elle est utilisée comme lubrifiant (pour les gonorrhées notamment[8]. Selon une étude récente (2018) un bain de bouche désinfectant avant un rapport oral diminue considérablement le risque de transmission d'une gonorrhée (maladie sexuellement transmissible en forte augmentation).
La salive peut contribuer à certains empoisonnements, notamment chez l'enfant, qui aurait en bouche un objet en plomb, ou qui lèche de la peinture (« Pica »), elle peut alors fortement aggraver le risque de saturnisme[9]. Dans certaines communautés amérindiennes et inuit où la chasse reste une tradition importante, il est courant que les enfants aient accès à une arme à air comprimé avant de pouvoir utiliser le fusil. Fréquemment entre deux tirs, ils tiennent entre les dents un ou plusieurs projectiles pour pouvoir recharger plus vite l'arme[9]. Une étude a porté sur 144 écoliers des Premières nations de la région ouest de la Baie James dont 152 ont pu participer (95 %). Parmi ces derniers, près de la moitié (41 %) ont déclaré avoir utilisé ou utilisé des fusils à plomb (71 % étaient des garçons et 17 % des filles) ; 52 % de ces élèves ont dit stocker des plombs dans leur bouche entre deux tirs (60 % des garçons et 29 % des filles utilisant ces armes)[9]. L'étude a montré que c'est une source significative et supplémentaire au plomb pour ces enfants déjà surexposés en raison d'une consommation plus élevée que la moyenne de gibier tué par des projectiles au plomb toxique sachant que 40 à 50 % du plomb ingéré est considéré comme absorbé par les enfants, ce qui est bien plus que chez les adultes[10]. Le plomb salivaire augmentait de jusqu'à 8 fois après la mise en bouche de seulement deux plombs/diabolos, passant de 1,5± 1,7µg/L à 12,4±5,7mg/L)[9]. Les pêcheurs peuvent aussi sertir leurs plomb sur le fil de pêche au moyen de leurs dents.
Le baiser dit intime, profond ou passionné est source d'échange de salive et donc d'une partie du microbiome des partenaires[11], avec échanges d'ADN susceptible de perturber certaines analyses médicolégales basées sur l'ADN[12].
Détournement de fonctions
Au cours de l'évolution divers virus et bactéries ont réussi à utiliser ou modifier les caractéristiques de la salive de leurs vecteurs-piqueurs pour se transmettre plus facilement aux animaux et à l'homme[2]. Selon l'OMS, en 2017 les pathogènes utilisant la salive d'un vecteur pour mieux infecter leur hôte sont responsables d'environ 17% de toutes les maladies transmissibles chez l'homme, soit d'un milliard de cas par an, et d'un million de morts directes par an[13].
Dans ces cas les vecteurs semblent être le plus souvent des arthropodes et essentiellement des moustiques, puces et tiques et quelques mouches piqueuses. Le moustique est le principal vecteur pour ce qui concerne les arbovirus qui sont à eux seuls sources d'une morbidité et mortalité très significatives chez l'Homme[2].
Depuis la fin du XXème siècle, nombre des maladies émergents ou ré-émergentes les plus préoccupantes (fièvre du Nil occidental, chikungunya, dengue et Zika pour les virus) et maladie de Lyme ou leishmaniose par exemple pour les bactéries) se sont répandus sur la planète, parfois de manière pandémique en devant source d'urgences répétées en matière de santé publique. En 2018, on manque encore de médicaments et/ou vaccins homologués ou efficaces contre la plupart de ces virus[2]. La production de nouveaux vaccins est compliquée par le nombre de virus et de souches virale contre lequel la protection est recherchée[2].
Une piste proposée par Jessica E. Manning et ses collègues en 2018 pour les arboviroses est de créer des vaccins non pas uniquement contre les protéines des virus ou bactéries, mais aussi contre certaines protéines propres à la salive du vecteur (moustiques par exemple), plutôt que contre seulement les protéines virales. Lors de premiers essais, l'immunisation par des antigènes salivaires de phlébotomes pour prévenir l'infection par des leishmania a donné de bons résultats en laboratoire avec le modèle animal[2]. J. Manning pense que des vaccins ciblant la salive d'Aedes aegypti pourrait protéger contre de multiples infections virales transmises par ce moustique[2].
Formation
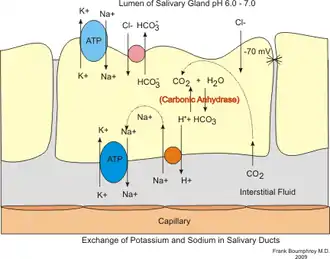
La salive primaire est formée dans les cellules acineuses, elle a la même composition que le plasma. Elle est ensuite modifiée dans le canal excréteur pour former la salive secondaire. Au cours du passage dans ce canal, les cellules canalaires sécrètent activement du K+ et du HCO3- et absorbent activement du Na+ et du Cl-. Son efficacité dépend des glandes salivaires, mais aussi du pancréas[14]
Volume
Seule une moitié du litre (environ) de salive produite par jour est sécrétée lors des repas.[réf. nécessaire]
D'une personne à l'autre, la sécrétion peut varier de 500 à 1 200 ml par jour : 70 % d'origine parotidienne, 20 % submandibulaire (la production des autres glandes étant relativement négligeable). La sécrétion de repos serait d'environ 100 ml par jour alors que la sécrétion stimulée serait environ dix fois supérieure. Le débit de sécrétion montre des variations nycthémérales (minimum à 3 h, maximum entre 12 h et 22 h). Un organisme humain peut produire plus de 36 000 litres de salive en une vie, soit plus d'une demi-tonne de ce liquide par an. À côté de la phonation et des repas, la déglutition salivaire est, de loin, le travail le plus important fourni par la bouche. En moyenne, il y a deux déglutitions par minute (de jour comme de nuit).
Viscosité
La viscosité varie selon l’origine :
- 1,5 centipoises pour les parotides
- 3,4 centipoises pour les submandibulaires
- 13,4 centipoises pour les sublinguales.
pH
Le pH varie selon l’origine.[réf. nécessaire]
Globalement, la salive humaine a un pH approximatif compris entre 6,5 – 7,4.
N.B. Une stimulation de la sécrétion fait augmenter le pH.
Composition biochimique
Compte tenu de sa riche composition en électrolytes[15] et protéines, la salive pourrait un jour remplacer les prises de sang pour un certain nombre de paramètres.
Une première étape clé dans cette voie a été franchie avec le décryptage complet du protéome salivaire. 1166 protéines ont en effet été identifiées dans la salive[16].
Les tests salivaires sont déjà employés pour la recherche de stupéfiants, de l'ADN ou du cortisol par exemple utilisé comme biomarqueur de stress[17],[18],[19].
La majorité des protéines présentes dans la salive sont impliquées dans les voies de signalisation activées par le corps en cas d’infection ou de lésion organique.
Des études précédentes[20][réf. incomplète] ont déjà prouvé qu’elles constituaient un bon indicateur pour diagnostiquer les cancers buccaux ainsi que l’infection par le virus du SIDA, par la recherche des anticorps ciblés sur le virus[21] (ce qui ne signifie pas que la salive soit contaminante pour le VIH ; elle ne l'est qu'en présence de plaie dans la bouche [22]). Cette liste sera probablement bientôt élargie pour inclure des principales causes de décès comme le cancer et les maladies du cœur. Si cette hypothèse se confirme, les médecins disposeront ainsi d’un nouvel outil de diagnostic plus aisé à mettre en œuvre et également moins coûteux, mieux adapté, par exemple, à des campagnes de dépistage à grande échelle ou à la pratique de la médecine humanitaire.
Eau
Le pourcentage de volume[réf. nécessaire] d'eau dans la salive est de 99 %. Solution hypotonique (qui est moins concentrée en ions) comparativement au plasma sanguin, elle peut devenir isotonique ou même hypertonique dans certaines conditions. En dissolvant des aliments, la salive permet de détecter leur goût.
Composés inorganiques
La salive n'est pas un simple ultrafiltrat du plasma ;
| Ion | Non-stimulée (mEq/l) | Stimulée (mEq/l) | Plasma (mEq/l) |
|---|---|---|---|
| Na+ | 2,7 | 54,8 | 143,3 |
| K+ | 48,3 | 28,7 | 5,1 |
| Cl- | 31,5 | 35,9 | 100,9 |
| HCO3- | 0,6 | 29,7 | 27,5 |
N.B. Noter la grande différence entre les concentrations en ion sodium et ion hydrogénocarbonate selon la condition de prélèvement.
Composés organiques
- Urée : environ 2 mM (soit 2 mmol/L), selon le taux sanguin et l'ingestion de protéines (catabolisme des acides aminés) ;
- Glucose : environ 0,056 mM (NB : 3,6 à 6,1 mM dans le plasma) ;
- Acide urique, acide citrique, acides aminés, créatinine, cholestérol et phospholipides sont présents en faible concentrations.
- Hormones : le dosage de la progestérone salivaire (en faible concentration) peut servir d'indicateur de la phase du cycle menstruel
- Molécules d'ARN : la salive contient plus de 3 000 types d'ARN messagers dont le dosage pourrait être un marqueur prometteur de cancer de la bouche[23].
Protéines
- Amylase
- Lipase linguale
- Lysozyme (muramidase)
- Kallicréine
- Protéines-riches-en-proline (PRP)
- Cystatine
- Stathérine
- Gustine
- Histatine
- Anhydrase carbonique
- Lactoferrine
- Immunoglobulines
- Peroxydases
- Protéases déshydrogénases
- Phosphatases
- Albumine
- Mucines
Pathologies
- Asialie
- Hyposialie
- Hypersialorrhée
- De nombreuses bactéries provenant du microbiote buccal et/ou de la nourriture ou encore des boissons sont retrouvés dans la salive, dont certaines peuvent être pathogènes.
Récemment une « nouvelle forme de vie » y a été découverte par hasard lors d’un screening de l’ADN et d’ARN (analyse métagénomique de la microflore buccale) : il s'agit d'une minuscule bactérie parasite d'Actinomyces odontolyticus (une bactérie normalement présente dans le sol, mais aussi fréquemment trouvée dans la bouche, et qui peut être pathogène, cause de gingivites, de fibrose kystique et liée à des mécanismes de résistance aux antimicrobiens[24]). Dotée d’un patrimoine génétique très réduit (environ 700 gènes, à comparer aux 2 200 gènes d’A. odontolyticus), elle semble entièrement dépendante de son hôte Actinomyces[24]. Bien plus petite que la plupart des autres bactéries, elle peut vivre à la surface de ses bactéries-hôtes ; de telles caractéristiques n’avaient jamais été trouvées chez une bactérie. Il semble que dans un premier temps, les hôtes (Actinomyces) tolèrent ces parasites qui s’attachent eux-mêmes à sa membrane en y prélevant des nutriments, puis le parasite attaque et tue l’hôte en transperçant sa membrane[24]. C’est pourquoi cette espèce été difficilement isolée et récemment découverte (elle ne peut être cultivée en boite de Petri indépendamment de son hôte Actinomyces ; ceci laisse d'ailleurs penser que, pour la même raison, de nombreuses autres bactéries parasites pourraient exister sans avoir été découvertes, car de nombreux indices (génétiques notamment) plaident pour des interactions durables entre microbes, parasitaires notamment[24].
Pathogénicité : ce micro-parasite pourrait être lié à certaines pathologies, car des taux plus élevés de son ADN ont été retrouvés chez des patients victimes de maladies des gencives ou de fibrose kystique. Les Actinomyces sont connues pour être potentiellement pathogènes pour les gencives, mais sont normalement contrôlées par les globules blancs (macrophagie) ; or il semble que les bactéries infectées par ce parasite puissent échapper aux macrophages, ce qui leur permettraient de se développer impunément dans les gencives[24].
Antibiorésistance : des chercheurs (de l’Université de Washington) ont trouvé une autre espèce de bactérie parasite infectant des archées (les archées sont des microorganismes qui ont longtemps été confondus avec les bactéries, mais qui en sont en réalité biologiquement et génétiquement distincts, sans véritable noyau cellulaire et dépourvus de structures intracellulaires complexes)[24]. Curieusement, ces deux bactéries parasites présentent une propriété commune : elles rendent leurs hôtes résistants à la streptomycine, point qui pourrait éclairer les phénomènes croissants d’antibiorésistance [24]. Un traitement antibiotique par la streptomycine favorise donc indirectement la bactérie hôte, connue pour être pathogène pour l’Homme.
Pour les patients ne produisant pas assez de salive ou privés de glandes salivaires (à la suite d'un cancer par exemple), on cherche à créer une salive artificielle[25],[26].
Chez l'animal non-humain

Des animaux utilisent leur salive pour des usages autres qu'alimentaires ; ainsi :
- de nombreux mammifères se lèchent le pelage ;
- le martinet construit son nid par une lente accumulation de salive qui forme une paroi en séchant ;
- les araignées et de nombreux acariens injectent de la salive dont les enzymes vont lyser de la chair ou des cellules végétales, qui pourra ensuite être réabsorbée par le rostre piqueur ;
- des moustiques piqueurs femelles ont une salive qui les aide à trouver les endroits où piquer pour leur repas sanguin[27] ;
- Les larves de phryganes, aquatiques, se construisent un fourreau protecteur en agglomérant avec de la salive des matériaux pris dans l'environnement (cailloux notamment).
Notes et références
- Goode, M. R., Cheong, S. Y., Li, N., Ray, W. C., & Bartlett, C. W. (2014). Collecte et d'extraction de l'ADN de la salive pour le séquençage de prochaine génération.
- Manning J.E, Morens D.M, Kamhawi S, Valenzuela J.G & Memoli M (2000) Mosquito saliva : the hope for a universal arbovirus vaccine?. The Journal of infectious diseases, 218(1), 7-15.
- Garrett, J. R. (1987). The proper role of nerves in salivary secretion: a review. Journal of dental research, 66(2), 387-397.
- (en) Afkari S, « Measuring frequency of spontaneous swallowing » Australas Phys Eng Sci Med. 2007;30:313-7.
- Jean Azerad, Physiologie de la manducation, Masson, , p. 70
- Malamud D, Davis C, Berthold P, Roth E, Friedman HM (1993) Human submandibular saliva aggregates HIV, AIDS Res Hum Retroviruses, vol. 9 (pg. 633-7)
- Nagashunmugam T, Friedman HM, Davis C, Kennedy S, Goldstein L, Malamud D (1997). Human submandibular saliva specifically inhibits HIV type 1, AIDS Res Hum Retroviruses, vol. 13 (pg. 371-6)
- Fairley, C. K., Zhang, L., & Chow, E. P. (2018). New thinking on gonorrhoea control in MSM: are antiseptic mouthwashes the answer ?. Current opinion in infectious diseases, 31(1), 45-49 (résumé).
- Tsuji L, Fletcher G & Nieboer E (2002) Dissolution of Lead Pellets in Saliva: A Source of Lead Exposure in Children |Bulletin of Environmental Contamination and Toxicology|68, 1, 1| URL : https://www.researchgate.net/profile/Evert_Nieboer/publication/7370461_Elevated_Levels_of_PCBs_in_First_Nation_Communities_of_the_Western_James_Bay_Region_of_Northern_Ontario_Canada_The_Use_of_Correspondence_Analysis_to_Identify_Source_of_Exposure/links/577a759f08aece6c20fbd13b.pdf
- Ziegler EE, Edwards BB, Jensen JL, Mahaffey KR, Fomon SJ (1978) Absorption and retention of lead by infants | Pediatric Res 12: 29-34
- Kort, R., Caspers, M., van de Graaf, A., van Egmond, W., Keijser, B., & Roeselers, G. (2014). Shaping the oral microbiota through intimate kissing. Microbiome, 2(1), 41.
- Banaschak, S., Möller, K., & Pfeiffer, H. (1998). Potential DNA mixtures introduced through kissing. International journal of legal medicine, 111(5), 284-285.
- World Health Organization (2017). A global brief on vector-borne diseases. Téléchargeable ici : http://www.who.int/campaigns/world-health-day/2014/global-brief/en/
- Gayda T (2015) Influence de la ligature du conduit pancréatique sur le pouvoir amylolytique de la salive et du sang. Archives Italiennes de Biologie, 90(30), 165-170 |résumé.
- Schneyer, L. H., Young, J. A., & Schneyer, C. A. (1972). Salivary secretion of electrolytes. Physiological reviews, 52(3), 720-777 |résumé
- (en) UCLA Human Salivary proteome project
- Hellhammer D.H, Wüst S & Kudielka B.M (2009) Salivary cortisol as a biomarker in stress research. Psychoneuroendocrinology, 34(2), 163-171.
- Kirschbaum, C., & Hellhammer, D. H. (1994). Salivary cortisol in psychoneuroendocrine research: recent developments and applications. Psychoneuroendocrinology, 19(4), 313-333.
- Kirschbaum, C., & Hellhammer, D. H. (1989). Salivary cortisol in psychobiological research: an overview. Neuropsychobiology, 22(3), 150-169.|résumé
- Journal of Proteome Research
- Bigot, A., Zohoun, I., Kodjoh, N., Ahouignan, G., Zohoun, T., Tonato, S., & Burtonboy, G. (1994). Détection des anticorps anti-VIH dans la salive: étude préliminaire. Médecine d'Afrique noire, 41(1), 11-14.
- Rotily, M., Prudhomme, J., Pardal, M. D. S., Hariga, F., Iandolo, E., Papadourakis, A., & Moatti, J. P. (2001). Connaissances et attitudes du personnel de surveillance pénitentiaire face au VIH et/ou sida: une enquête européenne. Santé publique, 13(4), 325-338
- Wong D. « Les diagnostics salivaires » Pour la Science, décembre 2008, p. 54-59
- Andy Coghlan (2016) New life form discovered in saliva is linked to human disease Article publié par New Scientist ; dans “Daily news” le 23 juin 2016
- Kang, M., Park, H., Jun, J. H., Son, M., & Kang, M. J. (2017). Facilitated saliva secretion and reduced oral inflammation by a novel artificial saliva system in the treatment of salivary hypofunction. Drug design, development and therapy, 11, 185.
- Apperley, O., Medlicott, N., Rich, A., Hanning, S., & Huckabee, M. L. (2017). A clinical trial of a novel emulsion for potential use as a saliva substitute in patients with radiation induced xerostomia. Journal of oral rehabilitation|résumé
- Ribeiro, J. M., Rossignol, P. A., & Spielman, A. (1984). Role of mosquito saliva in blood vessel location. Journal of Experimental Biology, 108(1), 1-7.
Voir aussi
Bibliographie
- Carolina, A. (2017). Food-saliva interactions: Mechanisms and implications. Trends in food science & technology |résumé.
- Ho, A., Affoo, R., Rogus-Pulia, N., Nicosia, M., Inamoto, Y., Saitoh, E., ... & Fels, S. (2017). Inferring the effects of saliva on liquid bolus flow using computer simulation. Computers in biology and medicine, 89, 304-313|résumé
- Kupirovič, U. P., Elmadfa, I., Juillerat, M. A., & Raspor, P. (2017). Effect of saliva on physical food properties in fat texture perception. Critical reviews in food science and nutrition, 57(6), 1061-1077.
- Ngamchuea, K., Chaisiwamongkhol, K., Batchelor-McAuley, C., & Compton, R. G. (2018). Chemical analysis in saliva and the search for salivary biomarkers–a tutorial review. Analyst.
- Portail de la physiologie