Physeteroidea
Physétéroïdes • Cachalots

| Règne | Animalia |
|---|---|
| Embranchement | Chordata |
| Sous-embr. | Vertebrata |
| Classe | Mammalia |
| Infra-classe | Placentalia |
| Ordre | Cetartiodactyla |
| Infra-ordre | Cetacea |
| Micro-ordre | Odontoceti |
Les physétéroïdes (Physeteroidea) sont une super-famille de cétacés odontocètes communément appelés cachalots. Ils ne comptent plus que trois espèces vivantes : le grand cachalot, dans le genre Physeter, le cachalot pygmée et le cachalot nain dans le genre Kogia. Ces genres sont souvent réunis dans une même famille, celle des physétéridés, avec le genre Kogia placé dans une sous-famille (Kogiinae), mais plus récemment on place ce genre dans sa propre famille, celle des Kogiidés, laissant la famille des Physétéridés comme monotypique, c'est-à-dire ne comptant qu'une seule espèce vivante, bien que d'autres représentants, fossiles, des deux familles soient connus.
Terminologie
Le terme « cachalot » est d'origine ibérique. On retrouve dans les textes français l'occurrence de cachalut dès 1628, où l'appellation était employée à Saint-Jean-de-Luz pour décrire l'animal considéré comme « le m[â]le de la baleine ». Le terme actuel, trouvé à l'écrit en 1694, est emprunté au portugais cachalote ou cacholote au XVIIe siècle, désignant le même animal, mais dont l'origine n'est pas claire. Il semble provenir du portugais cachola, signifiant « grosse tête »[1]. Le terme est aussi donné comme provenant du gascon cachau ou de caichal relevé à Carcassonne; au sens de « grandes dents »[2],[3]. Dans son dictionnaire étymologique Joan Coromines propose que les termes ibériques soient issus du latin populaire cappula, pluriel de cappulum, le manche de l'épée[4].
Désignant originellement le grand cachalot (Physeter macrocephalus), le terme affublé d'une dénomination spécifique s'est étendu à d'autres odontocètes proches, du genre Kogia.
Kyklos signifie Cycle en grec ancien. Le Cachalot mâle effectue de grandes migrations cycliques. Les femelles et les jeunes mâles restent dans les eaux chaudes en été, mais les mâles adultes migrent vers les eaux polaires pour se nourrir de vastes quantités de calmars, rejoignant les femelles en hiver pour se reproduire.
Caractéristiques
|
|
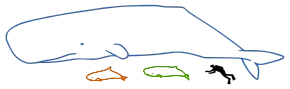
Le grand cachalot, ou cachalot macrocéphale, est la plus grande espèce de cétacés à dents[5], les mâles mesurant entre 15 et 18 mètres de long et pesant environ 45 à 70 tonnes. Les deux espèces de kogiidés sont beaucoup plus petites, mesurant seulement de 2,5 à 3,5 mètres de long et ayant une masse comprise entre 350 et 500 kg.
Le corps des cachalots est massif, robuste, avec des nageoires en forme de rame. La mâchoire inférieure est toujours relativement petite et mince par rapport à la mâchoire supérieure. Les os nasaux des cachalots sont nettement asymétriques, avec l'évent situé sur le côté gauche de la tête, près du sommet de la tête pour le grand cachalot, plus en avant pour les koggidés. Toutes les espèces ont un grand nombre de dents semblables et relativement simple. Chez les kogiidés, et parfois aussi chez le cachalot macrocéphale, les dents de la mâchoire supérieure ne percent pas dans la bouche, et sont parfois totalement absentes[6].
Les yeux des cachalots ne peuvent pas pivoter dans leurs orbites, et la chambre antérieure est vestigiale. Il est probable que l'écholocation soit un sens plus important que la vision pour ces animaux[6].
Une autre caractéristique commune est le spermaceti, une substance semi-liquide blanche et cireuse remplissant une grande partie de la tête du cétacé, et qui joue le rôle d'un ballast lors de la plongée et de maintien de la flottabilité, selon que l'eau froide entrant par le nez durcit la substance pour plonger ou que l'afflux de sang chaud fasse fondre le spermaceti, aidant ainsi la remontée à la surface. Les trois espèces plongent à grandes profondeurs pour trouver de la nourriture (ils peuvent effectuer entre quinze et vingt plongées profondes en vingt-quatre heures, jusqu'à 1 100 m de profondeur pour rejoindre la zone de calmars dont la ration quotidienne atteint plusieurs centaines d'individus), le grand cachalot battant tous les records, pouvant atteindre 2 500 m (il résiste à la pression grâce à une cage thoracique très flexible et un rete mirabile qui compense par un afflux de sang incompressible, la diminution de volume des alvéoles pulmonaires) et des apnées d'une heure. Les membres des deux familles consomment calmars, poissons et même requins[7].
La gestation dure de neuf à quinze mois selon les espèces. L'unique petit reste avec sa mère pendant au moins deux ans, avant d'être sevré. Les cachalots ne parviennent pas à leur pleine maturité sexuelle pendant plusieurs années. Toutes les espèces se rassemblent en groupes appelés « pods », composé pour la plupart de femelles et de leurs petits avec les adolescents, mais la taille de ces pods sont généralement plus faibles chez les kogiidés[6].
Les cachalots dorment en chandelle[7].
Leur communication sonore, comme le chant des baleines, est constituée de clics d'écholocation. Le coda (nombre de clics et variations des intervalles entre clics) caractérise chaque clan[7].
Les cachalots s'organisent selon de structures sociales élevées : groupes matriarcaux (généralement constitués d'une douzaine de femelles avec quelques jeunes, accompagnées d'autres femelles qui peuvent jouer le rôle de nourrices), groupe de célibataires (jeunes mâles immatures), groupe de solitaires (mâles prêts à se reproduire) et groupes de reproducteurs ou harems (les mâles régnant en maîtres sur les femelles)[8].
Des poissons nettoyeurs s'activent autour des cachalots en surface, se nourrissant de leur peau en lambeaux (desquamation régulière) et de leurs excréments[7].
Histoire évolutive

Les premiers fossiles de cachalots connus datent de la fin de l'Oligocène, c'est-à-dire il y a environ 25 millions d'années[9],[10], avec un parent remontant à l'Eocène le plus tardif ayant divergé du reste de la ligne des Odontoceti ayant conduit aux dauphins et marsouins.
Les fossiles connus laissent à penser que les cachalots étaient plus fréquents au Miocène, l'époque des lignées de base (tels que Zygophyseter et Naganocetus). D'autres genres fossiles sont attribués aux Physeteridae comme Ferecetotherium, Helvicetus, Idiorophus, Diaphorocetus, Aulophyseter, Orycterocetus, Scaldicetus et Placoziphius, tandis que les koggidés fossiles sont représentés par les genres Kogiopsis, Scaphokogia et Praekogia[10]. Les premiers kogiidés connus datent de la fin du Miocène, il y a de cela environ 7 millions d'années[10].
La relation étroite entre les Physeteridae et Kogiidae existants est confirmée par les études moléculaires récentes (de 2006) utilisant le cytochrome b des mitochondries[11],[12] ; sur la base de ces analyses, leurs parents les plus proches semblent être les Ziphiidés (baleines à bec) d'une part, les mysticètes (baleines à fanons) et les Platanistidae (dauphins d'eau douce) de l'autre. Cette même étude favorise également le regroupement des Physeteridae et des Kogiidae dans une super-famille unique, des Physeteroidea, comme cela a parfois été suggéré précédemment. Bianucci & Landini, 2006 suggèrent que Diaphorocetus, Zygophyseter, Naganocetus et Aulophyseter datent d'avant la scission des Kogiidés et Physétéridés et choisissent donc de limiter la famille des Physeteridae aux genres qui sont postérieurs à cette division (vue cladistique)[13]. En 2008 un groupe de paléontologues ont découvert un crâne presque complet d'un cachalot préhistorique . Deux ans plus tard il le décrit sous le nom de Livyatan melvillei, le plus grand cétacé carnivore surpassant le Physeter macrocephalus actuel.
L'étude génomique des cachalot a récemment révélé que l'espèce, avant qu'elle ne soit traquée par les baleiniers avait déjà été décimée par quelque chose. Sa population mondiale actuelle (environ 360 000 individus) semble intégralement descendre d'un noyau d'environ 10 000 individus qui a progressivement recolonisé la planète il y aurait environ 100 000 ans[14]. L'espèce n'est pas limitée dans ses déplacements dans l'océan mondial et les individus peuvent théoriquement se reproduire avec beaucoup d'autres, or leur diversité génétique actuelle se montre très faible, sans que la chasse à la baleine puisse à elle seule expliquer cette homogénéité génétique montre l'étude de 175 échantillons de génomes mitochondriaux (ADN hérité uniquement de la lignée maternelle) issus de cadavres échoués (vivants ou morts, provenant de tout le globe). La cause pourrait avoir été une période froide qui les a exclu de tous les océans, sauf le Pacifique. On ignore encore quelles seront les conséquences du dérèglemnet climatique en cours sur cette espèce et sur les autres cétacés[14].
Classification
| Position phylogénétique des cachalots parmi les cétacés | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Les Physeteroidea appartiennent au sous-ordre des odontocètes, contenant toutes les baleines à dents, dauphins y compris. Une espèce vivante est placée dans le genre Physeter, de la famille des Physeteridae. Deux espèces actuelles proches, du genre Kogia, à savoir le cachalot nain (Kogia sima) et le cachalot pygmée (Kogia breviceps), sont parfois aussi placées dans cette famille, ou bien dans leur propre famille, Kogiidae[15].
|
Résumé simplifié de la classification des taxons existants et disparus (†) :
|
Phylogénie des Physeteroidea : o Physeteroidea ├?─ † Ferecetotherium kelloggi ├?─ † Helvicetus rugosus ├?─ † Ontocetus oxymycterus ├?─ † Brygmophyseter shigensis ├──o † Hoplocetinae │ ├──o † Scaldicetus │ ├──o † Idiorophus │ ├──o † Diaphorocetus poucheti │ └──o † Hoplocetus └──o ├──o │ ├──o † Zygophyseter varolai │ └──o † Brygmophyseter shigensis └──o ├──o † Aulophyseterinae │ └──o † Aulophyseter └──o ├──o Kogiinae │ ├?─o † Miokogia elongatus │ ├?─o † Kogiopsis floridana │ ├──o † Praekogia cedrosensis │ ├──o † Scaphokogia cochlearis │ └──o Kogia └──o Physeterinae ├──o † Placoziphius duboisii ├──o † Orycterocetus └──o ├──o † Idiophyseter merriami └──o ├──o † Physeterula dubusii └──o Physeter |
Le cachalot et l'Homme
La relation étroite entre le cachalot et l'Homme est principalement basée autour de sa chasse. Bien que l'on recense plusieurs prises au cours du XVIIe siècle, celles-ci sont principalement dues à la chasse traditionnelle pratiquée par les populations autochtones de Marseille. Il faudra attendre le début du XVIIIe siècle, pour assister à une véritable traque à l'échelle industrielle par les premiers baleiniers américains et canadiens. La chasse au cachalot a principalement été justifiée par la récolte du précieux spermaceti, substance blanche et cireuse issue de la tête de l'animal.
Services écosystémiques
Le cachalot joue un rôle important de superprédateur et il remonte des profondeurs des oligoéléments (iode, fer…) qu'il libère dans l'eau en déféquant ; une étude faite par l'Université Flinders[18] (Australie) a montré en 2010 que le cachalot joue notamment un rôle important dans le cycle du fer. Il l'absorbe avec sa nourriture, et en rejette dans l'eau via ses excréments. or le fer - s'il est biodisponible ce qui est le cas ici - est un stimulant de la productivité phytoplanctonique, qui est elle même le moteur de la pompe à carbone océanique[18]. Les 12 000 cachalots d'Antarctique contribuent ainsi à permettre l'absorption d'environ 400 000 t de carbone (environ deux fois ce que les cachalots émettent en respirant). Leurs excréments dispersent annuellement environ 50 t/an (de fer) dans l'océan, ce serait au moins dix fois plus, s'ils n'avaient pas été pourchassés depuis deux siècles[18]. Sans la pêche baleinière, on estime qu'il y aurait aujourd'hui environ 120 000 (90 % plus qu'en réalité) cachalots rien que dans l'océan Antarctique[18]. Ceci a été confirmé par d'autres études[19],[20],[21].
Comme celui des grandes baleines, son cadavre, une fois coulé sur le plancher océanique devient pour des décennies un « sasis » de vie pour de nombreuses autres espèces. Néanmoins à cause de sa position en tête de pyramide alimentaire, et parce qu'il est gras, il fait partie des espèces susceptibles d'être les plus contaminées par de nombreux polluants qu'il a bioaccumulé tout au long de sa vie.
Annexes
Références taxinomiques
- (en) Référence Tree of Life Web Project : Physeteroidea
- (en) Référence Paleobiology Database : Physeteroidea Gray 1868
Lien externe
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Physeteroidea » (voir la liste des auteurs).
- « Cachalot : Etymologie », sur cntrl.fr (consulté le )
- (es) M. Fernández-Casado, « El Cachalote (Physester macrocephalus) », Galemys, vol. 12, no 2, (lire en ligne [PDF])
- (en) Paul Haupt, « Jonah's whale », Proceedings, American Philosophical Society, Philadelphie, American Philosophical Society, vol. 46, , p. 151–164 (ISBN 9781422373453, lire en ligne)
- (es) Joan Coromines, Breve diccionario etimológico de la lengua castellana, Madrid, Gredos, , 628 p. (ISBN 84-249-1332-9)
- Les orques et dauphins sont des cétacés à dents, les vraies baleines des cétacés à fanons.
- (en) Christina Lockyer, The Encyclopedia of Mammals, New York, D. Macdonald, Facts on File, , 895 p. (ISBN 0-87196-871-1), p. 204–209
- François Sarano, Le retour de Moby Dick. Ou ce que les cachalots nous enseignent sur les océans et les hommes, Éditions Actes Sud, , 230 p. (lire en ligne).
- François Gohier, Marines : le monde des baleines et des dauphins, Éditions Artemis, , 11 p. (lire en ligne).
- (en) R.E. Stucky et M.C. McKenna, « Mammalia », cité dans M.J. Benton, The Fossil Record 2, Londres, Chapman & Hall, , p. 739–771
- (en) Guram Andreevich Mchedlidze, « Sperm Whales, Evolution », cité dans (en) William F. Perrin, Bernd Wursig et J.G.M. Thewissen, Encyclopedia of Marine Mammals, Burlington, Academic Press, , 2e éd. (ISBN 978-0-12-373553-9, lire en ligne), p. 1097-1098
- (en) S.K. Verma, R.K. Sinha et L. Singh, « Phylogenetic position of Platanista gangetica: insights from the mitochondrial cytochrome b and nuclear interphotoreceptor retinoid-binding protein gene sequences », Molecular Phylogenetics and Evolution, vol. 33, , p. 280–288
- (en) L. May-Collado et I. Agnarsson, « Cytochrome b and Bayesian inference of whale phylogeny », Molecular Phylogenetics and Evolution, vol. 38, , p. 344–354
- (en) Giovanni Bianucci et W. Landini, « Killer sperm whale: a new basal physeteroid (Mammalia, Cetacea) from the Late Miocene of Italy », Zoological Journal of the Linnean Society, vol. 148, no 1, , p. 103–131 (DOI 10.1111/j.1096-3642.2006.00228.x)
- Morell V (2018) Something killed a lot of sperm whales in the past—and it wasn’t whalers ; Science news, 18 mai 2018
- (en) James G. Mead et Robert L. Brownell Jr., « Order Cetacea », cité dans Don E. Wilson et DeeAnn M. Reeder, Mammal Species of the World: A Taxonomic and Geographic Reference, Baltimore, Johns Hopkins University Press, , 2142 p. (ISBN 978-0-8018-8221-0, lire en ligne), p. 723-743
- (en) Oliver Lambert, Giovanni Bianucci et Christian de Muizon, « A new stem-sperm whale (Cetacea, Odontoceti, Physeteroidea) from the Latest Miocene of Peru », Comptes Rendus Palevol, vol. 7, no 6, , p. 361–369 (DOI 10.1016/j.crpv.2008.06.002)
- (en) Oliver Lambert, Giovanni Bianucci, K. Post, Christian de Muizon, R. Salas-Gismondi, M Urbina et J. Reumer, « The giant bite of a new raptorial sperm whale from the Miocene epoch of Peru », Nature, vol. 466, , p. 105–108 (DOI 10.1038/nature09067)
- Trish J. Lavery, Ben Roudnew, Peter Gill, Justin Seymour1, Laurent Seuront, Genevieve Johnson, James G. Mitchell et Victor Smetacek (2010) ; Iron defecation by sperm whales stimulates carbon export in the Southern Ocean ; Journal de recherche biologique de la Royal Society : Proceedings of the Royal Society, Biological Sciences ; en ligne (ISSN 1471-2954) ([résumé])
- Ratnarajah, L., Bowie, A. R., Lannuzel, D., Meiners, K. M., & Nicol, S. (2014). The biogeochemical role of baleen whales and krill in Southern Ocean nutrient cycling. PloS one, 9(12), e114067.
- Lavery, T., Roudnew, B., Gill, P., Seymour, J., Seuront, L., Johnson, G., ... & Smetacek, V. (2010). Iron defecation by sperm whales stimulates carbon export in the Southern Ocean. Proceedings of the Royal Society of London. (résumé)
- Lavery, T. J., Roudnew, B., Seymour, J., Mitchell, J. G., Smetacek, V., & Nicol, S. (2014). Whales sustain fisheries: blue whales stimulate primary production in the Southern Ocean. Marine Mammal Science, 30(3), 888-904. (résumé)
- Portail des cétacés
- Portail des mammifères