Lignine
La lignine (du latin lignum qui signifie bois) est une biomolécule, en fait une famille de macromolécules polymères polyphénoliques (famille des tannins lato sensu), qui est un des principaux composants du bois avec la cellulose et l'hémicellulose. La lignine est présente principalement dans les plantes vasculaires et dans quelques algues[1]. Ses principales fonctions sont d'apporter de la rigidité, une imperméabilité à l'eau et une grande résistance à la décomposition. Toutes les plantes vasculaires, ligneuses et herbacées, fabriquent de la lignine.
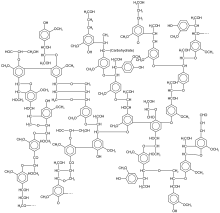
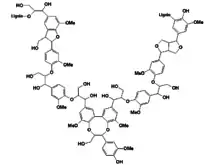
Quantitativement, la teneur en lignine est de 3 à 5 % dans les feuilles, 17 à 24 % dans les tiges herbacées, 18 à 33 % dans les tiges ligneuses (18 à 25 % du bois dur des arbres angiospermes, 27 à 33 % du bois tendre des arbres gymnospermes)[2],[3]. Elle est moindre pour les plantes annuelles que pour les vivaces, elle est maximum chez les arbres. La lignine est principalement localisée entre les cellules (voir paroi pectocellulosique), mais on en trouve une quantité significative à l'intérieur même de celles-ci. Bien que la lignine soit un réseau tridimensionnel hydrophobe complexe, l'unité de base se résume essentiellement à une unité de phénylpropane.
Après la cellulose (constituant 35 à 50 % de la biomasse végétale terrestre) et l'hémicellulose (30 à 45 %), la lignine (15 à 25 %) forme la troisième famille de composés par ordre d’abondance dans les plantes et dans les écosystèmes terrestres où domine la biomasse végétale morte ou vive[4]. L'abondance de ce biopolymère explique qu'il fasse l'objet de recherches en vue de valorisations autres que ses utilisations actuelles en bois d'œuvre et en combustible.
Voie de biosynthèse
La lignine est une biomolécule, un tanin du groupe des phénylpropanoïdes, qui dérivent d'un précurseur, la phénylalanine, après élimination de la partie contenant de l'azote[5]. Cet acide aminé subit une cascade de réactions faisant intervenir une dizaine de familles d'enzymes différentes afin de former des monolignols. Ces enzymes sont : phénylalanine ammonia-lyase (PAL) responsable de la désamination oxydative, cinnamate 4-hydroxylase (C4H), 4-coumarate-CoA ligase (4CL), hydroxycinnamoyl-CoA shikimate/quinate hydroxycinnamoyl transférase (HCT), p-coumarate 3-hydroxylase (C3H), cafféoyl-CoA o-méthyltransférase (CCoAOMT), cinnamoyl-CoA réductase (CCR), ferrulate 5-hydroxylase (F5H), Acide cafféique O-méthyltransférase (COMT) et cinnamyl alcool deshydrogénase (CAD). Dans un certain nombre de cas, des aldéhydes peuvent également être incorporés dans le polymère[6].
Apparition
La lignine est apparue il y a 380 millions d'années, au Dévonien, avec les premières plantes vasculaires que sont les Fougères (Ptéridophytes) et presque simultanément les premiers arbres (Archaeopteris)[7]. La biosynthèse de la lignine nécessite de l'oxygène et est probablement apparue à cette époque lorsque la concentration en oxygène atmosphérique a atteint un niveau suffisant[8].
Historique
En 1813, le botaniste suisse Augustin Pyramus de Candolle décrit brièvement la lignine en page 417 de son ouvrage Théorie élémentaire de la botanique; ou, Exposition des principes de la classification naturelle et de l'art de décrire et d'étudier les végétaux. Il en énumère plusieurs caractéristiques : « fibreuse, insipide, insoluble dans l'eau et l'alcool ; soluble dans les lessives alcalines faibles ; précipitée par les acides[9]. »
En 1839, le chimiste français Anselme Payen parle d'une « matière incrustante » ayant un lien exclusivement mécanique avec la cellulose[10].
C'est en 1856 que le terme lignine fait son apparition pour la première fois en littérature scientifique dans une publication du chimiste Franz Ferdinand Schulze (1815–1873)[11].
Le caractère aromatique de la lignine a été mis en évidence pour la première fois en 1868[12], et en 1897 le scientifique suédois P. Klasen décrira la lignine comme non cellulosique et confirmera sa nature aromatique. Après la Première Guerre mondiale, plusieurs travaux permettront d'attester le phénol comme étant un constituant de la lignine[13],[14], mais il faudra attendre jusqu'en 1927 avant que sa structure phénylpropane et ses dérivés soient clairement établis[15].
Structure chimique
On ne s'accorde toujours pas sur une définition unique et précise de la lignine du fait de sa grande variabilité et cela au sein même d'une espèce donnée, car sa formation dépend de l'environnement physico-chimique dans lequel le végétal croît. Il serait donc préférable de parler des lignines.
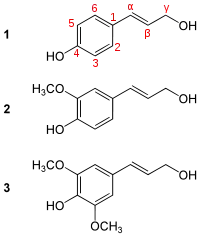
1 : alcool paracoumarylique.
2 : alcool coniférylique.
3 : alcool sinapylique.
Les lignines sont des polymères de monolignols. Il en existe au moins trois :
- l'alcool coumarylique, appelé unité H (hydroxyphényle), sans groupe méthoxy ;
- l'alcool coniférylique, appelé unité G (guaïacyle), à un groupe méthoxy ;
- l'alcool sinapylique, appelé unité S (syringyle), à deux groupes méthoxy.
La fraction de chaque monomère varie de façon importante en fonction de :
- la lignée végétale (gymnosperme, angiosperme monocotylédone, angiosperme dicotylédone) ;
- l’espèce ;
- l’organe ;
- le tissu.
Les gymnospermes contiennent presque exclusivement l'unité G.
Les angiospermes dicotylédones contiennent presque exclusivement les deux unités G et S.
Les angiospermes monocotylédones contiennent les trois unités G, S et H.
Ainsi, toutes les plantes vasculaires, ligneuses et herbacées, fabriquent des lignines où est toujours présente l'unité G (alcool coniférylique), dont l'oxydation donne l'acide férulique.
Les lignines de gymnospermes sont homogènes. Le bois de ces essences, dit homoxylé, est constitué à 95 % de trachéides et à 5 % de différents types de parenchymes. Le bois de résineux contient beaucoup de lignine (entre 25 et 35 %), une lignine dont la structure est « condensée » (nombreuses liaison carbone-carbone entre les unités constitutives).
Les angiospermes, évolutivement beaucoup plus jeunes, ont diversifié leurs tissus pour le transport des sèves par des éléments de vaisseaux en plus des trachéides (alors que chez les gymnospermes, les fonctions de transport des sèves et de support mécanique sont assurées exclusivement par les trachéides). On trouve ainsi une diversité énorme des bois de feuillus, dits hétéroxylés, dont certains sont plus poreux (riches en vaisseaux, comme les chênes) et les autres plus « fibreux » (comme les bouleaux). La lignine devient elle aussi plus diversifiée et elle varie entre les cellules des fibres et les cellules des vaisseaux.
Propriétés et lignification
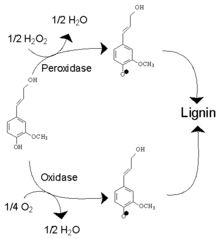
La lignification est un processus fondamental de l’évolution des plantes terrestres végétaux ligneuses. Elle assure une rigidité, une imperméabilité à l'eau, une résistance à l'implosion[16] des cellules conductrices de sève brute[17] et une grande résistance à la décomposition. Cette capacité a permis d'avoir un port dressé favorisant la réception de l'énergie lumineuse. L'ensemble de ces acquisitions étant un préalable à la conquête du milieu terrestre. La capacité de formation de lignine par les végétaux s'est mise en place au début du Paléozoïque (avec un fort développement à partir du Dévonien) et caractérise les trachéophytes (voir flore de Rhynie).
La lignine se dépose tout d'abord dans la lamelle moyenne, la paroi primaire et la couche S1 de la paroi secondaire de certaines cellules végétales, puis imprègne les couches S2 et S3. La paroi aura ainsi une meilleure solidité, car la lignine est très résistante à la compression. De plus, la lignine possède un pouvoir d’imperméabilisation des cellules, du fait de son hydrophobicité.
On trouve ainsi des parois imprégnées de lignine (lignifiées) dans les cellules de tissus servant au soutien de la plante (sclérenchyme) ou au transport de l’eau et des sels minéraux (xylème). En règle générale, les cellules lignifiées, devenues imperméables, ont perdu leur cytoplasme et n’acquièrent leur rôle dans le végétal qu’une fois mortes.
Intérêt biologique

La lignine, qui est donc caractéristique des plantes vasculaires terrestres, offre également une barrière de protection contre l'attaque microbienne du végétal. En effet, Sa nature chimique la rend extrêmement résistante à divers agents chimiques et à la dégradation biologique, ce qui explique la qualité biologique médiocre des fourrages hautement lignifiés.
Selon une hypothèse de A.C Neish et C. Hébant, la lignine serait une forme de stockage des excréments de la plante[18]. Sachant que la lignine est constituée de composés phénoliques qui sont toxiques pour la plante sous forme libre, cette dernière aurait trouvé une façon de les neutraliser en les stockant sous forme de lignine dans des cellules vasculaires mortes.
Dégradation biologique de la lignine
Certains micro-organismes, en particulier les champignons dits de la pourriture blanche du bois, sont capables de digérer entièrement le complexe lignine - hémicellulose - cellulose (ligninolyse) et ainsi d'améliorer la valeur nutritive des matériaux lignocellulosiques.
Voie de dégradation : la lignolyse fongique
Macromolécule très stable, la lignine n'est décomposée de manière significative que par des champignons saprotrophes à haut pouvoir de lyse fongique, principalement des basidiomycètes (agents de « pourriture blanche » de la litière, agents de pourriture du bois qui ont un équipement enzymatique spécifique : cellulases et hémicellulases, peroxydases et polyphénol-oxydases extracellulaires et intracellulaires attaquant les fragments de cellulose, hémicellulose et lignine importés dans la cellule fongique) responsables de la lyse de ces composés et de l'humification[19].

L'activité lignolytique est appelée lignolyse fongique (dégradation de la matière ligneuse du bois de manière significative sans nécessairement s'attaquer à la lignine, les champignons lignolytiques se répartissant en espèces cellulolytiques et en espèces ligninolytiques) et l'activité ligninolytique, ligninolyse fongique (dégradation de la lignine de manière significative)[22],[23].
L'apparition de champignons lignivores (dits aussi xylophages) il y a 280 millions d'années, aurait stoppé l'accumulation des débris végétaux qui avait permis jusqu'alors la formation du charbon par fossilisation pendant la période géologique appelée Carbonifère[24],[25].
Enjeux économiques
- La lignine présente une structure chimique lui permettant d'être intégrée à de nombreuses applications actuellement pétro-sourcées. Le potentiel de marché de la lignine est estimé à plus de 240 milliards de dollars[26].
- Les lignines, pour leur pouvoir calorifique important, sont recherchées dans les bois de chauffage.
- Au contraire, elles gênent la fabrication du papier blanc ; elles sont notamment responsables du jaunissement du papier après exposition au soleil. Ce sont les produits chlorés et organochlorés servant à l'extraction de la lignine des pâtes à papier (délignification) qui rendent polluants les effluents de l'industrie papetière.
- Peu digestes, les lignines sont peu recherchées dans la culture de plantes fourragères, mais néanmoins utilisées comme liant dans l'alimentation animale industrielle[27].
- La lignine, qui a des propriétés tensioactives, est aussi utilisée comme stabilisateur ou émulsifiant de ciments[28], dans des bétons de lignine-bois avec un liant de laitier alcalin (dès les années 1980 en Russie[29]).
Recherche/Prospective
Des recherches sont en cours pour trouver de nouveaux usages à la lignine (par exemple, le bois liquide produit à partir de lignine désoufrée[27]) ; l'industrie tente, essentiellement par transformation génétique, de créer des végétaux pauvres en lignine pour les papeteries, ou au contraire plus riches en lignine, comme bois de chauffage.
La production du complexe lignine-hémicellulose-cellulose est importante sur la planète, et environ 25 % de cette ressource renouvelable serait accessible à des procédés de conversion biotechnologiques. Les champignons xylophages, dont le champignon de la pourriture blanche, sont très étudiés pour leur intérêt dans les domaines suivants :
- amélioration et humification des sols (en utilisation directe via le bois raméal fragmenté) ;
- procédés propres et économiques de traitement de la lignine de l'industrie papetière ;
- bioconversion et production de molécules à haute valeur ajoutée (bois liquide, et polymères) ou produits d'intérêts agro-alimentaire et pharmaceutique à partir de matériaux lignocellulosiques ;
- biotraitement et valorisation des matériaux lignocellulosiques (notamment pour l'alimentation ou le paillage du bétail).
L'université de Tokushima (Japon) a réussi en 2009 à séparer, à haute température et haute pression, la lignine des autres composants du bois, permettant de produire avec cette lignine à faible masse moléculaire l'équivalent d'une résine époxy résistante à la température et non conductrice de l'électricité, comparable selon ses inventeurs aux résines actuellement utilisées[30]. Des résines à bases de lignine sont déjà utilisées comme agent de charge et liant pour agglomérer les particules des panneaux de bois[28], renforcer des caoutchoucs[28] ou la charge adhésive dans les colles à froid à base d'aminoplaste[28] et de phénoplastes[28].
Notes et références
- Martone, Pt; Estevez, Jm; Lu, F; Ruel, K; Denny, Mw; Somerville, C; Ralph, J (Jan 2009). "Discovery of Lignin in Seaweed Reveals Convergent Evolution of Cell-Wall Architecture". Current biology : CB. doi:10.1016/j.cub.2008.12.031.
- C. Lapierre, Séance de l'Académie d'Agriculture, 17 février 2010
- (en) Judith Becker, Christoph Wittmann, « A field of dreams: Lignin valorization into chemicals, materials, fuels, and health-care products », Biotechnology Advances, vol. 37, no 6, (DOI 10.1016/j.biotechadv.2019.02.016).
- (en) Commission of the European Communities, Biomass for energy, UK Section of the International Solar Energy Society, , p. 73.
- Marc-André Selosse, Les Goûts et les couleurs du monde. Une histoire naturelle des tanins, de l'écologie à la santé, actes sud, p. 87.
- (en) J. Ralph et al., « Lignins: Natural polymers from oxidative coupling of 4-hydroxyphenylpropanoids », Phytochem. Rev., vol. 3, no 1, , p. 29–60.
- B. Meyer-Berthaud, S. E. Scheckler, J. Wendt, Archaeopteris is the earliest known modern tree, Nature, 446, 904-907,1999
- (en) J. A. Raven, J. D. Lawson, « Comparative physiology of plant and arthropod land adaptation », Philos. Trans. R. Soc. Lond. B, vol. 309, no 1138, (DOI 10.1098/rstb.1985.0087).
- Augustin Pyramus de Candolle, Théorie élémentaire de la botanique ; ou, Exposition des principes de la classification naturelle et de l'art de décrire et d'étudier les végétaux, Paris, Déterville, (lire en ligne).
- Comptes rendus de l’Académie des Sciences (C.r.), 8 (1939) 51.
- Hägglund, E.; Chemistry of Wood. [Academic press Inc., New York, 1952].
- Bente F., Über die Konstitution des Tannen- und Pappelholzes. Chem. Ber., 8 (1868) 476–479.
- Klason, P.; Ber. dt. chem. Ges. (B.), 53(1920) 1864.
- Fuchs, W.; Berichte der Deutschen Chemischen Gesellschaft (B.), 54 (1921) 484.
- Freudenberg, K.; Zur Konstitution des Lignins. II. Mittl., B., 60 (1927) 581.
- Cette implosion (collapse) est l'effondrement sous l'effet d'une pression négative (tension), surtout en cas de sécheresse et de forte évaporation.
- Marie-Christine Trouy, Anatomie du bois. Formation, fonctions et identification, Éditions Quae, , p. 13.
- Les arbres ont-ils des excréments ?, Interview de Francis Hallé, Le Monde, (consulté le 22 février 2021).
- (en) Martínez AT, Speranza M, Ruiz-Dueñas FJ, Ferreira P, Camarero S, Guillén F, et al., « Biodegradation of lignocellulosics: microbial, chemical, and enzymatic aspects of the fungal attack of lignin », Int Microbiol J Span Soc Microbiol., vol. 8, no 3, , p. 195–204 (DOI 10.1093/femsre/fux049).
- Appelées aussi pourritures blanches de l'humus, elles se distinguent de la pourriture blanche du bois et de la pourriture brune sous l'action desquelles le bois acquiert une texture cubique puis se transforme progressivement en une masse pulvérulente brune.
- Guy Durrieu, Écologie des champignons, Masson, , p. 45.
- Jean-Michel Gobat, Michel Aragno, Willy Matthey, Le sol vivant : bases de pédologie, biologie des sols, PPUR Presses polytechniques, (lire en ligne), p. 304-305.
- (en) Pierre-Emmanuel Courty, Marc Buee, Abdala Gamby Diedhiou, Pascale Frey-Klett, Francois Le Tacon, Francois Rineau, Marie-Pierre Turpault, Stephane Uroz, Jean Garbaye, « The role of ectomycorrhizal communities in forest ecosystem processes: New perspectives and emerging concepts », Soil Biology & Biochemistry, vol. 42, no 5, , p. 679-698.
- (en) D. Floudas et al., « The Paleozoic origin of enzymatic lignin decomposition reconstructed from 31 fungal genomes », Science, vol. 336, no 6089, , p. 1715-1719 (DOI 10.1126/science.1221748).
- David Garon, Jean-Christophe Guéguen, Biodiversité et évolution du monde végétal, EDP Sciences, , p. 166.
- Finding Untapped Value: Converting Lignin to Higher Value Chemicals -Lux Research (juin 2014)
- Le « bois liquide », nouveau composant pour l'industrie du jouet, L'Usine nouvelle, 20/01/2009.
- « Valorisation des déchets de papeteries », mis en ligne par l'ENSEEIHT, consulté le .
- Khrulev V. M. ; Tinnikov A. A. ; Selivanov V. M. ; Étude des propriétés du béton de lignine-bois (article écrit en russe) ; « Izvestiâ vysših ucebnyh zavedenij ». Stroitel'stvo i arhitektura, 1984, no 3, p. 53-57 (2 ref.) ; (ISSN 0536-1052) ; Résumé Inist/CNRS.
- BE Japon numéro 514 (18/09/2009) - Ambassade de France au Japon / ADIT, intitulé Hitachi développe une nouvelle résine époxyde à base de lignine.
Voir aussi
Articles connexes
Liens externes
- Portail de la chimie
- Portail de la botanique