Jean-Pierre Changeux
Jean-Pierre Changeux, né le à Domont, est un neurobiologiste français, connu pour ses recherches dans plusieurs domaines de la biologie, de la structure et de la fonction des protéines (en particulier les protéines allostériques), au développement précoce du système nerveux jusqu’aux fonctions cognitives. Bien que célèbre dans les sciences biologiques pour le modèle Monod-Wyman-Changeux, il est aussi reconnu pour l’identification et la purification du récepteur nicotinique de l’acétylcholine et la théorie de l’épigenèse par stabilisation sélective des synapses. Changeux est connu du public non scientifique pour des idées concernant la relation entre l’esprit et le cerveau. Comme il l’écrit dans son livre Matière à pensée, Changeux défend la conception selon laquelle le système nerveux est actif plutôt que réactif et que l’interaction avec l’environnement, au lieu d’être instructive, résulte de la sélection de représentations internes préexistantes. Il est membre de l'Académie des sciences depuis 1986.
Pour les articles homonymes, voir Changeux.
Biographie
Jean-Pierre Changeux entre en 1955 à l’École normale supérieure. Il obtient sa licence en 1957 et son diplôme d’études supérieures en 1958. Il est reçu à l’agrégation de sciences naturelles la même année. Il commence sa carrière scientifique alors qu'il se trouve encore à l’École normale supérieure, lors de stages d’été au laboratoire Arago de Banyuls-sur-Mer, où il identifie une nouvelle espèce de parasite. Il rédige sa thèse à l’Institut Pasteur sous la direction de Jacques Monod et de François Jacob, et obtient son doctorat en 1964. Changeux quitte ensuite la France pour des études post-doctorales d’abord à l’Université de Californie (Berkeley) (1965-1966), puis à l’Université Columbia College of Physicians and Surgeons, New York (1967). Il rentre en France comme sous-directeur de la chaire de biologie moléculaire occupée par Jacques Monod au Collège de France et, en 1972, il est nommé directeur de l’Unité de neurobiologie moléculaire à l’Institut Pasteur, où il devient professeur en 1975. La même année, Changeux est élu professeur au Collège de France, chaire de « communications cellulaires », qu’il occupe jusqu’en 2006.
Il est auteur de plus de 600 articles scientifiques et de plusieurs livres spécialisés ou destinés à un plus large public.
Travaux scientifiques
Pendant toute sa carrière scientifique, Changeux a été fidèle à une conception moniste du cerveau de l’Homme alliant niveaux moléculaire, cellulaire et cognitif. Si l’on souhaite trouver un thème unificateur, c’est la conviction que la sélection est à la base de processus vitaux plutôt que l’instruction. Alors que ses lignes de recherche ont débuté comme des approches séparées, elles se sont trouvées réunies au cours des décennies récentes, autour des mécanismes allostériques comme fondement du rôle des récepteurs de neurotransmetteurs dans les fonctions cognitives.
Dans les années 1980, Francis Crick affirme que la conscience peut être étudiée scientifiquement. D'autres neurologues, dont Jean-Pierre Changeux de l'Institut Pasteur lui emboîtent le pas. Une controverse entre les dualistes et les matérialistes voit le jour en parallèle au développement des neurosciences[1].
Allostérie

Pendant son travail de thèse, effectué sous la direction de Jacques Monod et de François Jacob, Changeux étudie les propriétés allostériques d’enzymes régulatrices bactériennes, dont l’activité est modulée par des signaux chimiques de structure différente de celle de leurs substrats[2],[3],[4]. Son travail conduit au développement du modèle de transition concertée pour les protéines allostériques dit de Monod-Wyman-Changeux[5],[6]. L’idée principale de cette théorie est que : 1) ces protéines peuvent exister sous plusieurs conformations en équilibre thermique et en l’absence de signal régulateur : les effecteurs modifiant l’équilibre entre conformations en stabilisant celle pour laquelle ils montrent l’affinité la plus élevée, 2) toutes les sous-unités d’une protéine multimérique existent dans la même conformation, la transition ayant lieu de manière concertée. Le modèle explique la coopérativité concertée des protéines régulatrices sans changement progressif des paramètres biophysiques. Ce cadre conceptuel est encore utilisé pour expliquer les propriétés coopératives de protéines régulatrices comme l’hémoglobine.
Dans sa thèse de doctorat, Changeux suggère que la reconnaissance et la transmission de signaux par la membrane, en particulier par les membranes synaptiques, pourraient utiliser le même mécanisme que la régulation allostérique des enzymes bactériens. Pendant plus de quarante ans de recherche, Changeux a focalisé sa recherche sur les récepteurs de l’acétylcholine. En 1967, Changeux étend le modèle Monod, Wyman, Changeux à des réseaux bi-dimensionnels de récepteurs[7] (une idée qui sera développée trente ans plus tard par Dennis Bray[8]). Il applique également le modèle aux récepteurs présents dans la membrane post-synaptique de l’organe électrique[9],[10]. Son équipe démontre l’existence de plusieurs états interconvertibles du récepteur nicotinique - de repos, ouvert et désensibilisé - qui présentent des affinités différentes pour les ligands comme l’acétylcholine[11],[12],[13]. Les transitions entre ces états suivent des cinétiques différentes et ces cinétiques ainsi que différentes affinités suffisent pour expliquer la forme du potentiel post-synaptique. Un modèle mécaniste plus complet du récepteur nicotinique du muscle strié (ou de l’organe électrique) est publié plus tard en collaboration avec Stuart Edelstein, un autre spécialiste de l’allostérie, qui a travaillé pendant plusieurs décennies sur l’hémoglobine[14].
Structure du récepteur nicotinique
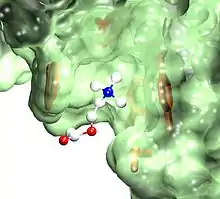
En 1970, Changeux isole le récepteur nicotinique de l’acétylcholine à partir de l’organe électrique d'un gymnote, le premier récepteur pharmacologique membranaire jamais isolé[16] et cela grâce aux propriétés d’une toxine de venin de serpent[17]. L’isolement du même récepteur à partir de l’organe électrique de torpille était rapporté quelques mois plus tard par Ricardo Miledi[18]. L’amélioration des méthodes de purification développées dans le groupe[19] lui permet de proposer que le récepteur est une protéine pentamérique[20], un résultat confirmé par la suite par l’équipe d’ Arthur Karlin[21]. Le groupe de Changeux a été parmi les premiers à élucider la structure primaire des sous-unités du récepteur[22],[23], en parallèle avec le groupe de Shosaku Numa[24] et de Stephen Heinemann[25].
Au cours des années 1980 et 1990, les méthodes de biologie moléculaire qu’il a développées dans son laboratoire lui ont permis de déchiffrer les structures tertiaire et quaternaire de ce récepteur. Il a localisé le canal ionique au niveau du second segment transmembranaire[26], un résultat confirmé plus tard par les groupes de Shosaku Numa[27] et de Ferdinand Hucho[28]. Les déterminants moléculaires de la sélectivité ionique étaient aussi identifiés dans le même segment transmembranaire[29],[30],[31]. La structure du site de liaison de l’acétylcholine et de la nicotine était identifiée comme une niche aromatique située à l’interface entre sous-unités adjacentes dans le domaine extracellulaire[32],[33],[34].
Les recherches de Changeux sur la structure du récepteur nicotinique ont culminé récemment avec la publication de la structure au niveau atomique d’un homologue bactérien du récepteur nicotinique dans la conformation ouverte[35], supportant l’idée d’une ouverture concertée et symétrique du canal ionique.
Stabilisation sélective des synapses par l’activité neuronale
En 1973, avec Philippe Courrège et Antoine Danchin, Changeux propose un modèle décrivant comment au cours du développement du système nerveux, l’activité du réseau entraine la stabilisation ou l’élimination des synapses qu’il contient[36] et l’illustre avec des expériences sur la jonction neuromusculaire. Ce modèle est précurseur de la thèse biologisante[37] du « Darwinisme neuronal » qui a été défendu par la suite par Gerald Edelman. Changeux poursuit et illustre cette idée[38]. Pendant les années 1980, il essaie de le documenter soit avec des souris mutantes[39],[40], soit avec des expériences de dénervation[41],[42].
Fonction du récepteur nicotinique
Au cours des années 1990, le groupe de Changeux s’intéresse à la structure du récepteur nicotinique de l’organe électrique du gymnote ou de la torpille et étend ses investigations au rôle physiologique de ce récepteur soit à la jonction neuromusculaire, la synapse reliant les neurones moteurs au muscle squelettique, soit dans le cerveau, notamment en relation avec la dépendance à la nicotine.
Dès les années 1980, le groupe étudie la compartimentalisation d’expression du récepteur dans les cellules musculaires en développement, en relation avec son travail théorique sur l’épigénèse. En particulier, le groupe s’intéresse à l’accumulation du récepteur nicotinique dans la région post-synaptique au cours du développement, concomitante d’un changement d’identité du récepteur. Ils démontrent que l’accumulation résulte : 1. de l’inhibition de la transcription des gènes du récepteur en dehors de la région synaptique par l’activité électrique qui simule l’entrée de calcium et l’activation de PKC[43],[44],[45],[46], et 2. une stimulation de la transcription au niveau de la synapse par le CGRP activant la PKA[47],[48],[49] ou par l’ARIA (héréguline) activant des cascades de tyrosines kinases[50],[51]. Les éléments promoteurs et facteurs de transcription concernés sont identifiés.
Au cours des années 1990, Changeux évolue progressivement de la jonction neuromusculaire aux récepteurs nicotiniques exprimés dans le cerveau. Parmi les résultats obtenus par le groupe, on peut noter la découverte que les récepteurs neuronaux sont perméables au calcium[52] – ce qui explique l'effet positif des récepteurs nicotiniques sur la libération de nombreux neurotransmetteurs dans le cerveau[53] – mais aussi que le calcium est un effecteur allostérique modulateur de ces récepteurs[54] (ce qui fut également découvert indépendamment par le groupe de John Dani[55]). Le groupe identifie par la suite les sites de liaison allostérique du calcium[56],[15].
Au milieu des années 1990, Changeux a concentré la plupart de ses intérêts sur la fonction du récepteur nicotinique dans les systèmes dopaminergiques mésencéphaliques en utilisant des souris invalidées sélectivement pour différents gènes du récepteur nicotinique. Le groupe a caractérisé les types de sous-unités du récepteur présents dans les neurones dopaminergiques[57],[58],[59] et identifié les récepteurs responsables de la dépendance à la nicotine, qui engagent les sous-unités α4, α6 et β2[60],[61]. Entre 1995 et 1998, son laboratoire a été en partie financé par le Council for Tobacco Research de l'industrie du tabac[62], contribuant en particulier à l'élucidation des rôles de la sous-unité β2 dans la mise en place de la dépendance à la nicotine[60].
Modélisation de la cognition
Depuis les années 1990, Changeux a poursuivi son activité de modélisation computationnelle en s’intéressant aux bases neuronales des fonctions cognitives. Cette recherche a été effectuée principalement en collaboration avec Stanislas Dehaene qui dirige maintenant une unité Inserm-CEA de neuroimagerie cognitive. Ils ont modélisé, par exemple, l’acquisition de la reconnaissance des chants d’oiseaux[63] ou le développement des capacités numériques chez l’Homme[64]. Plus récemment, Dehaene et Changeux ont développé un modèle d’accès à la conscience basé sur le recrutement au niveau cérébral global de réseaux de neurones avec des axones à longue distance: l’espace de travail neuronal conscient[65],[66].
Activités non scientifiques
Jean-Pierre Changeux a été président du Comité consultatif national d'éthique en France, de 1992 à 1998.
Il est passionné par l’art et a organisé plusieurs expositions : De Nicolo Dell’Abate à Nicolas Poussin : aux sources du classicisme (Meaux), La lumière au Siècle des Lumières (Nancy), Passions de l’âme (Meaux) et a coorganisé (avec Jean Clair) l’Âme au corps (Paris Grand Palais).
Il est membre du conseil scientifique de l’Agence Internationale des Musées, France Muséums, depuis 2007.
Jean-Pierre Changeux a été président, de 1989 à 2012, de la Commission interministérielle d'agrément pour la conservation du patrimoine artistique national, dite Commission des dations, qui examine l'acceptation des œuvres d'art proposées à l'État français en paiement de droits de succession. Il a lui-même donné des œuvres d'art à l'État dans ce cadre[67].
Il fut membre du conseil d'administration du Centre Royaumont pour une Science de l’Homme.
Prix et honneurs

Prix scientifiques
- 1977 : prix Alexandre Joannidès de l'Académie des sciences
- 1978 : prix Gairdner
- 1982 : Prix Wolf de médecine
- 1982 : prix Richard-Lounsbery de l'Académie des sciences
- 1983 : prix littéraire Broquette-Gonin de l'Académie française pour l'Homme neuronal
- 1985 : prix Céline
- 1985 : Ciba Geigy Drew Award in Biomedical Research
- 1986 : prix Francis O. Schmitt du Neurosciences Research Institute
- 1988 : prix Rita-Levi-Montalcini de la fondation Fidia
- 1990 : prix Bristol-Myers-Squibb du Neurosciences Research Institute
- 1991 : médaille Carl-Gustav-Bernhard de l'Académie des sciences suédoise
- 1992 : Science for Art, prix d'honneur LVMH
- 1992 : International Prize Amedeo e Frances Herlitzka for Physiological Sciences
- 1992 : médaille d'or du CNRS[68]
- 1993 : prix Louis-Jeantet de médecine
- 1993 : Thudichum medal, Biochemical Society
- 1994 : Goodman and Gilman Award in drug receptor pharmacology
- 1994 : Camillo Golgi medal, Accademia Nazionale dei Lincei
- 1994 : sir Hans Krebs medal, FEBS
- 1996 : médaille Max-Delbrück en Molecular Medicine
- 1997 : grand Prix de la Fondation pour la recherche médicale, Paris
- 1997 : prix Jean-Louis Signoret, en neuropsychologie, Fondation Ipsen
- 1998 : prix Emanuel Merck en Chimie, Darmstadt
- 1999 : medaille Linus Pauling, Stanford, USA
- 1999 : prix Eli Lilly, en Neuroscience préclinique, Collège européen de Neuropsychopharmacologie, Londres
- 2000 : Langley Award for basic research on nicotine and tobacco, Washington
- 2001 : prix Balzan pour les neurosciences cognitives
- 2002 : American Philosophical Society’s Karl Spencer Lashley Award in neuroscience
- 2005 : Lewis Thomas Prize for Writing about Science Rockefeller University, New-York
- 2006 : Dart/NYU Biotechnology Award in Basic Biotechnology, New-York
- 2006 : award of the Biotechnology Study Center de la New York University School of Medicine, avec Eric R. Kandel (Prix Nobel de physiologie ou médecine en 2000), et Charles Weissmann
- 2006 : Golden Eurydice Award from International Forum of Biophilosophy, Bruxelles
- 2005 : Rockefeller University's science writing prize
- 2007 : National Academy of Sciences Award in the Neurosciences
- 2008 : Prix de la plasticité neuronale, Fondation Ipsen
- 2008 : CINP Pioneer Award
- 2012 : Japanese Society for the Promotion of Science (JSPS) award for eminent scientists
- 2016 : International research award from the Olav Thon Foundation (Oslo)[69]
- 2018 : Prix mondial des sciences Albert-Einstein
Académies et diplômes honorifiques
- Deutsche Akademie der Naturforscher Leopoldina zu Halle (pharmacologie), 1974
- Académie de médecine de Turin, 1976
- National Academy of Sciences, Washington (États-Unis) (foreign associate), 1983
- Académie royale des sciences de Suède, Stockholm, (Suède) (membre étranger), 1985
- Académie des sciences, Paris, 1988
- Académie royale de médecine de Belgique (Bruxelles) (membre étranger honoraire), 1988
- Academia Europaea (membre fondateur), 1988
- American Academy of Arts and Sciences, Boston, (États-Unis) (membre étranger), 1994
- Romanian Academy of Medical Sciences, Bucarest (membre étranger), 1996
- Institute of Medicine of the National Academies, Washington, (États-Unis) (membre étranger associé), 2000
- Istituto Veneto di Scienze, Lettere Ed Arti, Venezia (Italie), 2001
- Hungarian Academy of Sciences, Budapest (membre étranger associé), 2004
- European Academy of Sciences, Bruxelles (membre), 2004
- Académie royale de Belgique, Bruxelles (membre), 2010[70].
- Docteur honoris causa de :
- Université de Turin, Italie, 1989
- Université de Dundee, Écosse, 1992
- Université de Genève, Suisse, 1994
- Université de Stockholm, Suède, 1994
- Université de Liège, Belgique, 1996
- École polytechnique fédérale de Lausanne, Suisse, 1996
- Université de Californie du Sud, Los Angeles, USA, 1997
- Université de Bath, Royaume-Uni, 1997
- Université de Montréal, Canada, 2000
- Université hébraïque de Jérusalem, Israël, 2004
- Université d'État de l'Ohio, Colombus, États-Unis, 2007
- HEC Paris, France, 2011[71]
- Membre honoraire du Neurosciences Research Program, MIT et Université Rockefeller (États-Unis), depuis 1984
- Membre honoraire de la Japanese Biochemical Society, Sendai, Japon, 1985
- Membre honoraire de l'American Neurology Association, 1988
- Membre honoraire de University College de Londres, Londres, 1990
- Membre honoraire à titre étranger de la Société belge de neurologie, Bruxelles, 1991
- Membre de l'Organisation européenne de biologie moléculaire
Distinctions
Articles scientifiques majeurs
- Monod J, Wyman J, Changeux JP (1965). On the nature of allosteric transitions: a plausible model. Journal of Molecular Biology 12: 88-118. Article classique où Jacques Monod, Jeffries Wyman et Jean-Pierre Changeux présentent le modèle MWC, qui explique les propriétés de coopérativité que l'on trouve dans les protéines allostériques, comme l'hémoglobine.
- Changeux JP, Kasai M, Lee CY (1970). Use of a snake venom toxin to characterize cholinergic receptor protein. Proceedings of the National Academy of Sciences USA 67: 1241-1247 (première purification d'un récepteur de neurotransmetteur).
- Changeux JP, Courrege P, Danchin A (1973). Theory of epigenesis of neuronal networks by selective stabilization of synapses. Proceedings of the National Academy of Sciences USA 70: 2974-2978.
- Giraudat J, Dennis M, Heidmann T, Chang JY, Changeux JP (1986). Structure of the high affinity site for noncompetitive blockers of the acetylcholine receptor: serine-262 of the delta subunit is labeled by [3H]-chlorpromazine. Proceedings of the National Academy of Sciences USA 83: 2719-2723.
Livres par Jean-Pierre Changeux
Neurosciences
- Changeux, Jean-Pierre. La beauté dans le cerveau. Odile Jacob, Paris (2016).
- Changeux, Jean-Pierre. Le cerveau et l'art. De Vive Voix, Paris (2010).
- Changeux, Jean-Pierre. (2008) Du vrai, du beau, du bien : Une nouvelle approche neuronale. ed. Odile Jacob, Paris.
- Changeux, Jean-Pierre ; Stuart Edelstein. (2004) Nicotinic Acetylcholine Receptors: From Molecular Biology to Cognition. Odile Jacob, New York.
- Gènes et culture, collectif sous la direction de Jean-Pierre Changeux, Odile Jacob, Paris, 2003.
- La Vérité dans les sciences, collectif sous la direction de Jean-Pierre Changeux, Odile Jacob, Paris, 2003.
- Changeux, Jean-Pierre. (2002) L'Homme de vérité. Odile Jacob, Paris (2004 The physiology of truth).
- Changeux, Jean-Pierre ; Paul Ricœur. (1998) Ce qui nous fait penser. Odile Jacob, Paris (2002 What Makes Us Think. À Neuroscientist and a Philosopher Argue About Ethics, Human Nature, and the Brain [63][64]).
- Changeux, Jean-Pierre. (1994) Raison et plaisir. Odile Jacob, Paris.
- Changeux, Jean-Pierre ; Alain Connes. (1989) Matière à pensée. Odile Jacob, Paris (1995 Conversations on Mind, Matter and Mathematics).
- Changeux, Jean-Pierre. (1983) L'Homme neuronal. Fayard Paris (1985 Neuronal Man: The Biology of Mind).
Éthique
- Une même éthique pour tous, collectif sous la direction de Jean-Pierre Changeux, Odile Jacob, Paris, 1997.
- Fondements naturels de l'éthique, Odile Jacob, Paris, 1993.
Arts
- La Lumière au siècle des Lumières et aujourd'hui, collectif sous la direction de Jean-Pierre Changeux, Odile Jacob, Paris, 2005.
- Jean-Pierre Changeux, Nicole Rouillé, Jean-Claude Boyer, Pierre Rosenberg, La Passion de l'âme : peintures des XVIIe et XVIIIe siècles de la collection Changeux, 2006, Odile Jacob.
- Article paru dans Art Aujourd’hui : Changeux et l'art.
- Les Neurones enchantés - Le cerveau et la musique, Entretiens avec Pierre Boulez et Philippe Manoury, Paris, Odile Jacob, 2014.
Notes et références
- Collectif La Recherche, Les grandes controverses scientifiques, Paris, Dunod, , 166 p. (ISBN 978-2-10-071033-1), p. 123 à 132
- Changeux J.-P. (1961). The feedback control mechanism of biosynthetic L-threonine deaminase by L-isoleucine. Cold Spring Harbor. Symp. Quant. Biol. 26: 313-318.
- Changeux J.-P. (1963). Allosteric Interactions on biosynthetic L-theonine deaminase from E. coli K12. Cold Spring Harb Symp Quant Biol, 28: 497-504
- Monod J., Changeux J.-P., and Jacob. F. (1963). Allosteric proteins and cellular control systems. J. Mol. Biol. 6: 306-329
- Monod J., Wyman J., and Changeux J.-P. (1965). On the nature of allosteric transitions: a plausible model. J. Mol. Biol. 12: 88-118.
- Rubin M.M., Changeux J.-P. (1966). On the nature of allosteric transitions ; implications of non exclusive ligand binding. J. Mol. Biol. 21: 265-274.
- Changeux J.-P., Thiéry J.-P., Tung Y., and Kittel C. (1967). On the cooperativity of biological membranes. Proc. Natl. Acad. Sci. USA 57, 335-341.
- Bray D, Levin MD, Morton-Firth CJ (1998) Receptor clustering as a cellular mechanism to control sensitivity. Nature, 393: 85-88.
- Changeux J.-P., Podleski T.R. (1968). On the excitability and cooperativity of electroplax membrane. Proc. Natl. Acad. Sci. USA 59:944-950
- Cartaud J., Benedetti E.L., Cohen J.B., Meunier J.C., Changeux J.-P. (1973) Presence of a lattice structure in membrane fragments rich in nicotinic receptor protein from the electric organ of Torpedo marmorata. FEBS Lett. 33: 109-113.
- Weber M., David-Pfeuty M.T., Changeux J.-P. (1975). Regulation of binding properties of the nicotinic receptor protein by cholinergic ligands in membrane fragments from Torpedo marmorata. Proc. Natl. Acad. Sci. USA 72: 3443-3447.
- Sugiyama H., Changeux J.-P. (1975). Interconversion between different states of affinity for acetylcholine of the cholinergic receptor protein from Torpedo marmorata. Eur. J. Biochem. 55: 505-515.
- Heidmann T., Changeux J.-P. (1979). Fast kinetic studies on the interaction of a fluorescent agonist with the membrane-bound acetylcholine receptor from T. marmorata. Eur. J. Biochem. 94: 255-279.
- Edelstein S., Schaad O., Henry E., Bertrand D. Changeux J.-P. (1996). A kinetic mechanism for nicotinic acetylcholine receptors based on multiple allosteric transitions. Biol. Cybern. 75: 361-379.
- Le Novère N., Grutter T., Changeux J.-P. (2002). Models of the extracellular domain of the nicotinic receptors and of agonist and Ca++ binding sites. Proc. Natl. Acad. Sci. USA, 99: 3210-3215.
- Changeux J.-P., Kasai M., Huchet M., Meunier J.-C. (1970). Extraction à partir du tissu électrique de gymnote d'une protéine présentant plusieurs propriétés caractéristiques du récepteur physiologique de l'acétylcholine. C. R. Acad. Sci. 270D: 2864-2867.
- Changeux J.-P., Kasai M., and Lee C.Y. (1970). The use of a snake venom toxin to characterize the cholinergic receptor protein. Proc. Natl. Acad. Sci. USA 67: 1241–1247.
- Miledi R., Molinoff P., Potter L.T. (1971). Isolation of the cholinergic receptor protein of Torpedo electric tissue. Nature 229:554-557.
- Olsen R., Meunier J.C., Changeux J.-P. (1972). Progress in purification of the cholinergic receptor protein from Electrophorus electricus by affinity chromatography. FEBS Lett. 28., 96-100.
- Hucho F., Changeux J.-P. (1973). Molecular weight and quaternary structure of the cholinergic receptor protein extracted by detergents from Electrophorus electricus electric tissue. FEBS Lett. 38: 11-15
- Weill C.L., McNamee M.G., Karlin A. (1974) Affinity-labeling of purified acetylcholine receptor from Torpedo Californica. Biochemical and Biophysical Research Communications 61: 997-1003.
- Devillers-Thiéry A., Changeux J.-P., Paroutaud P., and Strosberg A.D. (1979). The amino-terminal sequence of the 40.000 molecular weight subunit of the acetylcholine receptor protein from Torpedo marmorata. FEBS Lett. 104: 99-105.
- Devillers-Thiéry A., Giraudat J., Bentaboulet M., Changeux J.-P. (1983). Complete mRNA coding sequence of the acetylcholine binding alpha subunit of Torpedo marmorata acetylcholine receptor: a model for the transmembrane organization of the polypeptide chain. Proc. Natl. Acad. Sci. USA 80: 2067-2071.
- Noda M., Takahashi H., Tanabe T., Toyosato M., Furutani Y., Hirose T., Asai M., Inayama S., Miyata T., Numa S. (1982) Primary structure of alpha-subunit precursor of Torpedo californica acetylcholine receptor deduced from cDNA sequence. Nature 299:793-797.
- Ballivet M., Patrick J., Lee J., Heinemann S. (1982) Molecular cloning of cDNA coding for the gamma subunit of Torpedo acetylcholine receptor. Proc Natl Acad Sci U S A. 79:4466-4470.
- Giraudat J., Dennis M., Heidmann T., Chang J.Y., Changeux J.-P. (1986). Structure of the high affinity site for noncompetitive blockers of the acetylcholine receptor: serine-262 of the delta subunit is labeled by [3H]-chlorpromazine. Proc. Natl. Acad. Sci. USA 83: 2719-2723.
- Imoto K., Methfessel C., Sakmann B., Mishina M., Mori Y., Konno T., Fukuda K., Kurasaki M., Bujo H., Fujita Y., Shosaku N. (1986). Location of a delta-subunit region determining ion transport through the acetylcholine receptor channel. Nature. 1986 Dec 18-31;324(6098):670-4.
- Hucho F., Oberthür W., Lottspeich F. (1986) The ion channel of the nicotinic acetylcholine receptor is formed by the homologous helices M II of the receptor subunits. FEBS Lett.205: 137-142.
- Galzi J.-L., Devillers-Thiery A., Hussy N., Bertrand S., Changeux J.-P., Bertrand D. (1992). Mutations in the ion channel domain of a neuronal nicotinic receptor convert ion selectivity from cationic to anionic. Nature 359: 500-505.
- Bertrand D., Galzi J.-L., Devillers-Thiéry A., Bertrand S., Changeux J.-P. (1993). Mutations at two distinct sites within the channel domain M2 alter calcium permeability of neuronal alpha7 nicotinic receptor. Proc. Nat. Acad. Sci. USA 90: 6971-6975.
- Corringer P.-J., Bertrand S., Galzi J.-L., Devillers-Thiéry A., Changeux J.-P., Bertrand D. (1999). Mutational Analysis of the Charge Selectivity Filter of the a7 Nicotinic Acetylcholine Receptor. Neuron 22: 831-843.
- Dennis M., Giraudat J., Kotzyba-Hibert F., Goeldner M., Hirth C., Chang J.Y., Lazure C., Chrétien M., Changeux J.-P. (1988). Amino acids of the Torpedo marmorata acetylcholine receptor subunit labeled by a photoaffinity ligand for the acetylcholine binding site. Biochemistry 27: 2346-2357.
- Galzi J.-L., Revah F., Black D., Goeldner M., Hirth C., Changeux J.-P. (1990). Identification of a novel amino acid a-Tyr 93 within the active site of the acetylcholine receptor by photoaffinity labeling: additional evidence for a three-loop model of the acetylcholine binding site. J. Biol. Chem. 265: 10430-10437.
- Galzi J.-L., Bertrand D., Devillers-Thiéry A., Revah F., Bertrand S., Changeux J.-P. (1991). Functional significance of aromatic amino acids from three peptide loops of the alpha 7 neuronal nicotinic receptor site investigated by site-directed mutagenesis. FEBS Lett. 294: 198-202.
- Bocquet N., Nury H., Baaden M., Le Poupon C., Changeux J.-P., Delarue M., Corringer P.-J. (2008) X-ray structure of a pentameric ligand-gated ion channel in an apparently open conformation. Nature. Nov 5.
- Changeux J.-P., Courrège P., Danchin A. (1973). A theory of the epigenesis of neural networks by selective stabilization of synapses. Proc. Nat. Acad. Sci. USA 70: 2974-2978.
- Sébastien Lemerle, « Les habits neufs du biologisme en France », Actes de la recherche en sciences sociale, nos 176-177, , p. 75.
- Changeux J.-P., Danchin, A. (1976). Selective stabilization of developing synapses as a mechanism for the specificication of neuronal networks. Nature 264: 705-712.
- Sotelo C., Changeux J.-P. (1974). Transsynaptic degeneration 'en cascade' in the cerebellar cortex of staggerer mutant mice. Brain Res. 67: 519-526.
- Mariani J., Crepel F., Mikoshiba K., Changeux J.-P. (1977). Anatomical, physiological and biochemical studies of the cerebellum from reeler mutant mouse. Phyl. Trans. Royal Soc. B 281: 1-28.
- Benoit P, Changeux J.P. (1975) Consequences of tenotomy on the evolution of multiinnervation in developing rat soleus muscle. Brain Res.99:354-8.
- Henderson CE, Huchet M, Changeux JP. Denervation increases a neurite-promoting activity in extracts of skeletal muscle. Nature. 1983 Apr 14;302(5909):609-11.
- Betz H., Changeux J.-P. (1979). Regulation of muscle acetylcholine receptor synthesis in vitro by cyclic nucleotide derivatives. Nature 278: 749-752.
- Klarsfeld A., Changeux J.-P. (1985). Activity regulates the level of acetylcholine receptor alpha-subunit mRNA in cultured chick myotubes. Proc. Natl. Acad. Sci. USA 82: 4558-4562.
- Klarsfeld A., Laufer R., Fontaine B., Devillers-Thiéry A., Dubreuil C., Changeux J.-P. (1989). Regulation of muscle AChR alpha-subunit gene expression by electrical activity : involvement of protein kinase C and Ca++. Neuron 2: 1229-1236.
- Piette J., Bessereau J.-L., Huchet M., Changeux J.-P. (1990). Two adjacent MyoD1-binding sites regulate the expression of the acetylcholine receptor delta-subunit gene. Nature 345: 353-355.
- Fontaine B., Klarsfeld A., Hokfelt T., Changeux J.-P. (1986). Calcitonin gene-related peptide, a peptide present in spinal cord motoneurons, increases the number of acetylcholine receptors in primary cultures of chick embryo myotubes. Neurosci. Lett. 71: 59-65.
- Fontaine B., Klarsfeld A., Changeux J.-P. (1987). Calcitonin-gene related peptide and muscle activity regulate acetylcholine receptor alpha-subunit mRNA levels by distinct intracellular pathways. J. Cell Biol. 105: 1337-1342.
- Laufer R., and Changeux J.-P. (1987). Calcitonin gene-related peptide elevates cyclic AMP levels in chick skeletal muscle : possible neurotrophic role for a coexisting neuronal messenger. EMBO J. 6: 901-906.
- Altiok N., Bessereau J.-L., Changeux J.-P. (1995). ErB3 and ErbB2/neu mediate the effect of heregulin on acetylcholine receptor gene expression in muscle : differential expression at the endplate. EMBO J. 14: 4258-4266.
- Schaeffer L., Duclert N., Huchet-Dymanus M., Changeux J.-P. (1998). Implication of a multisubunit Ets related transcription factor in synaptic expression of the nicotinic acetylcholine receptor. EMBO J., 17: 3078-3090.
- Mulle C., Choquet D., Korn H., Changeux J.-P. (1992). Calcium influx through nicotinic receptor in rat central neurons : Its relevance to cellular regulation. Neuron 8: 135-143.
- Léna C, Changeux, JP (1997). Role of Ca2+ ions in nicotinic facilitation of GABA release in mouse thalamus. J Neurosci 17: 576-585.
- Mulle C., Léna C., Changeux J.-P. (1992). Potentiation of nicotinic receptor response by external calcium in rat central neurons. Neuron 8: 937-945.
- Vernino S, Amador M, Leutje CW, Patrick J, and Dani JA (1992) Calcium modulation and high calcium permeability of neuronal nicotinic acetylcholine receptors. Neuron 8: 127-134
- Galzi J.-L., Bertrand S., Corringer P.-J., Changeux J.-P., Bertrand D. (1996). Identification of calcium binding sites that regulate potentiation of a neuronal nicotinic acetylcholine receptor. EMBO J. 15: 5824-5832.
- Le Novère N., Zoli M., Changeux J.-P. (1996). Neuronal nicotinic receptor a6 subunit mRNA is selectively concentrated in catecholaminergic nuclei of the rat brain. Eur J Neurosci 8: 2428-2439
- Klink R., de Kerchove d'Exaerde A., Zoli M., Changeux J.-P. (2001). Molecular and Physiological Diversity of Nicotinic Acetylcholine Receptors in the Midbrain Dopaminergic Nuclei. J. Neurosci. 21: 1452-1463.
- Champtiaux N, Gotti C, Cordero-Erausquin M, David DJ, Przybylski C, Lena C, Clementi F, Moretti M, Rossi FM, Le Novere N, McIntosh JM, Gardier AM, Changeux JP (2003) Subunit composition of functional nicotinic receptors in dopaminergic neurons investigated with knock-out mice. J Neurosci., 2003 Aug 27;23(21):7820-9.
- Picciotto M.R., Zoli M., Rimondini R., Léna C., Marubio L., Merlo Pich E., Fuxe K., Changeux J.-P. (1998). Acetylcholine receptors containing the b2-subunit are involved in the reinforcing properties of nicotine. Nature 391: 173-177 (1998).
- Maskos U., Molles B.E, Pons S., Besson M., Guiard B.P., Guilloux J.P., Evrard A., Cazala P., Cormier A., Mameli-Engvall M., Dufour N., Cloz-Tayarani I., Bemelmans A.-P., Mallet J., Gardier A.M., David V., Faure P., Granon S. and Changeux J.-P. (2005) Nicotine reinforcement and cognition restored by targeted expression of nicotinic receptors. Nature 436: 103-107
- David Leloup et Stéphane Foucart, « Comment le lobby du tabac a subventionné des labos français », sur lemonde.fr,
- Dehaene S., Changeux J.-P., Nadal J.P. (1987). Neural networks that learn temporal sequences by selection. Proc. Natl. Acad. Sci. USA 84: 2727-2731.
- Dehaene S., Changeux J.-P. (1993). Development of elementary numerical abilities : a neuronal model. J. Cognitive Neurosci 5: 390-407.
- Dehaene S., Kerszberg M., Changeux J.-P. (1998). A neuronal model of a global workspace in effortful cognitive tasks. Proc Natl Acad Sci USA 95: 14529-14534.
- Dehaene S., Sergent C., Changeux J.-P. (2003) A neuronal network model linking subjective reports and objective physiological data during conscious perception. Proc. Natl. Acad. Sci. USA, 100: 8520-8525.
- Jean-Pierre Changeux, mécène de la peinture française, http://www.canalacademie.com/Les-passions-de-l-ame.html
- CNRS, « Liste des médaillés d'or du CNRS », sur http://www.cnrs.fr (consulté le ).
- (en) « International research award from the Olav Thon Foundation 2016 » (consulté le ).
- Écouter le discours de réception à l'Académie royale de Belgique, prononcé le 29 mai 2010
- HEC, « Jean-Pierre Changeux, Professeur Honoris Causa d’HEC Paris » (consulté le )
- Décret du 31 décembre 2010 portant élévation aux dignités de grand'croix et de grand officier du JORF no 0001 du , page 8, texte no 1.
- Décret du 3 décembre 1994 portant élévation à la dignité de grand'croix et de grand officier
- Archives des nominations et promotions dans l'ordre des Arts et des Lettres.
Liens externes
- Notices d'autorité :
- Fichier d’autorité international virtuel
- International Standard Name Identifier
- Bibliothèque nationale de France (données)
- Système universitaire de documentation
- Bibliothèque du Congrès
- Gemeinsame Normdatei
- Bibliothèque nationale de la Diète
- Bibliothèque nationale d’Espagne
- Bibliothèque royale des Pays-Bas
- Bibliothèque universitaire de Pologne
- Bibliothèque nationale tchèque
- Bibliothèque nationale du Portugal
- WorldCat Id
- WorldCat
- Ressources relatives à la recherche :
- Ressource relative à la santé :
- Notices dans des dictionnaires ou encyclopédies généralistes :
- Entretien sur Du vrai, du beau, du bien (Odile Jacob, 2008)
- Jean-Pierre Changeux - L'homme de l'art - Article du 04-05-03
- Discours de réception de Jean-Pierre Changeux à l'Académie royale de Belgique, le 29 mai 2010, en accès libre sur le site de l'Académie.
- 1983 : L'homme neuronal par Jean-Pierre Changeux - LExpress.fr (Article: Par Françoise Monier (Lire), publié le 01/11/2005)
- Portail des sciences
- Portail des neurosciences
- Portail des arts
- Portail de la bioéthique
- Portail de la France