Bleu de trypan
Le bleu de trypan est un colorant d'exclusion utilisé pour colorer sélectivement les tissus ou cellules morts. C'est un colorant azoïque.
| Bleu de trypan | |

| |
| Identification | |
|---|---|
| Nom UICPA | 3,3'-[(3,3'-diméthyl[1,1'-biphényl]-4,4'-diyl)bis(azo)]bis[5-amino-4-hydroxynaphtalène-2,7-disulfonate] de tétrasodium |
| Synonymes |
C.I. 23850 |
| No CAS | |
| No ECHA | 100.000.715 |
| No CE | 200-786-7 |
| PubChem | 5904246 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C34H28N6Na4O14S4 [Isomères] |
| Masse molaire[1] | 964,837 ± 0,055 g/mol C 42,32 %, H 2,93 %, N 8,71 %, Na 9,53 %, O 23,22 %, S 13,29 %, |
| Propriétés physiques | |
| T° fusion | > 300 °C[2] |
| Précautions | |
| Directive 67/548/EEC | |
 T |
|
| Écotoxicologie | |
| DL50 | 328 mg·kg-1 (souris, i.v.)[3] 267 mg·kg-1 (souris, s.c.)[4] |
| LogP | -0,120[2] |
| Unités du SI et CNTP, sauf indication contraire. | |
Le bleu de trypan est aussi connu sous le nom de bleu diamine et de bleu Niagara.
Chimie
Le bleu de trypan est dérivé de la ditoluidine (C14H16N2). Le bleu de trypan est ainsi nommé parce qu’il tue les trypanosomes, parasites responsables notamment de la maladie du sommeil. Un analogue du bleu de trypan, la suramine, est utilisé en pharmacie contre la trypanosomiase.
Le rouge de trypan et le bleu de trypan furent synthétisés pour la première fois par le chimiste allemand Paul Ehrlich en 1904.
Coloration au bleu de trypan
Principe
La coloration au bleu de trypan est une méthode de coloration des cellules mortes.
Chez une cellule vivante, le bleu trypan ne peut pas pénétrer la membrane intacte, contrairement aux cellules mortes dont les membranes sont altérées[5],[6]. Ainsi les cellules mortes sont colorées bleu alors que les cellules vivantes ne le sont pas[7]. C'est un mode d'action similaire à l'iodure de propidium qui ne rentre uniquement dans les cellules mortes, du fait que leurs membranes soient altérées.
Outre son effet tératogène[8],[9],[10] dangereux pour l'utilisateur, le bleu trypan est également cytotoxique[11],[12] et finira ainsi par colorer la totalité de la population cellulaire après un délai variable en fonction de la lignée considérée, habituellement de l'ordre de plusieurs heures. Il est utilisé par la quasi-totalité des automates de comptage cellulaires actuellement sur le marché, et reste au laboratoire la seule technique de dénombrement manuel utilisable en routine. L'emploi de méthodes par fluorescence (iodure de propidium,DAPI), basées sur le même principe d'exclusion et également génotoxiques est parfois privilégié lorsque les techniques d'imagerie idoines sont disponibles.
Utilisation
Cette méthode est couramment utilisée lors de numération cellulaire. On utilise alors un hémocytomètre afin de compter les cellules dans un volume précis.
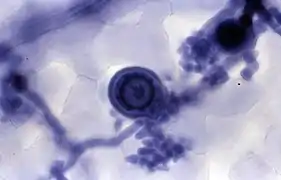
On peut également utiliser cette coloration pour visualiser les cellules mortes et les hyphes de champignon et Stramenopiles.
Cette méthode ne permet pas de distinguer les cellules mortes par apoptose des cellules nécrosées.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Bleu de trypan », sur NIST/WebBook, consulté le 12/05/2010
- Toxicology and Applied Pharmacology. Vol. 23, Pg. 537, 1972. PMID
- Naunyn-Schmiedebergs Archiv fuer Pharmakologie. Vol. 267, Pg. 31, 1970. PMID
- (en) « Viability using Trypan Blue », sur https://www.nexcelom.com/
- (en) I-Ju Fang, Brian G. Trewyn, « Methods in Enzymology », sur https://www.sciencedirect.com, (consulté le )
- http://www.champignons-passion.be/TrypanBleu.pdf Source douteuse
- A. N. Barber et J. C. Geer, « STUDIES ON THE TERATOGENIC PROPERTIES OF TRYPAN BLUE AND ITS COMPONENTS IN MICE », Journal of Embryology and Experimental Morphology, vol. 12, , p. 1–14 (ISSN 0022-0752, PMID 14155404, lire en ligne, consulté le )
- F. Beck et J. B. Lloyd, « DOSAGE-RESPONSE CURVES FOR THE TERATOGENIC ACTIVITY OF TRYPAN BLUE », Nature, vol. 201, , p. 1136–1137 (ISSN 0028-0836, PMID 14152802, lire en ligne, consulté le )
- J. G. Wilson, A. R. Beaudoin et H. J. Free, « Studies on the mechanism of teratogenic action of trypan blue », The Anatomical Record, vol. 133, , p. 115–128 (ISSN 0003-276X, PMID 13670433, lire en ligne, consulté le )
- (en) K. Mascotti, J. McCullough et S.r. Burger, « HPC viability measurement: trypan blue versus acridine orange and propidium iodide », Transfusion, vol. 40, , p. 693–696 (ISSN 1537-2995, DOI 10.1046/j.1537-2995.2000.40060693.x, lire en ligne, consulté le )
- (en) K. H. Jones et J. A. Senft, « An improved method to determine cell viability by simultaneous staining with fluorescein diacetate-propidium iodide. », Journal of Histochemistry & Cytochemistry, vol. 33, , p. 77–79 (ISSN 0022-1554 et 1551-5044, PMID 2578146, DOI 10.1177/33.1.2578146, lire en ligne, consulté le )
Source
- Portail de la biologie cellulaire et moléculaire
- Portail de la chimie