Biomarqueur
Un biomarqueur est une caractéristique biologique mesurable liée à un processus normal ou non[1].
Dans le domaine de l'écologie, un biomarqueur est un changement observable ou mesurable au plan moléculaire (génétique, biochimique), cellulaire ou physiologique qui révèlent l'exposition présente ou passée d'un organisme vivant à une substance chimique ou à un autre facteur de stress. Il révèle donc aussi la présence actuelle ou passée de polluants dans l'environnement et/ou l'impact de certaines pratiques. Ce peut être par exemple le nombre de poissons dans un lac, la quantité et le type de lichens sur les arbres d'une forêt, la couleur du pelage des animaux ou un taux anormal d'hormone de stress ou d'un enzyme de détoxication dans un organisme.
Dans le domaine médical, un biomarqueur peut être utilisé pour le dépistage médical (recherche d'une maladie dans une population), le diagnostic (caractérisation d'une maladie chez un individu), la réponse à un traitement médical, la rechute après un traitement, la toxicité d'une molécule. Le biomarqueur est alors le plus souvent une protéine (dosable dans le sang ou la présence d'une molécule dans l'urine).
En écologie
Un biomarqueur est un changement observable et/ou mesurable au niveau moléculaire, biochimique, cellulaire, physiologique, qui révèle l'exposition présente ou passée d'un individu à au moins une substance chimique à caractère polluant[2],[3].
Types de biomarqueurs
Le principe de l'utilisation d'un « biomarqueur » est de rechercher la signature biologique de l'impact (actuel ou passé) ou de la présence d'un xénobiotique dans l'organisme, ou de l'effet induit d'un changement ou stress environnemental (ex. : pollution thermique, pollution lumineuse induisant, déshydratation, perturbateur endocrinien..), et non la mise en évidence directe de la cause
Certains biomarqueurs (ex. : cerne des arbres...) révèlent des évènements anciens (contact avec un toxique, un pathogène, un évènement climatique...).
Exemple de biomarqueur
L'activité enzymatique EROD chez certains poissons (cyprinidés) a été proposée comme biomarqueur de la présence de certains polluants (HAP, PCB et dioxines) dans l'environnement aquatique de cours d'eau français, qui pourraient ainsi être suivis ponctuellement (pour vérifier si une pollution accidentelle a eu des impacts par exemple) ou en utilisant ces poissons comme sentinelles à long terme (analyse en routine). Ceci nécessite cependant préalablement d'avoir vérifié que le biomarqueur est bien spécifique de ces polluants et de connaître son expression chez des poissons en bonne santé, toute l'année, dans un environnement pas ou peu pollué par ces produits[4].
En médecine

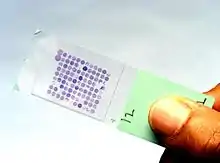
Historique de quelques biomarqueurs
En 1848, la chaine légère de l'immunoglobuline est identifiée comme étant présente chez 75 % des patients atteint d'un myélome (Protéine de Bence-Jones).
Dans les années 1960, découverte de l'alpha-fœtoprotéine et de l'antigène carcino-embryonnaire comme marqueurs de cancer.
Dans les années 1980, découverte du CA 125 comme marqueur dans le cancer de l'ovaire et de l'antigène prostatique spécifique dans le cancer de la prostate.
La recherche de biomarqueurs
Quelques précisions sur l'utilisation du terme « clinique » et ses différentes utilisations sont nécessaires[réf. nécessaire] :
- pour un test, « clinique » signifie que le test est utilisable en routine. Idéalement, ce test doit être peu coûteux, peu invasif, ne doit pas nécessiter un appareillage lourd et doit être relativement rapide ;
- pour une étude, « clinique » signifie que l'étude est réalisée sur l'homme (en premier lieu sur des personnes saines puis sur des malades), et non sur des modèles expérimentaux (animaux, cellules en culture) comme ce qui est réalisé en phase « pré-clinique »[5] ;
- pour une maladie, « clinique » signifie que des symptômes sont visibles lors d'un examen de routine, par exemple lors d'une consultation chez son médecin traitant (douleurs, rougeurs, masses palpables, etc.) La maladie est « préclinique » ou asymptomatique avant l'apparition des premiers symptômes.
La découverte de nouveaux biomarqueurs est souvent liée au développement d'une nouvelle technologie, par exemple, l'alpha-fœtoprotéine et de l'antigène carcino-embryonnaire après le développement des techniques immunologiques. Actuellement, des techniques telles que les biopuces ou la protéomique semblent offrir de nombreuses perspectives[6].
Le EDRN[7] recommande un processus en 5 étapes pour le développement d'un biomarqueur[8] :
- Phase exploratoire de recherche de biomarqueurs candidats lors d'une étude préclinique sur quelques dizaines ou centaines de patients comparant un groupe « malade » versus un groupe « sain ».
- Développement d'un test clinique reproductible sur un échantillon représentatif de la population ciblée.
- Étude clinique rétrospective permettant de valider la capacité du biomarqueur à détecter la maladie en phase préclinique (c'est-à-dire avant l'apparition des symptômes).
- Étude clinique prospective à long terme sur la population ciblée pour déterminer l'utilité du biomarqueur.
- Étude prospective à long terme pour valider le biomarqueur.
Valider un biomarqueur reste un processus long et complexe, ce qui explique leur faible nombre en routine. Pour faciliter l'utilisation des biomarqueurs en cours de développement dans des études cliniques, le centre d'Oxford EBM[9] a décrit une classification des biomarqueurs en fonction de leurs niveau de preuve[10][source insuffisante] :
- (Plus haut niveau de validation) : biomarqueur validé par une étude clinique prospective randomisée sur la population et sur le long terme.
- biomarqueur validé par une étude prospective sur un échantillon de la population.
- biomarqueur validé par une étude rétrospective sur un échantillon représentatif de la population.
- biomarqueur validé par une étude rétrospective sur un échantillon non représentatif de la population.
- (Plus faible niveau de validation) : biomarqueur validé en laboratoire uniquement.
Recherche
Les biomarqueurs suscitent un intérêt croissant. Par exemple, en Allemagne, pour mieux détecter les signes prédictifs ou précoces de certaines maladies (cancer de la vessie ou du foie, maladies d'Alzheimer ou de Parkinson), le land de Rhénanie-du-Nord-Westphalie (RNW) propose 37 millions d'euros pour créer un « Centre de recherche sur les protéines » dit Pure (Protein Research Unit Ruhr within Europe) sur le Campus-Santé RNW de l'Université de la Ruhr à Bochum)[11].
Autre exemple, Ellen Jorgensen, de 2001 à 2009, comme directrice de la recherche et développement de biomarqueurs à Vector Research, publie ses travaux, en particulier les premiers biomarqueurs des maladies pulmonaires liées au tabac[12] .
Notes et références
- (en) Biomarkers working group, « Biommarkers and surrogate endpoints: preffered definition and conceptual framework », Clin. Pharmacol. Ther., vol. 69, , p. 89-95.
- Lagadic L, Caquet T, Amiard J.C & Ramade F (1997) Biomarqueurs en écotoxicologie : Aspects fondamentaux. Collection Écologie, Paris, Masson, 419 p
- Jean-Claude Amiard, Claude Amiard-Triquet, coord., « Les biomarqueurs dans l'évaluation de l'état écologique des milieux aquatiques », Ed Tec & Doc, lavoisier, 2008, 978-2-7430-1017-1
- Mesure d'un biomarqueur de pollution chez des poissons d'eau douce. Validation et optimisation Measurement of a pollution biomarker for freshwater fish. Assesment and optimisation, Flammarion, 126 pages, Coll. Études du Cemagref, série Gestion des milieux aquatiques n° 15 (ISBN 2-85362-521-4) (Voir)
- Roselelyne Boulieu, Initiation à la connaissance du médicament, Ellipses,
- (en) Kulasingam V, Diamandis EP, « Strategies for discovering novel cancer biomarkers through utilization of emerging technologies », Nature Clinical Practice Oncology, vol. 5, no 10, , p. 588-599 (lire en ligne [PDF])
- Early Detection Research Network, qui peut se traduire par « Réseau de recherche sur la détection précoce », du NCI (National Cancer Institut, l'institut américain du cancer)
- (en) Pepe MS, Etzioni R, Feng Z et al., « Phases of biomarkers development for early detection of cancer », J Natl Cancer Inst, vol. 93, , p. 1054-1061 (lire en ligne [PDF])
- Evidence Based Medecine, signifiant médecine basée sur les faits.
- « Levels of evidence », BJU Int, vol. 101, , p. 150
- BE Allemagne N°466, (2010/01/15) Ambassade de France en Allemagne / ADIT.
- (en) « Ellen Jorgensen », ResearchGate, (lire en ligne, consulté le ).
Voir aussi
Articles connexes
Liens externes
- CancerDriver, une base de données ouverte sur les biomarqueurs en oncologie avec des liens vers les articles de référence et les essais cliniques ouverts.
- Biomarqueursinfos.fr Site d'information sur les biomarqueurs, avec des vidéos de conférences en ligne.
- Portail de la biologie
- Portail de la médecine