Bêta-oxydation
La β-oxydation est la principale voie métabolique de dégradation des molécules d'acides gras pour produire :
- d'une part de l'acétyl-CoA, dont le groupe acétyle est oxydé par le cycle de Krebs
- et d'autre part du NADH et du FADH2, dont les électrons à haut potentiel alimentent la chaîne respiratoire.
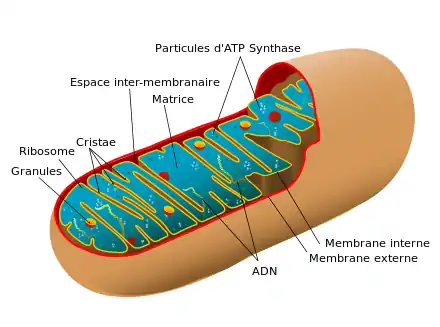
Dans les cellules eucaryotes, la β-oxydation se déroule en aérobiose dans la matrice mitochondriale, mais aussi dans d'autres organites que sont les peroxysomes et, chez les plantes, les glyoxysomes.
Activation des acides gras et transport par la navette de la carnitine
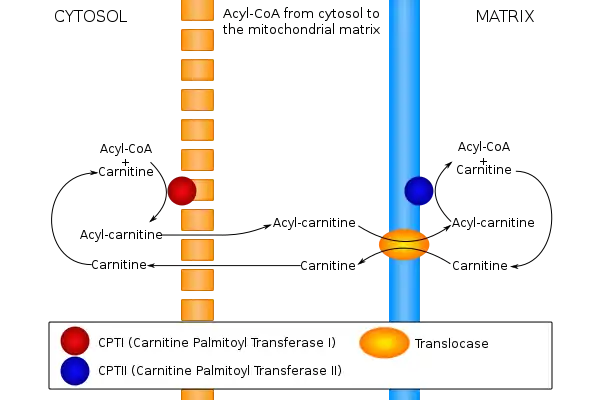
Les acides gras sont dégradés dans les mitochondries sous forme d'acyl-CoA. Ces derniers se forment sous l'action d'une acyl-CoA synthétase, qui catalyse la réaction :
Le pyrophosphate formé est rapidement hydrolysé dans le cytosol, ce qui déplace l'équilibre de la réaction vers la formation d'acyl-CoA. Le mécanisme réactionnel implique le passage par un intermédiaire acyladénylate. Les acides gras à chaîne courte peuvent diffuser à travers les membranes mitochondriales, de sorte que leur activation en acyl-CoA peut être réalisée au sein de la matrice mitochondriale ; en revanche, les acides gras à chaîne plus longue doivent être activés dans le cytosol et franchir les membranes mitochondriales en utilisant la navette de la carnitine. Ils sont dans ce cas convertis en acylcarnitine par transfert du groupe acyle sur une molécule de carnitine sous l'action d'une carnitine acyltransférase de la membrane mitochondriale externe (CPTI).
L'acylcarnitine peut alors pénétrer dans l'espace intermembranaire mitochondrial à travers une porine de la membrane externe, puis franchir la membrane mitochondriale interne en empruntant la carnitine-acylcarnitine translocase, qui fonctionne comme un antiport permettant d'échanger une molécule de carnitine de la matrice mitochondriale contre une molécule d'acylcarnitine de l'espace intermembranaire.
Une fois parvenues dans la matrice, les molécules d'acylcarnitine peuvent restituer leur groupe acyle à une coenzyme A sous l'action d'une carnitine acyltransférase de la membrane interne (CPTII) afin de redonner de l'acyl-CoA.
La β-oxydation peut alors commencer.
Dans les mitochondries
Acides gras saturés
Dans les mitochondries, la dégradation des acides gras saturés par la β-oxydation fait intervenir quatre réactions qui se déroulent dans la matrice mitochondriale.
| Réaction | Enzyme | Description |
|---|---|---|
 |
Acyl-CoA déshydrogénase | Déshydrogénation par le FAD. La déshydrogénation, en présence de FAD, catalysée par une oxydo-réductase, l'acyl-CoA déshydrogénase, a lieu entre les carbones β et α (carbones 2 et 3 dans la nomenclature IUPAC). Il y a formation de trans-Δ2-énoyl-CoA en Cn.
Le FADH2 est oxydé par la chaîne respiratoire avec libération d'énergie sous forme d'ATP. |
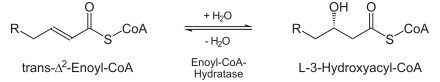 |
Énoyl-CoA hydratase | Hydratation. Cette réaction d'addition est catalysée par une crotonase du groupe des lyases. Du fait de la proximité du groupe cétone, la double liaison est polarisée (le carbone β est δ+, le carbone α est δ-) : le groupe OH de l'eau se lie au carbone β avec formation de L-β-hydroxyacyl-CoA en Cn.
Cette réaction réversible est stéréospécifique et aboutit à l'isomère L. |
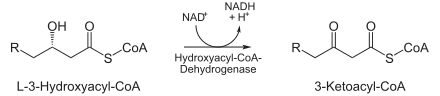 |
3-hydroxyacyl-CoA déshydrogénase | Oxydation par le NAD+ avec formation de β-cétoacyl-CoA en Cn.
Le NADH est oxydé par la chaîne respiratoire avec libération d'énergie sous forme d'ATP. |
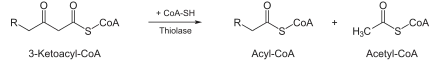 |
Acétyl-CoA C-acyltransférase | Thiolyse. Cette réaction est catalysée par une transférase, la β-cétothiolase, en présence de coenzyme A, et conduit à la formation :
|
La dégradation complète de l'acide gras se poursuit jusqu'à ce que la chaîne carbonée soit complètement découpée en molécules d'acétyl-CoA : c'est l'hélice de Lynen. Chaque tour de l'hélice raccourcit l'acyl-CoA de deux atomes de carbone et libère une molécule d'acétyl-CoA, une molécule de FADH2 et une molécule de NADH. Cette dégradation intervient par oxydations sur les carbones β successifs (étapes hydratation et thiolyse ci-dessus), d'où le terme de « β-oxydation ».
À nombre pair d'atomes de carbone
Dans le cas des acides gras saturés à nombre pair d'atomes de carbone, le dernier tour de l'hélice de Lynen conduit à la formation de deux molécules d'acétyl-CoA, d'une molécule de FADH2 et d'une molécule de NADH. Chacune des molécules d'acétyl-CoA peut alors être oxydée par le cycle de Krebs ou au contraire servir à des biosynthèses.
À nombre impair d'atomes de carbone
Dans le cas des acides gras saturés à nombre impair d'atomes de carbone, le dernier tour de l'hélice de Lynen conduit à la formation d'une molécule de propionyl-CoA, d'une molécule d'acétyl-CoA, d'une molécule de FADH2 et d'une molécule de NADH.
La propionyl-CoA est d'abord carboxylée par un ion bicarbonate HCO3– sous l'action de la propionyl-CoA carboxylase pour donner de la D-méthylmalonyl-CoA au cours d'une réaction impliquant un cofacteur biotine et l'hydrolyse d'une molécule d'ATP. La méthylmalonyl-CoA épimérase donne la L-méthylmalonyl-CoA, laquelle est convertie en succinyl-CoA par la méthylmalonyl-CoA mutase, une enzyme nécessitant un cofacteur B12 (cobalamine). La succinyl-CoA étant un intermédiaire du cycle de Krebs, c'est à ce niveau que la propionyl-CoA rejoint ce dernier.
Cependant, la succinyl-CoA n'alimente pas le cycle de Krebs en atomes de carbone à oxyder, elle ne fait qu'augmenter le nombre d'intermédiaires du cycle de Krebs présents dans la cellule. Si ceux-ci dépassent la demande cataplérotique, par exemple afin de produire de l'aspartate ou du glutamate, une partie de l'oxaloacétate du cycle peut être orientée vers la néoglucogenèse via le phosphoénolpyruvate par la phosphoénolpyruvate carboxykinase :
- GTP + oxaloacétate → GDP + phosphoénolpyruvate + CO2.
Acides gras insaturés
La β-oxydation des acides gras insaturés pose un problème particulier dû à la présence éventuelle d'une ou de plusieurs doubles liaisons mal positionnées empêchant la formation d'une double laison trans-Δ2 par l'acyl-CoA déshydrogénase.
Ainsi, la dodécénoyl-CoA isomérase convertit les liaisons cis-Δ3 ou trans-Δ3 en liaison trans-Δ2, qui est un substrat enzymatique pour l'acyl-CoA déshydrogénase.
La présence d'une liaison Δ4 ne bloque pas l'oxydation, qui donne deux doubles liaisons Δ2,Δ4 ; en revanche, cette configuration est bloquante pour l'énoyl-CoA hydratase et nécessite l'action d'une 2,4-diénoyl-CoA réductase pour convertir les liaisons trans-Δ2,trans-Δ4 ou trans-Δ2,cis-Δ4 en liaison trans-Δ2.
Enfin, dans les cas des acides gras polyinsaturés, la Δ3,5-Δ2,4-diénoyl-CoA isomérase est nécessaire pour convertir les liaisons Δ3,Δ5 en liaisons Δ2,Δ4, configuration qui peut être traitée par la 2,4-diénoyl-CoA réductase, puis par l'énoyl-CoA hydratase.
Dans les peroxysomes

Dans les peroxysomes, ce sont avant tout les acides gras à longue et très longue chaîne qui sont dégradés, jusqu'à l'octanoyl-CoA — avec un résidu d'acide gras en C8. On pense que les acides gras à longue chaîne — à 22 atomes de carbone et plus — commencent par être oxydés dans les peroxysomes avant d'être entièrement dégradés par β-oxydation dans les mitochondries.
Une différence essentielle de l'oxydation des acides gras dans les peroxysomes par rapport aux mitochondries est que la première étape de cette dégradation est réalisée par une enzyme spécifique, l'acyl-CoA oxydase (EC ), qui catalyse la réaction :
Ainsi, contrairement à l'acyl-CoA déshydrogénase, les électrons à haut potentiel ne sont pas récupérés sous forme de FADH2 permettant de libérer leur énergie métabolique sous forme d'ATP par la chaîne respiratoire ; à la place, on obtient du peroxyde d'hydrogène H2O2, dont la catalase, enzyme spécifique aux peroxysomes, catalyse ensuite la dismutation en eau H2O et oxygène O2.
Une autre particularité des peroxysomes est que l'énoyl-CoA hydratase et la 3-hydroxyacyl-CoA déshydrogénase y sont présentes sous forme d'un complexe enzymatique multifonctionnel, alors qu'elles sont distinctes dans les mitochondries.
Par ailleurs, la β-oxydation dans les peroxysomes requiert une carnitine acyltransférase peroxisomale, distincte des CPTI et CPTII mitochondriales, afin de permettre aux résidus acyle à très longue chaîne de traverser la membrane de cet organite.
De plus, les acides gras à longue chaîne métabolisés dans les peroxysomes y sont importés non pas à l'aide de la navette de la carnitine, mais à l'aide d'une protéine ABCD1 (en) de la famille des transporteurs ABC ; la mutation du gène codant cette protéine chez l'homme est responsable d'une maladie génétique, l'adrénoleucodystrophie liée à l'X[1],[2], qui se traduit par une démyélinisation progressive du système nerveux central et l'accumulation d'acides gras linéaires saturés à très longue chaîne, notamment l'acide cérotique (C26:0).
Enfin, la β-cétothiolase peroxysomale est également distincte de celle des mitochondries, avec une affinité différente pour les substrats ; elle n'est notamment efficace que sur les acides gras à plus de huit atomes de carbone, d'où l'accumulation d'octanoyl-CoA, qui doit être oxydé dans les mitochondries.
Rendement énergétique
L'activation d'un acide gras en acyl-CoA par l'acyl-CoA synthétase consomme l'équivalent de deux molécules d'ATP, car l'ATP est hydrolysée en AMP et non en ADP au cours de cette réaction :
Par ailleurs, chaque tour de l'hélice de Lynen libère une molécule d'acétyl-CoA, une molécule de FADH2 et une molécule de NADH. Le NADH et le FADH2 permettent chacun de produire respectivement 2,5 et 1,5 molécules d'ATP environ grâce à la chaîne respiratoire. L'acétyl-CoA produit au cours de la β-oxydation est prioritairement dégradé par le cycle de Krebs :
La CoQ10H2 permet de produire environ 1,5 molécules d'ATP grâce à la chaîne respiratoire, de sorte que l'oxydation complète du résidu acétyle de l'acétyl-CoA permet de produire 10 ATP, ce qui porte à 14 le nombre d'ATP produits par tour de l'hélice de Lynen en prenant en compte les 2,5 + 1,5 = 4 ATP issus du NADH et du FADH2 de la β-oxydation.
Enfin, dans le cas d'un acide gras à nombre pair d'atomes de carbone, la dernière molécule d'acétyl-CoA peut également être oxydée en libérant 10 ATP. Ainsi, la β-oxydation suivie de la dégradation par le cycle de Krebs d'un acide gras saturé à n = 2p atomes de carbone libère (10p – 2) ATP + (p – 1) × (FADH2 + NADH+H+), soit avec la chaîne respiratoire :
- 106 ATP pour une molécule d'acide palmitique CH3(–CH2)14–COOH, qui contient 16 atomes de carbone (n = 16, et donc p = 8) ;
- 44 ATP pour une molécule d'acide caproïque CH3(–CH2)4–COOH, qui contient 6 atomes de carbone (n = 6, et donc p = 3) ;
A titre de comparaison, l'oxydation complète d'une molécule de glucose, qui contient également 6 atomes de carbone, s'écrit selon l'équation :
- Glucose + 10 NAD+ + 2 CoQ10 + 2 ADP + 2 GDP + 4 Pi + 2 H2O → 10 (NADH + H+) + 2 CoQ10H2 + 2 ATP + 2 GTP + 6 CO2,
ce qui correspond à environ 32 ATP. Ainsi, par rapport au glucose, l'acide caproïque permet de libérer un surcroît de 37,5 % d'énergie métabolique à nombre d'atomes de carbone égal ; d'une manière générale, les acides gras sont sensiblement plus énergétiques que les oses.
Cas particulier de l'acide phytanique

L'acide phytanique est un acide gras saturé terpénoïde, donc ramifié, apporté dans l'organisme par le régime alimentaire. Il ne peut être dégradé directement par β-oxydation car le carbone β est porteur d'un groupe méthyle. Il doit donc au préalable subir une α-oxydation pour « raccourcir » la chaîne aliphatique d'un atome de carbone et faire en sorte que le groupe méthyle soit porté par le carbone α, permettant à la β-oxydation d'avoir lieu.
La phytanoyl-CoA est ainsi convertie en pristanoyl-CoA dans les peroxysomes, où la pristanoyl-CoA peut commencer à être dégradée par β-oxydation jusqu'à ne plus avoir qu'une chaîne de longueur moyenne ; à ce stade, la molécule doit migrer dans une mitochondrie pour que la β-oxydation puisse se poursuivre jusqu'à dégradation complète du composé.
Chaque molécule de pristanoyl-CoA entièrement dégradée par β-oxydation libère ainsi trois molécules de propionyl-CoA, trois molécules d'acétyl-CoA et une molécule d'isobutyryl-CoA.
Notes et références
- (en) Hugo W Moser, Asif Mahmood et Gerald V Raymond, « X-linked adrenoleukodystrophy », Nature Reviews Neurology, vol. 3, , p. 140-151 (lire en ligne) DOI:10.1038/ncpneuro0421
- (en) Clementina Dellomonaco, James M. Clomburg, Elliot N. Miller et Ramon Gonzalez, « Engineered reversal of the β-oxidation cycle for the synthesis of fuels and chemicals », Nature, vol. 476, , p. 355-359 (lire en ligne) DOI:10.1038/nature10333
Voir aussi
- Lipolyse
- Cycle de Krebs
- Chaîne respiratoire
- Alpha-oxydation
- Oméga-oxydation
- Cétogenèse
- Néoglucogenèse
- Métabolisme
- Portail de la biochimie