Équilibre thermique
En physique statistique et en thermodynamique, lorsque deux corps de températures différentes entrent en contact, ils échangent de l’énergie thermique. Lorsque leur température respective devient égale, ils se trouvent en équilibre thermique.
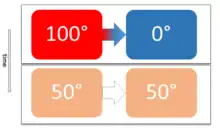
Température d'équilibre thermique
La température d'équilibre thermique est atteinte lorsqu'un corps ayant une température plus élevée transfère de l'énergie thermique à un autre corps ayant une température plus basse, selon le principe zéro de la thermodynamique. Ce transfert s'effectue jusqu'à ce que les deux corps soient à la même température.
Calcul
Supposons une évolution dans laquelle un corps 1, ayant une température élevée, transmet de l'énergie thermique à un corps 2, ayant une température basse. En l'absence de tout autre échange d'énergie, l'énergie dégagée par le corps 1 est entièrement récupérée par le corps 2, ce qu'on peut traduire par :
[Équation 1]
Où :
- est la capacité thermique massique (anciennement chaleur massique ou chaleur spécifique) du corps 1, en joules par kilogramme et par kelvin (J·kg-1·K-1)
- est la masse du corps 1, en kilogrammes (kg).
- est la température du corps 1, en kelvins (K).
- est la température d'équilibre thermique, en kelvins (K).
- est la capacité thermique massique (anciennement chaleur massique ou chaleur spécifique) du corps 2, en joules par kilogramme et par kelvin (J·kg-1·K-1)
- est la masse du corps 2, en kilogrammes (kg).
- est la température du corps 2, en kelvins (K).
De cette équation 1, on peut tirer :
Remarque : cette relation reste valable si toutes les températures sont exprimées en °C, étant alors également obtenue en °C.
- Portail de la physique