< Carbonyles

Addition nucléophile
Bilan

Ces réactions ne sont pas stéréosélectives, on obtient le composé en mélange racémique.
Sans catalyse
Ces équilibres sont atteints très lentement sans catalyse. On est alors sous contrôle cinétique.
Mécanisme :

La première étape est cinétiquement déterminante.
Avec catalyse
- En milieu acide : la protonation de la fonction carbonyle via l'atome d'oxygène rend l'attaque nucléophile plus facile. L'atome de carbone est rendu plus électrophile par appauvrissement électronique:
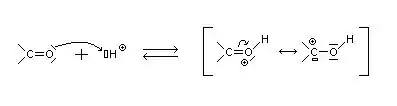
- En milieu basique : l'ionisation du réactif Nu-E est favorisée lorsque l'atome nucléophile est porteur d'un atome hydrogène labile (alcool, amine). Toutefois, une base est bien souvent un réactif nucléophile, il faut donc éviter la compétition avec le réactif nucléophile de la réaction.
Ce type de réactions est l’objet des 3 chapitres suivants.
Cet article est issu de Wikiversity. Le texte est sous licence Creative Commons - Attribution - Partage dans les Mêmes. Des conditions supplémentaires peuvent s'appliquer aux fichiers multimédias.