Canagliflozine
La canagliflozine est une molécule approuvée pour le traitement du diabète de type 2.
| Canagliflozine | |
 | |
| Identification | |
|---|---|
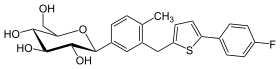
| Nom UICPA | (2S,3R,4R,5S,6R)-2-{3-[5-[4-fluorophényl)-thiophén-2-ylméthyl]-4-methylphéyl}-6-hydroxyméthyltétrahydropyran-3,4,5-triol |
| No CAS | |
| No ECHA | 100.223.671 |
| Code ATC | « BX11 » |
| DrugBank | DB08907 |
| ChEBI | 73274 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule brute | C24H25FO5S [Isomères] |
| Masse molaire[1] | 444,516 ± 0,027 g/mol C 64,85 %, H 5,67 %, F 4,27 %, O 18 %, S 7,21 %, |
| Données pharmacocinétiques | |
| Biodisponibilité | 65 % |
| Liaison protéique | 99 % |
| Métabolisme | hépatique |
| Demi-vie d’élim. | 10–13 heures |
| Excrétion |
fécale et rénale |
| Considérations thérapeutiques | |
| Voie d’administration | orale |
| Unités du SI et CNTP, sauf indication contraire. | |
Historique
La molécule a été découverte au Japon en 2010[2] par Mitsubishi Tanabe[3].
Elle a été approuvée par l'EMA (European Medicines Agency) le 15 novembre 2013[4].
Mode d'action
Il s'agit d'un inhibiteur de la SGLT2, co-transporteur du sodium et du glucose situé sur le tubule rénale et permettant la réabsorption du glucose dans les urines. La canaglifozine augmente par conséquent la glycosurie (taux de sucre dans les urines).
Efficacité
Dans un modèle animal de diabète, elle améliore la fonction des cellules bêta pancréatiques et diminue le gain de poids[5].
Elle améliore le contrôle de la glycémie chez le diabète de type 2 sous insuline[6]. En association avec la metformine, elle s'avère supérieure au glimépiride dans le contrôle de l'hémoglobine glyquée[7]. Elle permet une diminution du poids concernant essentiellement la masse grasse, une diminution de la pression artérielle sans modification de la fréquence cardiaque[7]. par contre, elle augmente le taux sanguin de LDL cholestérol ce qui est théoriquement délétère.
Il diminue le risque de survenue d'une maladie cardio-vasculaire[8], en particulier chez le patient porteur d'une insuffisance cardiaque[9].
Effets indésirables
Cette molécule comme les autres inhibiteurs de la SGLT2 exposerait les patients à un risque augmenté d’amputation des membres inférieurs[10],[8].
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Nomura S, Sakamaki S, Hongu M et al. Discovery of canagliflozin, a novel C-glucoside with thiophene ring, as sodium-dependent glucose cotransporter 2 inhibitor for the treatment of type 2 diabetes mellitus, J Med Chem, 2010;53:6355-6360
- 1. J Med Chem. 2010 Sep 9;53(17):6355-60. doi: 10.1021/jm100332n.
- http://www.ema.europa.eu/ema/index.jsp?curl=pages/medicines/human/medicines/002649/human_med_001707.jsp&mid=WC0b01ac058001d124
- Liang Y, Arakawa K, Ueta K et al. Effect of canagliflozin on renal threshold for glucose, glycemia, and body weight in normal and diabetic animal models, PLoS One, 2012;7:e30555
- Devineni D, Morrow L, Hompesch M et al. Canagliflozin improves glycemic control over 28 days in subjects with type 2 diabetes not optimally controlled on insulin, Diabetes Obes Metab, 2012;14:539-545
- Cefalu WT, Leiter LA, Yoon K-H et al. Efficacy and safety of canagliflozin versus glimepiride in patients with type 2 diabetes inadequately controlled with metformin (CANTATA-SU): 52 week results from a randomised, double-blind, phase 3 non-inferiority trial, Lancet, 2013;382:941-950
- Neal B, Perkovic V, Mahaffey KW et al. Canagliflozin and cardiovascular and renal events in type 2 diabetes, N Engl J Med, 2017;377:644-657
- Rådholm K, Figtree G, Perkovic V et al. Canagliflozin and heart failure in type 2 diabetes mellitus, results from the CANVAS program, Circulation, 2018;138:458-468
- Actualité de l'Agence National de Sécurité du Médicament
- Portail de la médecine
- Portail de la chimie
- Portail de la pharmacie