Étohexadiol
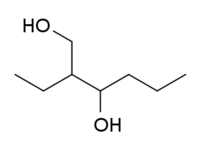
L'étohexadiol, 2-éthylhexane-1,3-diol ou encore octylène glycol est un composé organique de la famille des diols. Il est utilisé comme ectoparasiticide.
| Étohexadiol | |
 | |
| Identification | |
|---|---|
| Nom UICPA | 2-éthylhexane-1,3-diol |
| Synonymes |
octylène glycol |
| No CAS | |
| No ECHA | 100.002.162 |
| No EC | 202-377-9 |
| Code ATC | P03 |
| PubChem | 7211 |
| SMILES | |
| InChI | |
| Apparence | liquide incolore et inodore[1] |
| Propriétés chimiques | |
| Formule brute | C8H18O2 [Isomères] |
| Masse molaire[2] | 146,2273 ± 0,0083 g/mol C 65,71 %, H 12,41 %, O 21,88 %, |
| Propriétés physiques | |
| T° fusion | −40 °C[1] |
| T° ébullition | 243 °C[1] |
| Solubilité | 42 g·l-1 (eau, 20 °C)[1] |
| Masse volumique | 0,94 g·cm-3[1] |
| T° d'auto-inflammation | 340 °C[1] |
| Point d’éclair | 127 °C[1] |
| Pression de vapeur saturante | 0 01 hPa (20 °C)[1] |
| Précautions | |
| SGH[1] | |
 |
|
| Transport[1] | |
| non-soumis à régulation | |
| Écotoxicologie | |
| DL50 | 1 400 mg·kg-1 (rat, oral)[3] 2 000 mg·kg-1 (lapin, dermique)[4] |
| Unités du SI et CNTP, sauf indication contraire. | |
C'est un liquide très peu inflammable, soluble dans l'eau et légèrement volatil[1].
Stéréochimie
La molécule d'étohexadiol possède deux atomes de carbone asymétriques et pas de plan de symétrie. Il existe donc deux paires d'énantiomères, diastéréoisomères entre elles de l'étohexadiol :
- (2R,3R)-2-éthylhexane-1,3-diol
- (2S,3S)-2-éthylhexane-1,3-diol
- (2R,3S)-2-éthylhexane-1,3-diol
- (2S,3R)-2-éthylhexane-1,3-diol
Notes et références
- Entrée de « 2-Ethylhexane-1,3-diol » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 1à mars 2012 (JavaScript nécessaire)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Special Publication of the Entomological Society of America. Vol. 78-1, Pg. 52, 1978.
- Pesticide Manual. Vol. 1, Pg. 208, 1968.
- Portail de la chimie
- Portail de la pharmacie
- Portail de la parasitologie
This article is issued from
Wikipedia.
The text is licensed under Creative Commons - Attribution - Sharealike.
Additional terms may apply for the media files.